Основные способы репликации днк
Деление клеток происходит посредством митоза, при этом, во избежание потери генетической информации, вначале удваивается весь ядерный геном в S-фазе клеточного цикла. Продолжительность S-фазы составляет 8 ч. ДНК центромер хромосом реплицируется во время средней стадии митоза, что предшествует процессу сегрегации хромосом.
Репликация митохондриальной и ядерной ДНК происходит в разные фазы клеточного цикла. Несмотря на то что общая последовательность стадий при репликации ядерной ДНК у высших существ (эукариот) и у бактерий (прокариот) одинакова, сам процесс имеет незначительные отличия. Так, у эукариот во время репликации ДНК (ядерная) остаётся в нуклеосомной конфигурации.
Фрагменты ДНК, богатые парами оснований Г—Ц (R-полосы эухроматина в уплотнённом хроматине), экспрессируют гены «домашнего хозяйства», которые функционируют во всех клетках организма. Данные фрагменты реплицируются на ранней стадии S-фазы. Участки гетерохроматина, богатые парами оснований А—Т (G-полосы), экспрессируют небольшое количество генов и реплицируются на поздней стадии S-фазы.
Гены с большим содержанием пар А—Т, кодирующие различные свойства и функционирующие лишь в определённых клетках, входят в состав факультативного гетерохроматина. Их репликация происходит на ранней стадии S-фазы только в тех клетках, в которых они экспрессируются, и на поздних стадиях — в клетках, где экспрессии не происходит.
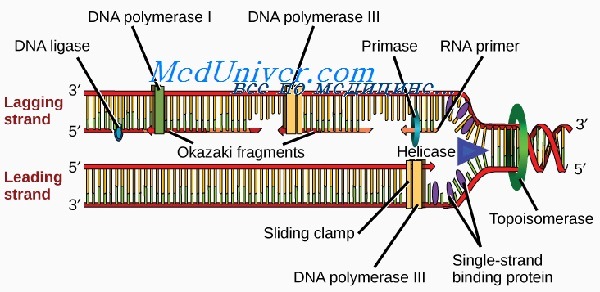
Область спирали ДНК, которая в начале репликации раскручивается в первую очередь, называют участком начала репликации (репликоном). В этом месте двойную нить расплетает фермент хеликаза, раскрывающий последовательность оснований. Процесс репликации происходит вдоль одной цепи со скоростью примерно 40-50 нуклеотидов в секунду одновременно в обоих направлениях. У высших существ имеется множество репликонов, расположенных на расстоянии 50 000—300 000 п.н. В месте разделения нити ДНК возникают репликационные вздутия, на каждом конце которого формируется репликационная вилка.
Новая ДНК синтезируется при участии ферментов, называемых ДНК-полимеразами, из дезоксирибонуклеотидтрифосфатов (АТФ, ГТФ и др.), которые превращаются в монофосфатные нуклеотиды (АМФ, ГМФ и др.). Отщепление и гидролиз пирофосфатов из трифосфатов обеспечивают процесс энергией и обусловливают его полную необратимость, делая молекулу ДНК достаточно устойчивой.
Все ДНК-полимеразы могут выстраивать новую ДНК только в направлении от 5′- к 3′-концу. Это означает, что ферменты должны двигаться вдоль матричной цепи от 3′- к 5′-концу. В связи с этим репликация может непрерывно происходить от репликона только по одной цепи, называемой опережающей. Из-за расположения Сахаров репликация по второй, отстающей цепи происходит только на коротких отрезках, известных как фрагменты Оказаки.
Длина новых фрагментов ДНК, образующихся вдоль отстающей цепи, в среднем составляет 100—200 пар нуклеотидов. Во время синтеза фрагменты Оказаки сшивает между собой фермент ДНК-лигаза. В ожидании репликации стабильность первичной одноцепочечной нуклеотидной последовательности отстающей цепи поддерживается белком, связывающим одноцепочечную ДНК (или спиральдестабилизирующим белком).
Для синтеза опережающей цепи необходим фермент ДНК-полимераза S, а для синтеза отстающей — ДНК-полимераза а. Последняя имеет субъединицу, называемую ДНКпраймазой, которая синтезирует короткую РНК-затравку, играющую роль праймера. Репликация мито-хондриальной ДНК происходит независимо от процессов в ядре. При этом используется ряд других ферментов, один из которых — ДНК-полимераза у.
В геноме присутствует большое количество копий пяти гистонных генов, благодаря чему происходит синтез множества гистонов (особенно во время S-фазы), которые сразу после репликации связываются с новой цепью ДНК.
Следует отметить, что процесс репликации носит название полуконсервативного, так как в состав дочерних молекул ДНК входит одна первичная цепь и одна синтезированная.
Репликация теломер ДНК
Основной проблемой синтеза ДНК на конце отстающей цепи служит то, что ДНК-полимеразе а необходимо прикрепиться выше конца последовательности, которая реплицирована, и работать проксимально в направлении от 5′- к 3′-концу. Для решения этой проблемы нужен ДНК-синтетический фермент теломераза, который продлевает отстающую цепь.
Теломераза — рибонуклеопротеин, содержащий матричную РНК с последовательностью 3′-ААУЦЦЦААУ-5′, которая комплементарна полутора повторам шестиосновной теломерной ДНК (5′-ГГГТТА-3′). Фрагмент последовательности 3′-ААУ РНК-теломеразы связывается с терминальным концом ТТА-5′ матричной отстающей цепи, при этом остальная часть РНК остаётся свободной. Затем к этой матричной РНК присоединяются дезоксирибонуклеотиды, тем самым продлевая повторяющуюся последовательность в ДНК на один сегмент.
После этого теломераза отщепляется и направляется к другому терминальному концу с последовательностью ТТА-5′, и процесс повторяется. Как только возникает достаточно длинный терминальный повтор, ДНК-полимераза а прикрепляется к полученному одноцепочечному фрагменту и достраивает вторую цепь по методу комплементарности в проксимальном 5’—3′-направлении, двигаясь к уже существующему двухцепочечному участку, последующее слияние с которым происходит благодаря действию ДНК-лигазы.
Репаративные механизмы ДНК
Иногда в растущую цепь случайно вклинивается неправильное основание, однако, к счастью, у здоровых клеток присутствуют пострепликационные репаративные ферменты и система коррекции ошибочного спаривания оснований, которые исправляют подобные ошибки. В основе механизма действия данных систем лежат удаление и замена ошибочно вставленных оснований в соответствии с последовательностью матричной цепи. Для их функционирования необходимы ДНК-полимеразы b и е.
Значение ДНК для медицины. Патология пострепликационных механизмов репарации иногда обусловливает предрасположенность пациентов к некоторым онкологическим заболеваниям. К ним относят синдром множественной ломкости хромосом (синдром Блума), наследственную предрасположенность к раку молочной железы, вызванную мутациями генов BRCA1 и BRCA2, и аутосомно-доминантную форму рака кишечника (наследственный неполипозный рак толстой кишки).
Существует теория, утверждающая, что после каждого клеточного цикла теломеры укорачиваются на один повтор, а следовательно, количество делений клетки ограничено числом повторов в теломерной цепи. Согласно этому бесконечный рост и деление опухолевых клеток происходят из-за присутствия активных мутантных теломераз, которые препятствуют разрушению теломер.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в содержание раздела «генетика» на нашем сайте
Источник
Основные способы репликации днк
• Репликация происходит после прохождения клеткой точки рестрикции или START
• Репликация регулируется поэтапно и скоординирована с наступлением митоза
• Репликация происходит в точках инициации, которые могут обладать особой первичной структурой, специфическим положением, или располагаться в ДНК на определенных расстояниях
• Инициация происходит только в разрешенных точках, способных к репликации
• Осуществив свои функции, до наступления следующего цикла, точки начала репликации не могут использоваться повторно
Когда клетки проанализировали состояние окружающей среды и приняли решение вступить в цикл деления, они проходят точку G1/S и начинают репликацию ДНК. Как клетки объединяют и активируют факторы, необходимые для репликации ДНК? Какие механизмы контроля гарантируют, что клетка лишь однажды реплицировала ДНК, и только один раз в цикле?
Хотя пока невозможно дать полные ответы на эти вопросы, в результате идентификации и анализа последовательности дрожжевых хромосомных ДНК, способных к независимой репликации, было получено много информации о самом процессе репликации ДНК Эти последовательности в хромосоме, называемые автономно реплицирующиеся последовательности (ARS), являются частью точек начала репликации. Точка инициации или начала (ориджин репликации) представляет собой участок последовательности ДНК, на котором начинается репликация.
У почкующихся дрожжей, но не у большинства других организмов, точки начала репликации представлены небольшими консенсусными последовательностями. У сливающихся дрожжей эти точки занимают большие участки ДНК, богатые АД парами, но не отличаются какой-то особой структурой. У остальных эукариот точки начала репликации расположены случайно, в соответствии с распределением по геному белков, неспецифически связанных с ДНК.
Для того чтобы гарантировать своевременную дупликацию генома, на хромосоме должно быть достаточное количество точек начала репликации. У бактерий для репликации единственной кольцевой хромосомы необходима лишь одна точка начала, однако у эукариот, имеющих большой геном, распределенный по многим линейным хромосомам, должно быть много точек начала репликации. У почкующихся дрожжей, величина генома которых составляет около 13 Мб, в 16 хромосомах находится примерно 400 точек начала репликации.
Это создает несколько проблем, связанных с регуляцией процесса репликации. Функционирование точек начала репликации должно быть скоординировано с клеточным циклом таким образом, чтобы репликация начиналась только в течение S фазы. Должна быть полная уверенность в том, что репликация завершилась до перехода клетки в митоз. Каждая из точек начала репликации должна функционировать только один раз, с тем чтобы гарантировать, что ДНК реплицируется лишь один раз за цикл.
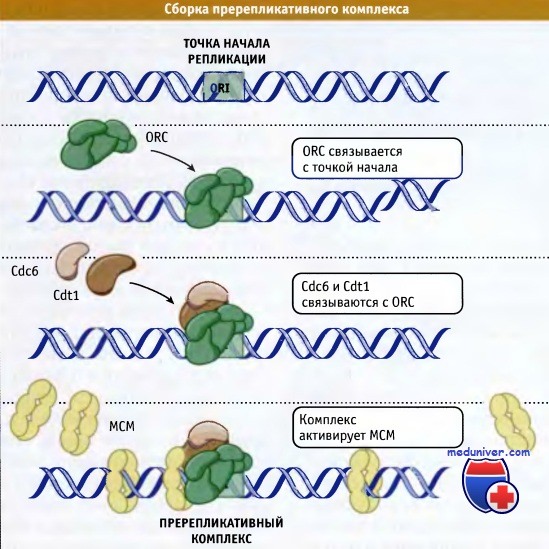
В течение короткого промежутка времени, от поздего митоза до G1, с точкой начала также связываются белки, активирующие репликацию,
Cdc6 и Cdt1, что, в свою очередь, активирует гексамерный МСМ геликазный комплекс (МСМ2-7).
Этот этап завершает снятие блока репликации и сборку пре-RC.
Точки начала репликации связывают факторы, необходимые для активации репликации и инициации синтеза ДНК. Инициация репликации ДНК происходит только в тех точках, которые содержат связанные факторы и которые поэтому относятся к разрешенным точкам. Однако в каждом раунде репликации ДНК в процессе участвует ограниченный набор потенциальных начальных точек, присутствующих в хромосомах. Более того, по мере активации в разное время различных разрешенных начальных точек, события инициации также происходят через различные интервалы времени. Например, некоторые точки активируются в ранней S-фазе, а другие переходят в это состояние позже.
Неизвестно, чем задается этот временной фактор, но похоже, что расположение специфической точки начала репликации на хромосоме определяет время ее наступления.
Ддя того чтобы репликация началась, в точке начала должен сформироваться пререпликативный комплекс (pre-RC). В результате проведения генетических исследований на дрожжах и биохимических экспрериментов на экстрактах яйцеклеток Xenopus, выяснилась картина сборки pre-RC. Процесс начинается со связывания с ДНК комплекса из шести белков, который носит название комплекса, распознающего область начала репликации (origin recognition complex, ORC). Этот комплекс помечает потенциальную точку начала репликации, однако его недостаточно для активации. Он служит платформой для связывания еще двух консервативных белков: Cdc6, который относится к семейству ААА+АТФазы, и Cdt1. (Многие белки, обладающие АТФазным доменом, для выполнения работы используют энергию АТФ.)
Затем к ним присоединяется комплекс поддерживающий минихромосому (minichromosome maintenance complex, МСМ), представляющий собой кольцевую структуру, состоящую из шести родственных белков, которые также относятся к большому семейству ААА+АТФаз. Комплексы МСМ присутствуют в избытке и распространяются за пределы точки начала репликации. После присоединения МСМ, ORC и Cdc6 становятся необязательными компонентами и pre-RC переходит в состояние способное к активации. Порядок событий, происходящих при сборке pre-RC в точках начала репликации, схематически представлен на рисунке ниже.
Сборка pre-RC ограничена промежутком между концом М-фазы и ранней S-фазой, что объясняется следующими причинами. Во-первых, в клетке уровень белка Cdc6 контролируется таким образом, что он присутствует только в этот промежуток времени. В отсутствие белка Cdc6, МСМ белок не связывается с точкой начала репликации. Во-вторых, у Метазоа, белок Cdt1 негативно регулируется другим белком, геминином, который блокирует его активность во всех периодах, за исключением окна в G1. Наконец, сборка самого pre-RC ограничивается активностью митотического CDK-циклинового комплекса.
Субстратами для этого комплекса являются субъединицы ORC, Cdc6 и МСМ. При фосфорилировании Cdc6 инактивируется, а фосфорилирование белка МСМ в S-фазе вызывает его отщепление от ДНК. Поэтому pre-RC может сформироваться только при низкой активности CDK-циклинового комплекса. Это характерно для промежутка между уровнями высокой активности митотического комплекса CDK-циклина в М-фазе, и в S-фазе, когда она снова увеличивается, способствуя активации точки начала репликации.
Каким образом точка начала репликации переходит из пререпликативного в репликативное состояние? Для такого перехода необходимо формирование многих дополнительных белковых комплексов, и процесс находится под контролем двух киназ, комплекса CDK-циклин и Cdc7-Dbf4 (DDK). Таким образом, активность CDK-циклинового комплекса координирует процессы репликации и клеточного цикла. При этом координация может носить как негативный (предотвращая сборку pre-RC и, таким образом, повторное функционирование точек начала репликации), так и позитивный характер (промотируя активацию точек начала репликации). К числу вопросов, ожидающих своего ответа, относится вопрос относительно субстратов киназ, промотирующих инициацию репликации.
Если комплексы CDK-циклин обеспечивают координацию процессов во всем цикле, то DDK действует на уровне отдельных точек, инициирующих синтез ДНК. К числу наиболее известных субстратов этой киназы относятся сами МСМ-белки. Интересно, что точечная мутация в гене Mcm5 отменяет необходимость присутствия DDK. Это позволяет предполагать, что фосфорилирование приводит к изменению струтуры белка МСМ, что служит причиной инициации репликации. Впрочем, имеющиеся данные свидетельствуют о том, что эти изменения крайне незначительны. На показаны контрольные процессы репликации ДНК с участием CDK и DDK.
Вероятно, лимитирующим процессом инициации репликации в отдельных начальных точках является связывание белка Cdc45, для которого необходимы как CDK-циклиновый комплекс, так и DDK. Связывание этого белка, которое сопровождается образованием дополнительного комплекса, называемого GINS, приводит к раскручиванию спирали ДНК в начальной точке, за счет активации комплекса МСМ, действующего как хеликаза. Таким образом, МСМ превращается из фактора сборки, участвующего в формировании pre-RC, в фермент хеликазу, который является частью комплекса элонгации. Раскручивание двойной спирали ДНК в точке начала репликации приводит к образованию однонитевой ДНК, которая связывает специфический белок RPA, относящийся к группе белков, связывающихся с однонитевой ДНК (ssDNA binding proteins).
В свою очередь, белок RPA способствует связыванию комплекса праймаза/ДНК-полимераза альфа, который инициирует синтез ДНК. Комплекс МСМ и Cdc45 движется вдоль ДНК, формируя расширяющуюся репликативную вилку, которая образует большую реплисому, включающую в основном ДНК-полимеразу 6, а не полимеразу а. Процессы инициации репликации ДНК представлены на рисунке ниже. В поддержании функционирования реплисомы и защите ДНК в области репликативной вилки от повреждений участвуют контрольные точки и системы репарации ДНК.
Как только МСМ отошли от точки начала репликации, она считается «использованной» и не может активироваться повторно до окончания следующей М-фазы, пока в начальной точке снова не сформируется pre-RC. По мере прохождения S-фазы, МСМ удаляются из хроматина. Наряду с этим, при движении репликативной вилки устанавливаются связи, соединяющие вместе до наступления митоза вновь образованные сестринские хроматиды. Таким образом, завершение S-фазы связано с формированием структур, необходимых для правильной сегрегации хромосом в митозе, что свидетельствует об образовании связей между различными фазами клеточного цикла.
Функция точек начала репликации также регулируется на уровне целой хромосомы. Целесообразно напомнить, что в клетке ДНК с помощью нуклеосом упакована в хроматин, который накладывает на нее ряд структурных ограничений. Это обстоятельство может влиять на временную организацию репликации; например не на всех точках начала в S-фазе репликация происходит в одно и то же время. В некоторых случаях относительное время наступления активации точек начала репликации может определяться не самой точкой, а ее расположением на хромосоме. Точки, расположенные поблизости от транскрипционно-активного эухроматина, инициируются раньше, чем расположенные вблизи транскрипционно-неактивного гетерохроматина, которые обычно инициируются в поздней S-фазе.
Например, точки, расположенные вблизи теломерных областей хромосом (которые обычно транскрипционно неактивны), реплицируются в конце S-фазы. Это общее правило подтверждается изящными экспериментами, выполненными на почкующихся дрожжах. В этих экспериментах перемещение поздней точки начала репликации в эухроматиновую область приводило к ее ранней репликации, и наоборот Однако время наступления начала репликации контролируется также внутренними факторами, присущими самой точке, и роль структуры хроматина и ядра в динамике репликации выяснена недостаточно.
Таким образом, процесс дупликации генома требует интеграции разнообразных сигналов, связывающих вместе регуляторные системы всего клеточного цикла, контролирующие состояние клетки (CDK), и специфические белки хроматина, которые регулируют индивидуальные cis-сайты. Скоординированное действие CDK и DDK демонстрирует, как различные типы киназ обеспечивают выработку конвергентного сигнала, управляющего прохождением клетки по циклу.
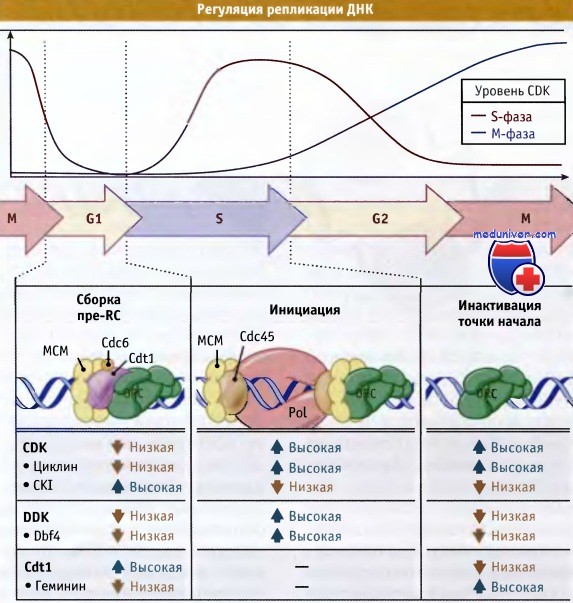
По мере роста их активности начинается инициация синтеза ДНК.
После инициации npe-RC разбирается и может быть собран повторно, только когда в конце митоза активность CDK снова понизится. 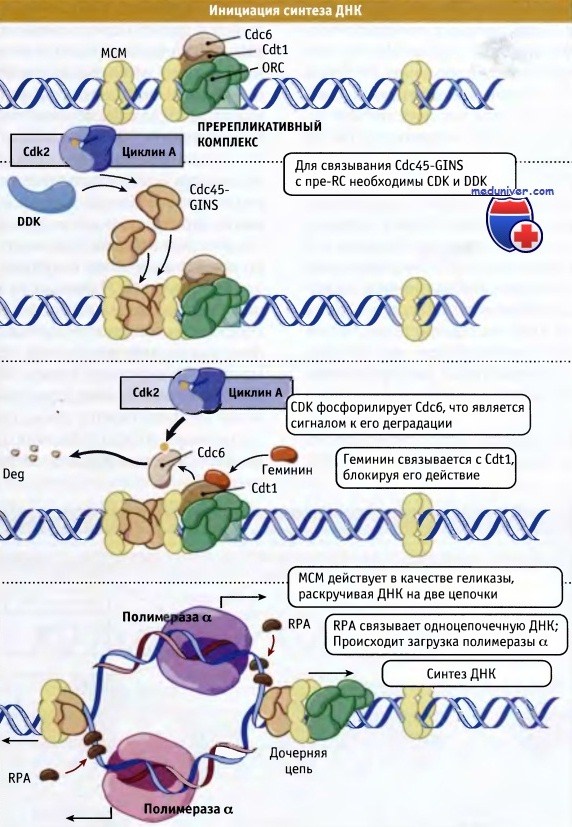
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник