- Производство водорода
- Содержание
- Способы получения водорода [ править ]
- Паровой риформинг (SMR) [ править ]
- Другие методы производства из ископаемого топлива [ править ]
- Пиролиз метана [ править ]
- Частичное окисление [ править ]
- Реформирование плазмы [ править ]
- Из угля [ править ]
- Из нефтяного кокса [ править ]
- Из воды [ править ]
- Электролиз [ править ]
- Объем промышленного производства и эффективность [ править ]
- Электролиз с химическим воздействием [ править ]
- Радиолиз [ править ]
- Термолиз [ править ]
- Термохимический цикл [ править ]
- Ферросилиций метод [ править ]
- Фотобиологическое расщепление воды [ править ]
- Фотокаталитическое расщепление воды [ править ]
- Биоводородные маршруты [ править ]
- Производство ферментативного водорода [ править ]
- Ферментативное производство водорода [ править ]
- Биокатализируемый электролиз [ править ]
- Наногальванический порошок алюминиевого сплава [ править ]
- Воздействие на окружающую среду [ править ]
- Использование водорода [ править ]
Производство водорода
Производство водорода — это семейство промышленных методов получения газообразного водорода . По состоянию на 2020 год большая часть водорода (∼95%) производится из ископаемого топлива путем паровой конверсии природного газа, частичного окисления метана и газификации угля . [1] [2] Другие методы производства водорода включают газификацию биомассы и электролиз воды. Последнее можно сделать напрямую от любого источника электроэнергии, например, от солнечной энергии.
Производство водорода играет ключевую роль в любом промышленно развитом обществе, поскольку водород необходим для многих основных химических процессов. [3] По состоянию на 2019 [Обновить] год во всем мире ежегодно производится около 70 миллионов тонн водорода для различных целей, таких как нефтепереработка, производство аммиака (с помощью процесса Габера ) и метанола (за счет снижения содержания оксида углерода ), а также как топливо при транспортировке. Ожидается, что рынок производства водорода в 2017 году будет оценен в 115,25 млрд долларов США [4].
Содержание
Способы получения водорода [ править ]
Существует четыре основных источника промышленного производства водорода: природный газ, нефть, уголь и электролиз; на которые приходится 48%, 30%, 18% и 4% мирового производства водорода соответственно. [5] Ископаемое топливо является основным источником промышленного водорода. [6] Двуокись углерода можно отделить от природного газа с эффективностью 70–85% для производства водорода и от других углеводородов с различной степенью эффективности. [7] В частности, водород в массе обычно получают путем паровой конверсии метана или природного газа. [8]
Паровой риформинг (SMR) [ править ]
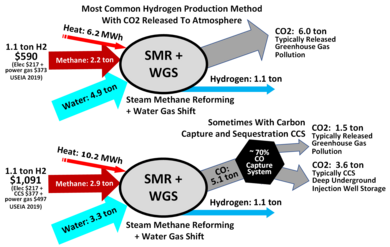
Паровой риформинг — это процесс производства водорода из природного газа. В настоящее время этот метод является самым дешевым источником промышленного водорода. Процесс заключается в нагревании газа до 700–1100 ° C в присутствии водяного пара и никелевого катализатора. Возникающая эндотермическая реакция разрушает молекулы метана и образует оксид углерода CO и водород H 2 . Затем газообразный монооксид углерода можно пропускать с водяным паром над оксидом железа или другими оксидами и подвергать реакции конверсии водяного газа для получения дополнительных количеств H 2 . Обратной стороной этого процесса является то, что его основными побочными продуктами являются CO, CO 2 и другие парниковые газы. [5] В зависимости от качества сырья (природный газ, богатые газы, нафта и т. Д.) Из одной тонны произведенного водорода также будет производиться от 9 до 12 тонн CO 2 , парникового газа, который может улавливаться. [9]
Для этого процесса высокотемпературный (700–1100 ° C) пар (H 2 O) реагирует с метаном (CH 4 ) в эндотермической реакции с образованием синтез-газа . [10]
На второй стадии дополнительный водород генерируется посредством низкотемпературной экзотермической реакции конверсии водяного газа , проводимой при температуре около 360 ° C:
По сути, атом кислорода (O) отделяется от дополнительной воды (пара), чтобы окислить CO до CO 2 . Это окисление также дает энергию для поддержания реакции. Дополнительное тепло, необходимое для запуска процесса, обычно получают за счет сжигания некоторой части метана.
Другие методы производства из ископаемого топлива [ править ]
Пиролиз метана [ править ]
Пиролиз метана (природного газа) с выделением водорода через поток через расплавленный металлический катализатор в «барботажной колонне» [11] представляет собой подход «без парниковых газов», который тестируется в масштабе [12] для производства водорода. [13] Процесс проводится при более высоких температурах (1340 K, 1065 ° C или 1950 ° F). [14] [15] [16] [17]
CH
4 (г) → C (s) + 2 H
2 (г) ΔH ° = 74 кДж / моль
Твердый углерод промышленного качества может быть продан как сырье для производства или захоронен.
Частичное окисление [ править ]
Производство водорода из природного газа или других углеводородов достигается частичным окислением. Смесь топливо-воздух или топливо-кислород частично сгорает, в результате чего получается синтез-газ, богатый водородом . Водород и монооксид углерода получают в результате реакции конверсии водяного газа. [5] Двуокись углерода может подаваться совместно, чтобы снизить отношение водорода к монооксиду углерода.
Реакция частичного окисления происходит, когда субстехиометрическая топливно-воздушная смесь или топливо-кислород частично сгорает в установке риформинга или в реакторе частичного окисления. Различают частичное термическое окисление (TPOX) и частичное каталитическое окисление (CPOX). Химическая реакция принимает общий вид:
Идеальные примеры для топочного мазута и угля, предполагающие составы C 12 H 24 и C 24 H 12 соответственно, следующие:
Реформирование плазмы [ править ]
Процесс Kvrner или процесс Kvaerner сажи и водород (CB&H) [18] представляет собой метод плазменного риформинга, разработанный в 1980-х годах одноименной норвежской компанией для производства водорода и технического углерода из жидких углеводородов (C n H м ). Примерно 48% доступной энергии сырья содержится в водороде, 40% — в активированном угле и 10% — в перегретом паре. [19] CO 2 не образуется.
Вариант этого процесса представлен в 2009 году с использованием технологии утилизации отходов плазменной дуги для производства водорода, тепла и углерода из метана и природного газа в плазменном конвертере [20]
Из угля [ править ]
Для производства водорода из угля , газификация угля используется. В процессе газификации угля используется пар и тщательно контролируемая концентрация газов для разрыва молекулярных связей в угле и образования газообразной смеси водорода и окиси углерода. [21] Этот источник водорода выгоден, поскольку его основным продуктом является угольный газ, который можно использовать в качестве топлива. Газ, полученный в результате газификации угля, позже может быть использован для более эффективного производства электроэнергии и обеспечения лучшего улавливания парниковых газов [22], чем при традиционном сжигании угля. [23]
Другой способ конверсии — низкотемпературная и высокотемпературная карбонизация угля . [24]
Из нефтяного кокса [ править ]
Подобно углю, нефтяной кокс можно также преобразовать в синтез-газ , богатый водородом , посредством газификации угля. Синтез-газ в этом случае состоит в основном из водорода, окиси углерода и H 2 S, в зависимости от содержания серы в коксовом сырье. Газификация является привлекательным вариантом для производства водорода практически из любого источника углерода, обеспечивая при этом привлекательные альтернативы использованию водорода за счет интеграции процессов. [25]
Из воды [ править ]
Способы производства водорода без использования ископаемого топлива включают процесс расщепления воды или расщепления молекулы воды H 2 O на составляющие кислород и водород. Когда источник энергии для расщепления воды является возобновляемым или низкоуглеродным, производимый водород иногда называют зеленым водородом . Преобразование может быть выполнено несколькими способами, но все методы обычно более дороги, чем методы производства на основе ископаемого топлива. В Австралии зеленый водород стоит вдвое дороже, чем обычный водород и синий водород , но Австралийский национальный университет 2020 г. Согласно отчету, Австралия могла бы производить его гораздо дешевле, даже в настоящее время, и к 2030 году она могла бы сравняться по цене с обычным и голубым водородом (около 2 австралийских долларов за килограмм ), что будет конкурентоспособно по стоимости с ископаемым топливом. В начале 2021 года аналитик энергетического рынка предположил, что цена на экологически чистый водород упадет на 70% в ближайшие 10 лет в странах с дешевой возобновляемой энергией . [26]
Электролиз [ править ]
По всему миру установлено около 8 ГВт электролизных мощностей, что составляет около 4% мирового производства водорода. [ когда? ] [ необходима ссылка ]
Электролиз заключается в использовании электричества для разделения воды на водород и кислород. Электролиз воды имеет КПД 70–80% (потери преобразования 20–30%) [27] [28], в то время как паровой риформинг природного газа имеет тепловой КПД между 70–85%. [29] Ожидается, что к 2030 году электрический КПД электролиза достигнет 82–86% [30] , при этом сохранится долговечность, поскольку прогресс в этой области продолжается высокими темпами. [31]
Электролиз воды может происходить при температуре от 50 до 80 ° C, в то время как паровой риформинг метана требует температур от 700 до 1100 ° C. [32] Разница между двумя методами заключается в используемой первичной энергии; либо электричество (для электролиза), либо природный газ (для парового риформинга метана). Благодаря использованию воды, легкодоступного ресурса, электролиз и аналогичные методы разделения воды привлекли интерес научного сообщества. С целью снижения стоимости производства водорода возобновляемые источники энергии были нацелены на возможность электролиза. [21]
Существует три основных типа ячеек: ячейки с твердым оксидным электролизером (SOEC), ячейки с мембраной с полимерным электролитом (PEM) и ячейки с щелочным электролизом (AEC). [33] Обычно щелочные электролизеры дешевле с точки зрения инвестиций (обычно в них используются никелевые катализаторы), но менее эффективны; Электролизеры PEM, наоборот, более дорогие (в них обычно используются дорогие катализаторы из металлов платиновой группы ), но они более эффективны и могут работать при более высоких плотностях тока и, следовательно, могут быть дешевле, если производство водорода достаточно велико. [ необходима цитата ]
SOEC работают при высоких температурах, обычно около 800 ° C. При таких высоких температурах значительное количество требуемой энергии может быть предоставлено в виде тепловой энергии (тепла), что называется высокотемпературным электролизом . Тепловая энергия может поступать из различных источников, включая отходы промышленного тепла, атомные электростанции или солнечные тепловые электростанции. Это может снизить общую стоимость производимого водорода за счет уменьшения количества электроэнергии, необходимой для электролиза. [34] [35] [36] [37] Электролизные ячейки PEM обычно работают при температуре ниже 100 ° C. [34] Эти элементы имеют то преимущество, что они сравнительно просты и могут быть спроектированы так, чтобы принимать входное напряжение в широком диапазоне, что делает их идеальными для использования с возобновляемыми источниками энергии, такими как солнечные фотоэлектрические панели. [38] AEC оптимально работают при высоких концентрациях электролита (КОН или карбонат калия) и при высоких температурах, часто около 200 ° C.
Объем промышленного производства и эффективность [ править ]
Эффективность современных генераторов водорода измеряется количеством энергии, потребляемой на стандартный объем водорода (МДж / м 3 ), принимая стандартные температуру и давление H 2 . Чем ниже энергия, потребляемая генератором, тем выше будет его КПД; 100% -ный электролизер потребляет 39,4 киловатт-часов на килограмм (142 МДж / кг) водорода, [39] 12 749 джоулей на литр (12,75 МДж / м 3 ). Практический электролиз (с использованием вращающегося электролизера при давлении 15 бар) может потреблять 50 киловатт-часов на килограмм (180 МДж / кг) и еще 15 киловатт-часов (54 МДж), если водород сжимается для использования в водородных автомобилях. [40]
Обычный щелочной электролиз имеет эффективность около 70% [41], однако доступны усовершенствованные электролизеры на щелочной воде с эффективностью до 82%. [42] С учетом использования более высокой теплотворной способности (поскольку неэффективность из-за тепла может быть перенаправлена обратно в систему для создания пара, необходимого для катализатора), средняя эффективность электролиза PEM составляет около 80% или 82% при использовании самые современные щелочные электролизеры. [43]
Ожидается, что к 2030 году эффективность ПЭМ возрастет примерно до 86% [44]. Теоретическая эффективность электролизеров на основе ПЭМ прогнозируется до 94%. [45]
По состоянию на 2020 год стоимость водорода при электролизе составляет около 3-8 долларов за кг. [46] Учитывая промышленное производство водорода и использование лучших в настоящее время процессов электролиза воды (PEM или щелочной электролиз), которые имеют эффективный электрический КПД 70–82%, [47] [48] [49] производят 1 кг водорода. (который имеет удельную энергию 143 МДж / кг или около 40 кВтч / кг) требует 50–55 кВтч электроэнергии. При стоимости электроэнергии 0,06 доллара США / кВтч, как указано в планах Министерства энергетики по производству водорода на 2015 год [50]. стоимость водорода составляет 3 доллара за кг. Целевая цена Министерства энергетики США на водород в 2020 году составляет 2,30 долл. США / кг, при этом стоимость электроэнергии составляет 0,037 долл. США / кВтч, что вполне достижимо с учетом недавних тендеров PPA для ветровой и солнечной энергии во многих регионах. [51] Одним из преимуществ электролиза перед водородом парового риформинга метана (SMR) является то, что водород можно производить на месте, а это означает, что исключается дорогостоящий процесс доставки на грузовике или по трубопроводу.
Паровая конверсия метана в среднем составляет 1 [46] –3 долл. США / кг. [ необходима цитата ] Это делает производство водорода путем электролиза конкурентоспособным по стоимости уже во многих регионах, как указано Nel Hydrogen [52] и другими, включая статью IEA [53], в которой рассматриваются условия, которые могут привести к конкурентному преимуществу для электролиза. .
Электролиз с химическим воздействием [ править ]
Помимо снижения напряжения, необходимого для электролиза за счет повышения температуры электролизной ячейки, также можно электрохимически потреблять кислород, произведенный в электролизере, путем введения топлива (такого как углерод / уголь, [54] метанол , [55] ] [56] этанол , [57] муравьиная кислота , [58] глицерин, [58] и т.д.) в кислородную сторону реактора. Это снижает требуемую электрическую энергию и потенциально снижает стоимость водорода до менее чем 40
60% с оставшейся энергией, обеспечиваемой таким образом. [59] Кроме того, водный электролиз с использованием углерода / углеводородов (CAWE) может предложить менее энергоемкий и более чистый метод использования химической энергии в различных источниках углерода, таких как угли с низким и высоким содержанием серы, биомасса, спирты и метан ( Природный газ), где произведенный чистый CO 2 может быть легко изолирован без необходимости разделения. [60] [61]
Радиолиз [ править ]
Ядерное излучение может разрушить водные связи посредством радиолиза . [62] [63] На золотом руднике Мпоненг , Южная Африка , исследователи обнаружили бактерии в естественной зоне высокой радиации. Бактериальное сообщество , которое преобладает в новом phylotype из Desulfotomaculum , кормил в первую очередь радиолитическому производства водорода. [64]
Термолиз [ править ]
Вода самопроизвольно диссоциирует при температуре около 2500 ° C, но этот термолиз происходит при температурах, слишком высоких для обычных технологических трубопроводов и оборудования.
Термохимический цикл [ править ]
Термохимические циклы объединяют исключительно источники тепла ( термо ) с химическими реакциями для разделения воды на водородные и кислородные компоненты. [65] Термин « цикл» используется потому, что, помимо воды, водорода и кислорода, химические соединения, используемые в этих процессах, непрерывно рециркулируют. Если электричество частично используется в качестве входа, полученный термохимический цикл определяется как гибридный .
Цикл серы-йод (СИ цикл) является термохимическими процессами цикла , который генерирует водород из воды с эффективностью примерно 50%. Сера и йод, используемые в процессе, восстанавливаются и повторно используются, а не потребляются в процессе. Цикл может быть выполнен с любым источником очень высоких температур, около 950 ° С, например, путем концентрации солнечной энергией системы (CSP) и рассматриваются как хорошо подходят для производства водорода высокотемпературных ядерных реакторов , [66] и, как таковой, изучается в высокотемпературном инженерном испытательном реакторе в Японии. [67] [68] [69] [70] Существуют и другие гибридные циклы, в которых используются как высокие температуры, так и некоторое количество электроэнергии, например, цикл медь-хлор , он классифицируется как гибридный термохимический цикл, потому что он использует электрохимическую реакцию на одной из стадий реакции, он работает при 530 ° C и имеет КПД 43 процента. [71]
Ферросилиций метод [ править ]
Ферросилиций используется военными для быстрого производства водорода для воздушных шаров . В химической реакции используются гидроксид натрия , ферросилиций и вода. Генератор достаточно мал, чтобы поместиться в грузовике, и требует лишь небольшого количества электроэнергии, материалы стабильны и негорючие, и они не производят водород, пока не смешиваются. [72] Этот метод используется со времен Первой мировой войны . Тяжелый стальной сосуд высокого давления заполняется гидроксидом натрия и ферросилицием, закрывается и добавляется контролируемое количество воды; растворение гидроксида нагревает смесь до примерно 93 ° C и запускает реакцию; производятся силикат натрия , водород и водяной пар. [73]
Фотобиологическое расщепление воды [ править ]
Биологический водород можно производить в биореакторе из водорослей . [74] В конце 1990-х было обнаружено, что если водоросли лишены серы, они переключатся с производства кислорода , то есть нормального фотосинтеза , на производство водорода. Кажется, что производство в настоящее время экономически целесообразно, если превзойти барьер энергоэффективности 7–10% (преобразование солнечного света в водород). [75] со скоростью производства водорода 10–12 мл на литр культуры в час. [76]
Фотокаталитическое расщепление воды [ править ]
Преобразование солнечной энергии в водород посредством процесса разделения воды — один из самых интересных способов создания экологически чистых и возобновляемых источников энергии . Однако, если этому процессу способствуют фотокатализаторы, взвешенные непосредственно в воде, вместо использования фотоэлектрической и электролитической систем, реакция проходит всего за одну стадию, ее можно сделать более эффективной. [77] [78]
Биоводородные маршруты [ править ]
Потоки биомассы и отходов в принципе могут быть преобразованы в биоводород с помощью газификации биомассы , парового риформинга или биологического преобразования, такого как биокатализируемый электролиз [59] или ферментативное производство водорода. [6]
Среди методов производства водорода, таких как паровой риформинг метана, термический крекинг, газификация и пиролиз угля и биомассы, электролиз и фотолиз, биологические методы являются более экологичными и менее энергоемкими. Кроме того, для производства водорода биохимическими путями можно использовать широкий спектр отходов и малоценных материалов, таких как сельскохозяйственная биомасса, в качестве возобновляемых источников. Тем не менее, в настоящее время водород производится в основном из ископаемого топлива, в частности из природного газа, который не является возобновляемым источником. Водород — не только самое чистое топливо, но и широко используется в ряде отраслей, особенно в производстве удобрений, нефтехимической и пищевой. Это делает логичным исследование альтернативных источников для производства водорода. Основными биохимическими технологиями получения водорода являются процессы темного брожения и фотоферментации.При темной ферментации углеводы преобразуются в водород ферментативными микроорганизмами, включая строго анаэробные и факультативные анаэробные бактерии. Теоретический максимум 4 моль H2 / моль глюкозы может быть произведено, и, помимо водорода, сахара превращаются в летучие жирные кислоты (ЛЖК) и спирты в качестве побочных продуктов во время этого процесса. Фотоферментативные бактерии способны генерировать водород из ЛЖК. Следовательно, метаболиты, образующиеся при темной ферментации, можно использовать в качестве сырья для фотоферментации для увеличения общего выхода водорода. [79]
Производство ферментативного водорода [ править ]
Биоводород можно производить в биореакторах. В процессе участвуют бактерии, потребляющие углеводороды и производящие водород и CO 2 . CO 2 и водород можно разделить.
Ферментативное производство водорода является ферментативным превращением органического субстрата в биоводород проявляется разнообразной группой бактерий с использованием мульти ферментных систем , включающих три этапа , аналогичного анаэробной конверсией . Реакции темного брожения не требуют световой энергии, поэтому они способны постоянно производить водород из органических соединений в течение дня и ночи. Фотоферментация отличается от темной ферментации тем, что она протекает только при наличии света . Например, фото-ферментация с Rhodobacter sphaeroides SH2C может использоваться для преобразования низкомолекулярных жирных кислот в водород. [80]
Ферментативное производство водорода может осуществляться с использованием прямого биофотолиза зелеными водорослями, непрямого биофотолиза цианобактериями, фото-ферментации анаэробными фотосинтетическими бактериями и темного брожения анаэробными ферментативными бактериями. Например, в литературе сообщается об исследованиях производства водорода с использованием H. salinarium , анаэробных фотосинтезирующих бактерий, связанных с донором гидрогеназы, таким как E. coli . [81] Enterobacter aerogenes — еще один производитель водорода. [82]
Ферментативное производство водорода [ править ]
Были разработаны разнообразные ферментативные пути для производства водорода из сахаров. [83]
Биокатализируемый электролиз [ править ]
Помимо темного брожения, другой возможностью является электрогидрогенез (электролиз с использованием микробов). Используя микробные топливные элементы , сточные воды или растения могут использоваться для выработки энергии. Биокатализируемый электролиз не следует путать с биологическим производством водорода , поскольку последний использует только водоросли, а в последнем водоросли сами генерируют водород мгновенно, тогда как при биокатализируемом электролизе это происходит после прохождения микробного топливного элемента и различных водных растений. [84] можно использовать. К ним относятся тростник душистая , кордграсс, рис, помидоры, люпин и водоросли. [85]
Наногальванический порошок алюминиевого сплава [ править ]
Было показано, что порошок алюминиевого сплава, изобретенный исследовательской лабораторией армии США в 2017 году, способен производить газообразный водород при контакте с водой или любой жидкостью, содержащей воду, благодаря своей уникальной наноразмерной гальванической микроструктуре. Сообщается, что он производит водород с выходом 100 процентов от теоретического без необходимости использования каких-либо катализаторов, химикатов или внешней энергии. [86] [87]
Воздействие на окружающую среду [ править ]
По состоянию на 2020 год большая часть водорода производится из ископаемого топлива, что приводит к выбросам углерода. [88] Это часто называют серым водородом, когда выбросы выбрасываются в атмосферу, и голубым водородом, когда выбросы улавливаются с помощью CCS улавливания и хранения углерода . [89]
Водород, полученный с использованием более новой экологически чистой технологии пиролиза метана [90] , часто называют бирюзовым водородом . Высококачественный водород производится непосредственно из природного газа, а связанный с ним экологически чистый твердый углерод не выбрасывается в атмосферу, а затем может быть продан для промышленного использования или храниться на свалках.
Водород, полученный из возобновляемых источников энергии, часто называют зеленым водородом . Есть два практических способа производства водорода из возобновляемых источников энергии. Один заключается в использовании энергии для газа , в котором электроэнергия используется для производства водорода в результате электролиза, а другой — в использовании свалочного газа для производства водорода в установке парового риформинга. Водородное топливо, когда оно производится из возобновляемых источников энергии, таких как энергия ветра или солнца, является возобновляемым топливом . [91]
Использование водорода [ править ]
Водород используется для преобразования тяжелых нефтяных фракций в более легкие путем гидрокрекинга . Он также используется в других процессах, включая процесс ароматизации , гидрообессеривания и производство аммиака с помощью процесса Габера .
Водород может использоваться в топливных элементах для местного производства электроэнергии или потенциально в качестве транспортного топлива.
Водород образуется как побочный продукт производства промышленного хлора путем электролиза . Хотя для этого требуются дорогостоящие технологии, водород можно охлаждать, сжимать и очищать для использования в других процессах на месте или продавать заказчику через трубопровод, баллоны или грузовики. Открытие и разработка менее дорогостоящих методов производства объемного водорода имеет отношение к созданию водородной экономики . [6]
Источник




_at_varying_natural_gas_prices.jpg/440px-H2_production_cost_($-gge_untaxed)_at_varying_natural_gas_prices.jpg)






