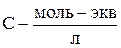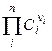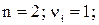- Лабораторная работа № 10. Определение степени диссоциации слабого электролита кондуктометрическим способом
- Кондуктометрическое титрование
- Определение степени диссоциации слабой кислоты путем измерения электропроводности раствора
- Страницы работы
- Содержание работы
- Лабораторные работы «Кондуктометрическое титрование» «Определение степени и константы диссоциации слабого электролита»
- Теоретическая часть
Лабораторная работа № 10. Определение степени диссоциации слабого электролита кондуктометрическим способом
Цель работы: определить степень и константу диссоциации слабой кислоты путем измерения электропроводности раствора.
Сущность работы: электропроводность раствора электролита зависит от концентрации ионов в растворе и их подвижности. В растворах слабых электролитов концентрация ионов зависит от степени диссоциации. Получив зависимость электропроводности от концентрации электролита, вычисляют его степень диссоциации и константу диссоциации слабого электролита.
Оборудование и реактивы. Кондуктометр или кондуктометр – иономер; магнитная мешалка; химический стакан объемом 100 мл – 5 шт.; химический стакан объемом 50 мл – 1 шт.; химический стакан объемом 250 мл – 1 шт.; мерные колбы объемом 250 мл – 4 шт.; мерная пипетка объемом 50 мл – 1 шт.; мерная пипетка объемом 10 мл – 1 шт.; бюретка для титрования объемом 25 мл – 1 шт.; гидроксид натрия – раствор (концентрация указана на емкости с реактивом); слабая кислота – СН3СООН или НСООН – раствор (примерное значение концентрации указано на емкости с реактивом).
Выполнение работы
I. Анализ концентрации раствора слабой кислоты методом кондуктометрического титрования.
1. Получить от преподавателя раствор слабой кислоты.
2. Отобрать аликвоту 10 мл в химический стакан объемом 250 мл.
3. В бюретку залить раствор гидроксида натрия и «занулить» бюретку.
4. Поставить пробу на магнитную мешалку и поместить в раствор якорь магнитной мешалки.
5. Погрузить в стакан с пробой электрод кондуктометра.
6. Долить в стакан для титрования дистиллированную воду до закрытия щели электрода раствором.
7. Включить магнитную мешалку.
8. Зафиксировать показания кондуктометра.
9. Приливать гидроксид натрия из бюретки порциями по 0,5 мл, фиксируя после каждой порции щелочи значение электропроводности раствора.
10. Титрование продолжать до получения изменения хода зависимости удельной электропроводности от объема щелочи.
11. Данные занести в таблицу 1.
II. Получение зависимости удельной электропроводности от содержания слабого электролита в растворе
1. Приготовить серию из 4 последовательно разбавленных растворов слабого электролита:
1) мерной пипеткой объемом 50 мл отобрать исходный раствор, поместить его в мерную колбу № 1 на 250 мл, довести до метки дистиллированной водой; закрыть колбу пробкой и перемешать раствор, переворачивая колбе не менее 40 раз;
2) из колбы № 1 в колбу № 2 перенести при помощи мерной пипетки 50 мл раствора, довести объем в колбе № 2 дистиллированной водой до метки, закрыть колбу пробкой и перемешать раствор, переворачивая колбе не менее 40 раз;
3) повторить с колбами № 3 и № 4.
2. Пробы приготовленных растворов отобрать в маркированные химические стаканы объемом 100 мл.
3. Измерить удельную электропроводность приготовленных растворов слабой кислоты путем погружения электрода кондуктометра в стакан с раствором. Начинать измерения следует с самого разбавленного раствора. При погружении электрода в раствор необходимо следить за тем, чтобы щель электрода была полностью закрыта раствором. При переходе от одного раствора к другому электрод следует насухо протереть кусочком фильтровальной бумаги.
4. Результаты измерений занести в таблицу 2.
Содержание протокола лабораторной работы
1. Название слабого электролита.
2. Химическая формула слабого электролита.
2. Ориентировочное значение концентрации слабого электролита (указано на емкости с этим электролитом) С.
3. Концентрация раствора гидроксида натрия (титранта) СNaOH.
Объем пробы слабого электролита, взятый для титрования Vа.
Данные для построения кривой кондуктометрического титрования
| № п/п | VNaOH, мл | Удельная электропроводность c, См |
| 0,5 | ||
| … | … |
Зависимость удельной электропроводности слабого электролита от его концентрации
Источник
Кондуктометрическое титрование



Экспериментальные приложения метода измерения электропроводности.
1. Определение константы диссоциации и степени диссоциации
Степень диссоциации a слабого электролита может быть найдена из соотношения:
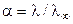
Константа диссоциации КД бинарного слабого электролита типа АВ связана со степенью диссоциации a уравнением
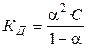
С учетом (17), получаем
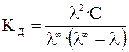
Величина λ ∞ рассчитывается по закону Кольрауша (уравнение (16)).
2 Определение произведения растворимости
Растворимостью электролита (S) называется его концентрация в насыщенном растворе (моль/л), а произведением растворимости (ПР) – произведение активностей катиона и аниона труднорастворимой соли.
Насыщенный раствор труднорастворимой соли является очень разбавленным раствором (α → 1 и λ → λ ∞ ). Тогда для такого раствора можно считать, что эквивалентная электропроводность численно равна λ ∞ .
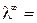
Найдя значение λ ∞ по табличным данным, и измерив удельную электропроводность раствора, можно вычислить концентрацию насыщенного раствора (в моль-экв/л),
Затем перейдя от нормальной концентрации С к молярной концентрации СM можно вычислить растворимость (S) соли.
Поскольку удельная электропроводность растворов труднорастворимых веществ (æр-ра) часто соизмерима с электропроводностью растворителя (воды) (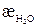
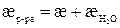
где æ –удельная электропроводность соли
Для труднорастворимых солей активности катиона и аниона практически совпадают с их концентрациями, 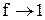
ПР =
где ni – стехиометрический коэффициент иона в уравнении диссоциации;
n – число видов ионов, на которые диссоциирует электролит;
Ci – концентрация иона, связанная с молярной концентрацией электролита СМ соотношением 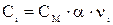
Так как a = 1, то

и произведение растворимости будет:
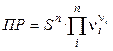
Так, для труднорастворимого (бинарного) одно–одновалентного электролита, диссоцииирующего по схеме
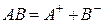
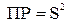
Кондуктометрия – это метод установления эквивалентной точки титрования, основанный на измерении электропроводности растворов.
Широко распространенный на практике, этот метод анализа не требует применения индикаторов и особенно удобен в тех случаях, когда необходимо проанализировать мутные, окрашенные или содержащие осадки растворы. Сущность метода состоит в измерении проводимости титруемого раствора как функции объёма прибавляемого реагента. Точку эквивалентности находят по графику “электропроводность – объём титрующего раствора” как точку пересечения двух прямых или точку перегиба. За ходом реакции следят по изменению удельной электропроводности или сопротивления, которое связано с заменой в растворе одних ионов другими (с иной подвижностью).

Рассмотрим титрование сильной кислоты щелочью (рис. 7а). При титровании раствора кислоты (например, HCl) раствором щелочи (например, NaOH) часть ионов H + (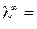
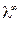
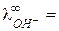
Рассмотрим титрование слабой кислоты щелочью (рис. 7б). На “кислотном“ участке титрования электропроводность раствора растёт вследствие замещения слабо диссоциированной кислоты на её сильно диссоциированную соль. После достижения точки эквивалентности наблюдается более сильное увеличение электропроводности, что связано с появлением в растворе высокоподвижных ионов гидроксила.
При титровании смеси слабой и сильной кислот щелочью (рис. 7в) в реакцию нейтрализации в первую очередь будет вступать сильная кислота так как в присутствии сильной кислоты диссоциация слабой будет подавлена. Только после того, как она будет полностью оттитрована, начнет реагировать слабая кислота.
Источник
Определение степени диссоциации слабой кислоты путем измерения электропроводности раствора
Страницы работы
Содержание работы
Министерство образования Российской федерации
Санкт-Петербургский государственный горный институт
по лабораторной работе:
Определение степени диссоциации электролита кондуктометрическим способом.
Выполнил: студент Павлов Р. Д.
Проверила: доцент Литвинова Т. Е.
1. Цель работы: определить степень диссоциации слабой кислоты путем измерения электропроводности раствора.
2. Приборы и реактивы:
- кондуктометр кондуктометр-иономер;
- магнитная мешалка;
- химический стакан объемом 50-100 мл;
- Мерные колбы объемом 10-20 мл;
- Гидроксид натрия 0,898 н;
- Раствор – задача слабой кислоты (муравьиная кислота
).
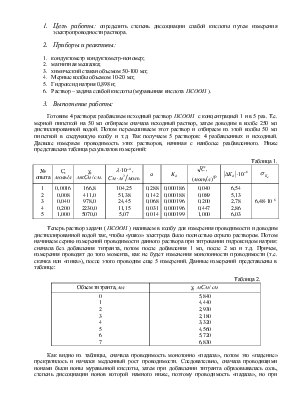
Готовим 4 раствора: разбавляем исходный раствор 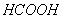
χ, 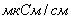
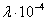
Источник
Лабораторные работы «Кондуктометрическое титрование» «Определение степени и константы диссоциации слабого электролита»
Метод исследования, основанный на измерении электрической проводимости, называется кондуктометрией. Он относится к физико-химическим методам анализа, которые основаны на взаимосвязи между составом системы и её физическими и физико-химическими свойствами. Способность проводить электрический ток является одним из важнейших физико-химических свойств водных растворов электролитов. Поэтому с помощью кондуктометрии можно определять степень и константу диссоциации слабых электролитов, растворимость малорастворимых веществ, количественно оценивать состав раствора.
Провести кондуктометрическое титрование слабой кислоты щелочью, построить кривую титрования, найти точку эквивалентности и рассчитать концентрацию кислоты;
По экспериментальным данным рассчитать степень и константу диссоциации СН3СООН.
Колба для титрования;
Реактивы: 0,1н HCl, 1н NaOH, 0,1н СН3СООН, 0,1н KCl.
Теоретическая часть
Из курса физики известно, что электрическое сопротивление любого проводника можно рассчитать по формуле

где R – сопротивление, Ом;
l – длина проводника, см;
S – площадь поперечного сечения, см 2 ;
ρ – удельное сопротивление, т. е. сопротивление проводника длиной 1см и с площадью поперечного сечения 1см 2 .
В электрохимии принято пользоваться величинами, обратными указанным
Величина L называется электрической проводимостью и измеряется в Сименсах (См),
Величина χ называется удельной электрической проводимостью. Это электрическая проводимость раствора, помещенного между двумя электродами площадью 1см 2 , находящимися на расстоянии 1см. Размерность χ – См∙см -1 .
Кроме удельной электрической проводимости, используют и молярную (эквивалентную) электрическую проводимость. Молярная (эквивалентная) проводимость– это проводимость раствора, содержащего 1 молярную массу эквивалента вещества, при расстоянии между электродами, равном 1см. Обозначается λ (лямбда). Размерность См∙см 2 моль -1.
Связь между двумя видами электрической проводимости
где с – молярная концентрация эквивалента.
Метод исследования, основанный на измерении электрической проводимости, называется кондуктометрией. Прибор для измерения электрической проводимости называется кондуктометром.
Кондуктометрический метод позволяет определять степень и константу диссоциации слабого электролита, растворимость малорастворимых веществ, концентрации различных электролитов. В последнем случае говорят о кондуктометрическом титровании.
Кондуктометрическое титрование – это метод определения концентрации электролитов титрованием до эквивалентной точки, которая устанавливается по изменению электрической проводимости. Этим методом часто пользуются для определения концентрации электролита в случае окрашенных или мутных растворов, а также при титровании смесей кислот или смесей оснований, когда подбор цветного индикатора затруднен.
При титровании происходит изменение ионного состава раствора, что изменяет электрическую проводимость. Экспериментальные данные наносят на график в координатах: электрическая проводимость – объем прибавляемого реагента и по точке резкого изгиба кривой определяют эквивалентную точку.
Характер изменения электрической проводимости обусловлен:
заменой ионов одной подвижности на ионы другой подвижности. Например, при титровании соляной кислоты гидроксидом натрия ионы Н + , обладающие высокой подвижностью, заменяются на менее подвижные ионы Na + ;
заменой малодиссоциирующих молекул на более диссоциирующие. Этот случай наблюдается при титровании уксусной кислоты гидроксидом натрия.
Для проведения высококачественных измерений проводимости используется микропроцессорный портативный многодиапазонный кондуктометр «Н 8733 N»






Для работы необходимо
Включить прибор, нажав кнопку ON/OFF.
Погрузить датчик в исследуемый раствор, осторожно перемешать, постукивая кончиком датчика о дно сосуда для удаления пузырьков воздуха.
Выбрать необходимый интервал измерений с помощью кнопок 3.
Подождать некоторое время, пока не установится термическое равновесие. Значение проводимости появится на экране 1.
Внимание! Электрод должен быть погружен в раствор примерно на 8 см. Если измерения проводятся в различных образцах, рекомендуется тщательно промывать датчик, чтобы избежать загрязнения образцов. Для споласкивания лучше использовать достаточное количество раствора, проводимость которого предстоит измерить.
Тут вы можете оставить комментарий к выбранному абзацу или сообщить об ошибке.
Источник