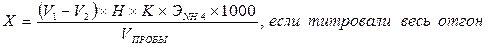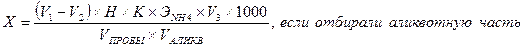- Лекция 16. Определение аммиака в солях аммония
- Титриметрический метод определения аммиака
- ПНД Ф 14.1:2:3.1-95 ФР 1.31.2017.27257 Количественный химический анализ вод. Методика измерений массовой концентрации ионов аммония в природных и сточных водах фотометрическим методом с реактивом Несслера / МИ / 14 1 2 3 1 95 1 31 2017 27257
- 1 ВВЕДЕНИЕ
- 2 ТРЕБОВАНИЯ К ПОКАЗАТЕЛЯМ ТОЧНОСТИ ИЗМЕРЕНИЙ
Лекция 16. Определение аммиака в солях аммония
Ключевые слова: кривая титрования, обратное титрование, метод Кьельдаля, заместительное титрование, формальдегидный метод.
Катион аммония NH4 + проявляет очень слабые кислотные свойства, за счет гидролиза: NH4 + + H2O 
Процесс характеризуется константой гидролиза:
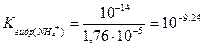
Поскольку константа очень мала, на кривой титрования соли аммония щелочью скачок отсутствует и его прямое титрование щелочью с применением рН-индикатора невозможно. Поэтому для определения аммиака (NH3) в солях аммония (NH4 + ) применяют косвенные методы анализа: обратное титрование или заместительное титрование.
В первом вариантеметода обратного титрования к анализируемому раствору добавляют избыток точно отмеренного титрованного раствора NaOH и нагревают до полного удаления NH3 из раствора.
Окончание удаления аммиака (≈30 мин) определяют по влажной индикаторной бумаге, ее вносят в пары над нагреваемой колбой с раствором. По окончании удаления всего аммиака индикаторная бумага не синеет.
Оставшееся количество щелочи определяют титрованием стандартным раствором кислоты (например, HCl) в присутствии метилоранжа.
Фенолфталеин в качестве индикатора не применяется, так как возможно искажение результата за счет взаимодействия щелочи с СО2.
Расчет результатов анализа проводят по закону эквивалентов.
1 способ. Если известны концентрации растворов кислоты и щелочи, по результатам титрования рассчитывают объем щелочи (VNaOH(остаток)), пошедший на реакцию с кислотой (HCl), по соотношению
где NNaOH – нормальная концентрация рабочего раствора щелочи; NHCl – нормальная концентрация рабочего раствора кислоты; VHCl – объем рабочего раствора кислоты, пошедший на титрование в присутствии метилоранжа; VNaOH – избыточный объем добавленного рабочего раствора щелочи.
Объем раствора щелочи, пошедший на реакцию с NH4Cl, равен разности:
где nэкв — количество эквивалентов указанных веществ, моль.
2 способ. Щелочь (NaOH) расходуется на взаимодействие с двумя веществами (NH4Cl и HCl), поэтому справедливо соотношение
Если концентрация щелочи неизвестна, в ходе анализа проводят контрольное титрование, в котором определяют объем кислоты (VHCl(контр)), необходимый для полной нейтрализации объема щелочи, взятого на анализ (VNaOH). В этом случае:
Массу аммиака (m(NH3)) рассчитывают по формуле
где M(ЭNH3) =17 г/моль – молярная масса эквивалента NH3.
Пример.К навеске соли аммония добавили 30,00 мл 0,1024 н раствора щелочи, прокипятили до полного удаления аммиака, после чего оттитровали 10,50 мл 0,09876 н раствора соляной кислоты. Рассчитать массу аммиака и массу азота, содержащегося в образце.
В широко известном методе определения азота в органических соединениях по Кьельдалю используется второй вариант метода обратного титрования. Методом Кьельдаля можно определять азот в аминах, аминокислотах, алкалоидах, белках, пищевых продуктах и многих других азотсодержащих соединениях. Пробу органического вещества обрабатывают при нагревании концентрированной серной кислотой, в результате чего органические соединения окисляются до СО2 и Н2О, а азот переходит в (NH4)2SО4. После охлаждения к остатку — анализируемому раствору соли аммония — добавляют избыток щелочи:
Выделившийся аммиак отгоняют в точно измеренный избыточный объем (VHCl) титрованного раствора кислоты.
Количество кислоты, оставшейся в растворе после взаимодействия с аммиаком, определяют титрованием щелочью c метилоранжем.
Применение фенолфталеина и других индикаторов с рТ > 7 недопустимо, так как в реакцию могут вступить ионы аммония, присутствующие в растворе. Результат анализа рассчитывают по закону эквивалентов для обратного титрования:
где VHCl – избыточный объем рабочего раствора кислоты;
VNaOH – объем рабочего раствора щелочи, пошедший на титрование в присутствии метилоранжа.
Одним из самых точных методов определения солей аммония является формальдегидный метод заместительного титрования. Он основан на реакции
В результате реакции в количестве, эквивалентном соли аммония, образуется сильная кислота (HCl), которую титруют раствором щелочи в присутствии фенолфталеина
HCl + NaOH → NaCl + H2O.
Необходимо применять индикатор с рТ≈9, поскольку в результате реакции образуется слабое основание— гексаметилентетрамин ((CH2)6N4), и точка эквивалентности лежит при рН > 7.
Кроме того, формальдегид может быть загрязнен муравьиной кислотой в результате его окисления кислородом воздуха:
Муравьиная кислота также оттитровывается раствором щелочи с образованием формиата натрия, водный раствор которого имеет щелочную реакцию. Для введения поправки на содержание муравьиной кислоты проводят «холостой опыт» титрования образца формальдегида раствором щелочи в присутствии фенолфталеина.
CHOOH + NaOH → CHOONa + H2O.
Объем щелочи, пошедший на титрование образца формальдегида (VNaOH(мк)), вычитают из объема, пошедшего на титрование исследуемого раствора (VNaOH). Содержание аммиака рассчитывают по соотношению
Контрольные вопросы
1. Почему невозможно прямое титрование катионов аммония щелочью?
2. Метод обратного титрования для определения содержания аммиака в
3. В каком случае и для чего проводят контрольное титрование щелочи?
4. Определение азота в органических соединениях по методу Кьельдаля.
5. Метод заместительного титрования (формальдегидный метод) для
определения содержания аммиака в солях аммония.
6. Что такое «холостой опыт» и для чего его проводят?
Список рекомендуемой литературы
1. Васильев В.П. Аналитическая химия. Кн. 1. Титриметрические и гравиметрический методы анализа. — М.: Дрофа, 2005. — С. 159 – 161.
2. Харитонов Ю.Я. Аналитическая химия (аналитика): учебник для вузов. В 2 кн. Кн. 2. Количественный анализ. Физико-химические (инструментальные) методы анализа. – М.: Высшая школа, 2001. – С.126 — 128.
Источник
Титриметрический метод определения аммиака



Сущность метода. Метод основан на титрованииаммиака, обладающего слабыми основными свойствами, раствором кислоты в присутствии индикатора.
Реактивы и оборудование
Серная кислота, 0,02 н. раствор
Предварительная отгонка аммиака.При низком содержании NH4 + и NH3 , когда отсутствуют мешающие вещества, отгонку можно не проводить, но она все же обязательна при наличии мути, при присутствии сильно окрашенных веществ, при кислотности, превышающей 100 мг/дм 3 , и щелочности, превышающей 500 мг/дм 3 . Если отгонку проводить из сильнощелочного раствора, то при этом возможен гидролиз некоторых азотсодержащих органических веществ с образованием аммиака, поэтому отгонку надо вести при соответствующем рН исходного раствора.
Отгонку аммиака рекомендуется проводить при рН 9,5 (если предполагается присутствие цианатов, а также большинства азотсодержащих органических соединений), при рН 7,4 (когда предполагается присутствие карбамида) и из сильнощелочной среды (если анализируют сточные воды, содержащие большие количества фенолов – сточные воды коксохимических заводов, газогенераторных предприятий и др.). Если наряду с фенолами присутствуют вещества, гидролизующиеся в щелочной среде, то отгонку надо провести дважды: сначала при рН = 7,4, собирая отгон в разбавленный раствор сильной кислоты, потом подщелочив этот отгон до сильнощелочной реакции.
Поглотителем аммиака служит раствор борной кислоты, когда определение заканчивают титрованием или фотометрическим методом с реактивом Несслера. При применении фенол – гипохлоритного метода отогнанный аммиак поглощают раствором серной кислоты. Отгонку проводят из круглодонной колбы вместимостью от 800 до 2000 см 3 с вертикальным холодильником, конец которого (или форштос) надо погрузить в раствор кислоты, находящийся в приемнике.
Реактивы и оборудование для отгонки
Безаммиачная вода: бидистиллят пропускают через колонку с катионитом КУ-2
Боратный буферный раствор, рН 9,54: к 500 см 3 0,025 М раствора тетрабората натрия, содержащего 9,5 г/дм 3 Na2B4O7 ×10H2O, приливают 88 см 3 0,1 Н раствора NaOH и разбавляют безаммиачной водой до 1 дм 3
Фосфатный буферный раствор, рН 7,4.
Дехлорирующий раствор: 3,5 г Na2S2O3 5H2O растворяют в безаммиачной воде и разбавляют до 1 дм 3
Поглощающие растворы: 0,2 Н Н2SO4 или 0,2 Н HCl, или раствор борной кислоты: растворяют 40 г Н3ВО3 в безаммиачной воде и разбавляют такой же водой до 1 дм 3
Колбы для отгонки, холодильник
Мерные цилиндры, мерная колба
Ход отгонки.Отгонку следует проводить в комнате, воздух которой не содержит аммиака. В колбу для отгонки вместимостью 800 – 1000 см 3 помещают 400 см 3 анализируемой сточной воды (или меньший объем, разбавленный до 400 см 3 безаммиачной водой). Если проба содержит «активный хлор», ее предварительно дехлорируют добавлением эквивалентного количества дехлорирующего реагента. Пробу нейтрализуют, если надо, до рН = 7 разбавленной кислотой или щелочью, определив необходимое количество титрованием отдельной порции. Затем приливают 25 см 3 буферного раствора (рН = 9,5 или 7,4 в зависимости от предполагаемых загрязнений) или 20 см 3 раствора едкого натра при анализе фенольных вод. В приемник наливают указанное количество поглощающего раствора: при титриметрическом методе или фотоколориметрическом методе с реактивом Несслера – 50 см 3 раствора борной кислоты, при фотометрическом фенол-гипохлоритном методе 40 см 3 0,2 Н Н2SO4 или HCl.
Отгоняют 300 см 3 жидкости, количественно переносят отгон в мерную колбу вместимостью 500 см 3 , разбавляют до метки безаммиачной дистиллированной водой и перемешивают.
Определение аммиака. К аликвотной части полученного после перегонки раствора (или ко всему раствору, не разбавляя его в мерной колбе) прибавляют несколько капель индикатора бромфенолового синего или метилового красного и титруют 0,02 н. раствором серной кислоты до изменения окраски индикатора. Проводят холостой опыт со всеми примененными в анализе реактивами: используют те же количества раствора борной кислоты, индикатора, вместо отгона используют дистиллированную воду, освобожденную от СО2 кипячением

Расчет.Содержание аммонийных ионов (Х) в мг/дм 3 находят по формуле:
где V1 – объем 0,02 н. серной кислоты, израсходованной на титрование пробы, см 3 ;
V2 – объем 0,02 н. серной кислоты, израсходованной в холостом опыте, см 3 ;
Н – концентрация титранта — серной кислоты, моль-экв/дм 3 ;
К – поправочный коэффициент к концентрации титранта;
Vпробы – объем воды, взятой для анализа, см 3 ;
Vаликв – объем отобранной аликвотной части, см 3 ;
V3 –объем мерной колбы, до которого был разбавлен отгон, см 3 ;
ЭNH4 – моль-эквивалент катиона аммония, г/моль-эквивалент;
1000 – коэффициент для перехода от граммов к миллиграммам.
Источник
ПНД Ф 14.1:2:3.1-95 ФР 1.31.2017.27257 Количественный химический анализ вод. Методика измерений массовой концентрации ионов аммония в природных и сточных водах фотометрическим методом с реактивом Несслера / МИ / 14 1 2 3 1 95 1 31 2017 27257
ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ
В СФЕРЕ ПРИРОДОПОЛЬЗОВАНИЯ
Директор ФГБУ
«Федеральный центр анализа и
оценки техногенного воздействия»
___________________ В.В. Новиков
КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ ВОД
МЕТОДИКА ИЗМЕРЕНИЙ
МАССОВОЙ КОНЦЕНТРАЦИИ
ИОНОВ АММОНИЯ
В ПРИРОДНЫХ И СТОЧНЫХ ВОДАХ
ФОТОМЕТРИЧЕСКИМ МЕТОДОМ
С РЕАКТИВОМ НЕССЛЕРА
Методика допущена для целей государственного
экологического контроля
МОСКВА
(Издание 2017 г)
Методика измерений аттестована Центром метрологии и сертификации «СЕРТИМЕТ» Уральского отделения РАН (Аттестат аккредитации № RA.RU.310657 от 12.05.2015), рассмотрена и одобрена федеральным государственным бюджетным учреждением «Федеральный центр анализа и оценки техногенного воздействия» (ФГБУ «ФЦАО»).
Настоящее издание методики введено в действие взамен предыдущего издания ПНД Ф 14.1:2.1-95 (издание 2004 г.) и действует с 01 сентября 2017 года до выхода нового издания.
Сведения об аттестованной методике измерений переданы в Федеральный информационный фонд во обеспечению единства измерений.
Заместитель директора ФГБУ «ФЦАО»
Адрес: 117105, г. Москва, Варшавское шоссе, 39А
1 ВВЕДЕНИЕ
Круговорот азота в природе, находящегося в формах аммиака, нитрита, нитрата, органически связанного и свободного азота — азота неорганических и органических соединений, имеет огромное значение для функционирования биосферы.
Аммиачный азот в различных концентрациях содержится в воде многих источников. Аммиак и ионы аммония могут быть обнаружены в грунтовых водах как продукты процессов жизнедеятельности микроорганизмов, в поверхностных природных водах в небольших количествах в период вегетации в результате разложения белковых веществ, а также в результате загрязнения природных вод хозяйственно-бытовыми сточными и промышленными водами. Соединения азота, содержащиеся в сточных водах (преимущественно в виде аммонийного азота, азота нитратов, азота нитритов и азота, связанного в органических соединениях), при поступлении в поверхностные водоемы наносят значительный ущерб экологической системе.
Настоящий документ устанавливает методику количественного химического анализа (методику измерений), предназначенную для измерений массовой концентрации ионов аммония (суммарной массовой концентрации ионов аммония и свободного аммиака 1 ) от 0,05 до 150 мг/дм 3 в природных (поверхностных и подземных) и сточных водах (в том числе производственных, промышленных, очищенных, талых, ливневых, хозяйственно-бытовых) фотометрическим методом с реактивом Несслера.
1 Отклонение концентрации свободного аммиака (NH3) к ионам аммония (NH4 + ) зависит от концентрации водородных ионов.
Методика применяется в лабораториях, осуществляющих испытания (анализ, контроль, мониторинг) природных и сточных вод.
Мешающие влияния, обусловленные присутствием аминов, хлорамина, ацетона, альдегидов, спиртов, фенолов, компонентов жесткости воды, взвешенных веществ, железа, сульфидов, хлора, гуминовых веществ, устраняются специальной подготовкой пробы к анализу.
Допускается разбавление пробы в диапазоне, соответствующем регламентированному.
При невозможности устранения мешающих влияний (аминов, хлораминов, альдегидов и других соединений) с помощью процедур пробоподготовки, предусмотренных настоящим нормативным документом, рекомендуется выполнять анализ с использованием другого метода анализа.
При проведении контроля аммоний-иона необходимо периодически знакомиться с нормативно-правовыми документами, определяющими нормативы вещества на текущий момент, так как к нормативу могут предъявляться различные требования для разных областей. Например, в соответствии с Постановлением Правительства РФ от 29.07.2013 г. № 644 «Об утверждении Правил холодного водоснабжения и водоотведения и о внесении изменений в некоторые акты Правительства Российской Федерации» максимальное допустимое значение нормативных показателей общих свойств сточных вод и концентраций загрязняющих веществ в сточных водах, установленные в целях предотвращения негативного воздействия на работу централизованных ливневых систем водоотведения, а также централизованных комбинированных систем водоотведения (применительно к сбросу в ливневые системы водоотведения), для азота аммонийного составляет 2 мг/л; в соответствии с ГН 2.1.5.1315-03 «Предельно допустимые концентрации (ПДК) химических веществ в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования» ПДК в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования для аммиака и аммоний-иона (по азоту) составляет 1,5 мг/л; согласно Приказу Минсельхоза РФ от 13.12.2016 г. № 552 «Об утверждении нормативов качества воды водных объектов рыбохозяйственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйственного значения» ПДК Аммоний-ион NH4 + 0,5 мг/дм 3 (в пересчете на азот 0,4 мг/дм 3 ).
2 ТРЕБОВАНИЯ К ПОКАЗАТЕЛЯМ ТОЧНОСТИ ИЗМЕРЕНИЙ
Методика обеспечивает выполнение требований к точности измерений, установленных для измерений массовых концентраций неорганических и органических веществ в поверхностных, подземных, сточных водах Приказом Минприроды от 7 декабря 2012 г. № 425 «Об утверждении перечня измерений, относящихся к сфере государственного регулирования обеспечения единства измерений и выполняемых при осуществлении деятельности в области охраны окружающей среды, и обязательных метрологических требований к ним, в том числе показателей точности измерений», а также выполнение измерений с погрешностью (неопределенностью), не превышающей норм точности измерений показателей состава и свойств вод, установленных ГОСТ 27384-2002.
Настоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведенных в таблице 1.
Диапазон измерений массовой концентрации ионов аммония, мг/дм 3
Показатель точности (границы относительной погрешности при вероятности Р = 0,95), ±δ, %
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости) σ r , %
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), σ R , %
Источник