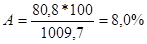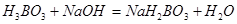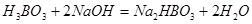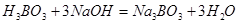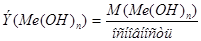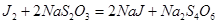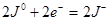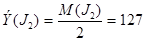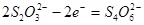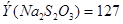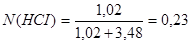- Концентрация растворов. Способы выражения концентрации растворов.
- Способы выражения концентрации растворов.
- Концентрация растворов в фармации.
- Концентрация подразделяется на:
- Весовая концентрация:
- Объемная концентрация:
- Массо-объемная концентрация:
- Способы и методы выражения концентрации растворов в аптеках.
- 1) Процентная концентрация раствора:
- 2) Концентрация раствора соотношением:
- Задачи на концентрацию растворов:
- Способы выражения концентрации раствора
Концентрация растворов. Способы выражения концентрации растворов.
Концентрация раствора может выражаться как в безразмерных единицах (долях, процентах), так и в размерных величинах (массовых долях, молярности, титрах, мольных долях).
Концентрация – это количественный состав растворенного вещества (в конкретных единицах) в единице объема или массы. Обозначили растворенное вещество — Х, а растворитель — S. Чаще всего использую понятие молярности (молярная концентрация) и мольной доли.
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:

ω – массовая доля растворенного вещества;
mв-ва – масса растворённого вещества;
Массовую долю выражают в долях от единицы или в процентах.
2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:

C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl);
n – количество растворенного вещества, моль;
V – объём раствора, л.
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества.
3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:

С (x) – моляльность, моль/кг;
n – количество растворенного вещества, моль;
4. Титр – содержание вещества в граммах в 1 мл раствора:

T – титр растворённого вещества, г/мл;
mв-ва – масса растворенного вещества, г;
5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:

N – мольная доля растворённого вещества;
n – количество растворённого вещества, моль;
nр-ля – количество вещества растворителя, моль.
Сумма мольных долей должна равняться 1:
Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
ω(X) — массовая доля растворенного вещества, в %;
М(Х) – молярная масса растворенного вещества;
ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента) – число грамм-эквивалентов данного вещества в одном литре раствора.
Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.

СН – нормальная концентрация, моль-экв/л;
z – число эквивалентности;
Растворимость вещества S — максимальная масса вещества, которая может раствориться в 100 г растворителя:
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя:
Источник
Концентрация растворов в фармации.
Концентрация – определенное количество лекарственного вещества в определенном (необходимом) количестве растворителя.
Концентрация подразделяется на:
— Весовую;
— Объемную;
— Массо-объемную.
Весовая концентрация:
При данной концентрации и вещество и растворитель берут по массе (весовое количество).
В данной концентрации готовят:
— масляные растворы;
— глицериновые растворы;
— суспензии с процентом нерастворимых веществ три и более;
— эмульсии;
— гомеопатические лекарственные формы.
Объемная концентрация:
В этом случае растворенное вещество берется по объему и добавляется растворитель до получения нужного общего объема раствора.
В данной концентрации готовят: растворы газов в воде.
Массо-объемная концентрация:
Лекарственное вещество берется по массе (граммы), а растворитель доводится до требуемого объема раствора (миллилитры).
В данной концентрации готовят:
— водные растворы;
— спиртовые растворы;
— суспензии с процентом нерастворимого вещества меньше трех.
Друзья я вот тут задумался что-то, как все таки правильно: массо-объемная или массово-объемная концентрация, кто знает напишите в комментариях!?

Способы и методы выражения концентрации растворов в аптеках.
Рассмотрим 2 способа обозначения концентраций, которые применяются в аптеках и в фармации в целом:
1) Процентная концентрация раствора:
Процент показывает количество лекарственного вещества:
— в граммах находящееся в 100 мл раствора при массо-объемной концентрации;
— в граммах, находящееся в 100 граммах раствора при весовой концентрации;
— в миллилитрах в 100 мл раствора при объемной концентрации.
2) Концентрация раствора соотношением:
Концентрация раствора может также обозначаться соотношением весового количества растворенного лекарственного вещества ко всему количеству раствора.
| — 1 : 10 (1 часть растворенного лекарственного вещества в 10 частях раствора); — 1 : 100 (1 часть растворенного лекарственного вещества в 100 частях раствора); Очень редко концентрацию раствора могут обозначать соотношением весового количества растворенного лекарственного вещества к количеству взятого растворителя, то есть 1 + 9 (1 часть растворенного лекарственного вещества + 9 частей растворителя). |
Задачи на концентрацию растворов:
1) 5% раствор перевести в соотношение.
| 5,0 — 100 мл раствора 1,0 — х , следовательно: х = 20 А значит, что 5% концентрация равна соотношению 1:20. |
2) Соотношение 1:5 перевести в процент.
| 1,0 вещества в 5 мл раствора х — 100мл раствора следовательно: х = 20 А значит, что соотношение 1:5 соответствует 20% концентрации. |
Друзья в ближайшее время будет статья о приготовлении растворов, там так же будут разобраны различные примеры и задачи. Не пропустите ее, вступив в наши группы и подписавшись по @mail !
А на сегодня все, предлагаю посмотреть очередное красивейшее видео:
Источник
Способы выражения концентрации раствора



МИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
Государственное образовательное учреждение высшего профессионального образования
«Тюменский государственный нефтегазовый университет»
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к контрольным заданиям по дисциплине «Химия»
для студентов нехимических специальностей
заочной формы обучения
Утверждено редакционно-издательским советом
Тюменского государственного нефтегазового университета
Составители: доцент к. х. н. Андрианова Л. И.
доцент к. х. н. Пнёва А. П.
доцент, к. х. н., Обухов В. М.
© Государственное образовательное учреждение высшего профессионального образования
«Тюменский государственный нефтегазовый университет»
РАСТВОРЫ
Способы выражения концентрации раствора
Растворы имеют важное значение в жизни и практической деятельности человека. Производства, в основе которых лежат химические процессы, обычно связаны с использованием растворов. Раствором называется твердая или жидкая гомогенная система, состоящая из двух или более компонентов, относительные количества которых могут изменяться в широких приделах. Наиболее важный вид растворов – жидкие растворы.
Всякий раствор состоит из растворенных веществ и растворителя, т.е. среды, в которой эти вещества равномерно распределены в виде молекул или ионов. Обычно растворителями считают тот компонент, который в чистом виде существует в таком же агрегатном состоянии, что и полученный раствор. Растворение является обратимым процессом. Когда скорость растворения кристаллического вещества, становится равной обратному процессу, процессу кристаллизации, наступает динамическое равновесие, при котором в единицу времени столько же молекул растворяется, сколько и выделяется из раствора. Раствор, находящийся в равновесии с растворяющимся веществом, называется насыщенным раствором. Насыщенными растворами приходится пользоваться сравнительно редко. В большинстве случаев употребляют растворы ненасыщенные, т.е. с меньшей концентрацией растворенного вещества, чем в насыщенном растворе.
Концентрация раствора – это количество вещества, заключенного в определенном весовом или объемном количестве раствора или растворителя.
Существуют различные способы выражения концентраций растворов:
1) массовая доля растворенного вещества или процентная концентрация показывает число граммов растворенного вещества в 100 граммах раствора.
Если g1 – масса растворенного вещества, g2 – масса раствора, то процентная концентрация А равна:
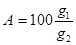
Например, растворено 80,8 г. уксусной кислоты СН3СООН в 1 л. раствора и полученный раствор имеет плотность 1,0097 г/см 3 . Рассчитаем процентную концентрацию.
Масса раствора равна g = V*d, V – объем раствора, d – его плотность, т. е. 
2) в химии часто используются объемные концентрации, поскольку жидкие растворы удобно измерять по объему, а не по весу.
Рассмотрим молярную концентрацию – С (моль/л). Она показывает число грамм-молей растворенного вещества в 1 литре раствора.
Например, пересчитаем концентрацию А соляной кислоты в молярную концентрацию
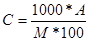
где М – молекулярный вес растворённого вещества HCI (36,5 г/моль). Тогда 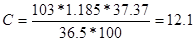
3) моляльная концентрация – это число молей, растворённого вещества в 1000 г, растворителя.
Например, вес раствора объёмом 1 л равен 1185 г, в этом количестве раствора содержится:
100 г – 37,27 г HCI
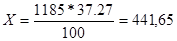
4) нормальная концентрация (нормальность) означает число грамм-эквивалентов вещества, содержащихся в 1 л раствора.
Эквивалентом элементов называется число, которое показывает, сколько весовых частей элемента соединяется с 8 весовыми частями кислорода или с 1 весовой частью водорода или замещает те же количества водорода или кислорода в их соединениях при химических превращениях.
Теперь можно сформулировать закон эквивалентов: элементы соединяются между собой и замещают друг друга в количествах, пропорциональных их эквивалентам, т.е.
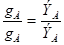
где gА и gВ – массы взаимодействующих элементов А и В, ЭА и ЭВ – эквиваленты элементов А и В. отсюда следует, что эквивалент водорода ЭН, а эквивалент кислорода Э0 = 8.

Эквиваленты других элементов можно определить по составу их соединений с другим элементом, эквивалент которого известен.
Грамм-эквивалентом называется число граммов вещества, равное по своей величине его эквиваленту.
Эквивалент элемента можно посчитать, разделив атомную массу М на валентность элемента 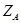
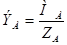
Если элемент имеет несколько соединений с разными валентностями, то его эквиваленты также различны, но относятся между собой как целые числа. Особенно широко применяется закон эквивалентов в аналитической химии.
Пусть V1 – объем одного раствора, мл.,
V2 – объем второго раствора, мл.,
N1 – нормальность первого раствора, г – экв./л,
Уравнение (5) лежит в основе всех расчетов в объемном аналитическом анализе.
Для соединений эквивалент вычисляется на основании химической реакции, у которой это соединение участвует.
Например, для реакции:
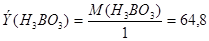
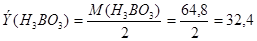
Наконец, для реакции:
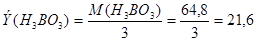
Следовательно, эквивалент кислоты равен её молекулярному весу, делённому на основность кислоты, т.е. на количество замещённых атомов водорода. Аналогично для оснований эквивалент равен молекулярному весу, делённому на основность (число диссоциирующих гидроксильных групп).
Эквивалент соли равен её молекулярному весу, делённому на произведение валентности металла на число атомов этого металла в молекуле.
Например, молекулярный вес 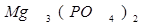
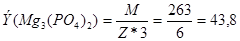
где Z=2 – валентность магния в соли.
В окислительно-восстановительном процессе участвуют и окислители, и восстановители.
Окислительным эквивалентом называется количество окислителя, приходящееся на один электрон, отдаваемым восстановителем в данной реакции. Оба эти эквивалента рассчитываются по формуле:
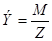
где М – молекулярный вес окислителя или восстановителя, Z – число электронов.
Например, для реакции
окислитель:
восстановитель:
Расчёт нормальности можно проводить по формуле, аналогичной формуле (2), только вместо молекулярного веса следует взять эквивалентный вес:
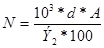
где 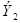
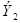
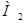
5) Мольная доля Ni растворенного вещества, i – это число молей компонента на 1 моль раствора.
Эта концентрация наиболее удобна в теоретических уравнениях. Рассмотрим пример с соляной кислотой, концентрация которой 37,27%. Число молей растворенного вещества:
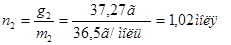
Число молей растворителя:
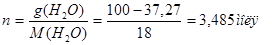
Мольная доля кислоты:
Мольная доля в этом растворе 1,0-0,23 = 0,77.
Вычисления при приготовлении и разбавлении растворов.
Рассмотрим типичные расчеты при приготовлении рабочих растворов.
1. Приготовление раствора нужной нормальности N в количестве V мл. Пусть g – навеска исходного вещества в граммах. Следует отвесить:
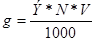
Источник