Определение аминного азота медным способом
Необходимые реактивы и посуда:
Суспензия фосфата меди, состоящая из смеси хлорида меди (27,3 г соли растворяют в 1 дм³ воды), трехзамещенного фосфата натрия (64,5 г гидроортофосфата натрия растворяют в 500 см³ воды, добавляют 7,2 г гидроксида натрия и доводят до 1 дм³) и боратный буферный раствор (57,21 г буры растворяют в 1,5 дм³ воды, добавляют 100 см³ 1 М раствора соляной кислоты и доводят до 2 дм³), смесь состоит из компонентов в соотношении 1:2:2 и готовится в день анализа. Спиртовой раствор тимолфталеина; 1 М раствор ΝаОН; 0,01 М раствор тиосульфата натрия, 1 % раствор крахмала, 80 % уксусная кислота, 10 % раствор КJ или 1г КJ.
Мерная колба вместимостью 50 см³, коническая колба вместимостью 150 см³, воронка, фильтровальная бумага, пипетки вместимостью 10, 5, 2 см³, цилиндр вместимостью 50 см³.
Расход сусла 5 см³ на один анализ.
В мерную колбу вместимостью 50 см³ помещают 5 см³ сусла, прибавляют 2-3 капли тимолфталеина и 2-3 капли 1 М раствора ΝаОН до появления бледно-голубого окрашивания сусла. В несколько приемо, при перемешивании, добавляют 15 см³ суспензии фосфата меди, затем содержимое колбы доводят до метки дистиллированной водой. Смесь перемешивают и фильтруют через бумажный фильтр, возвращая на фильтр первые порции фильтрата.
10 см³ прозрачного фильтрата помещают в коническую колбу вместимостью 150 см³ и добавляют 0,5 см³ 80 % уксусной кислоты, 1г или 10 см³ 10 % раствора КJ. Содержимое колбы размешивают и выделившийся свободный йод оттитровывают 0,01 М раствором тиосульфата натрия, добавляя в конце титрования 1-2 капли 1 % раствора крахмала. Конец титрования определяют по исчезновению синей окраски раствора. Титрование заканчивается при переходе синего окрашивания раствора в безцветный. Содержание аминного азота рассчитывают по формулам:
Содержание аминного азота в 100 см³ сусла определяют по формуле 1.4:
х = 
Содержание аминного азота в 100 г экстракта определяют по формуле 1.5:
х = 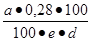
где: а- объем 0,01 М раствора тиосульфата натрия, пошедшего на
0,28- количество мг аминного азота, эквивалентное 1 см³ раствора
тиосульфата натрия концентрацией 0,01 М;
20 – перевод в 100 см³ сусла;
е — массовая доля сухих веществ в сусле, %;
d — относительная плотность сусла.
По количеству аминного азота в солоде судят о степени растворения белков. Солод считается перерастворенным, если содержит более 230 мг на 100 г экстракта аминного азота, очень хорошо растворен, если содержит 200-230 мг на 100 г экстракта аминного азота, хорошо растворен, если содержит 180-200 мг на 100 г экстракта аминного азота и плохо растворен, если содержит менее180 мг на 100 г экстракта аминного азота.
Дата добавления: 2015-02-10 ; просмотров: 1937 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Источник
Определение аминного азота медным способом



Необходимые реактивы и посуда:
Суспензия фосфата меди, состоящая из смеси хлорида меди (27,3 г соли растворяют в 1 дм³ воды), трехзамещенного фосфата натрия (64,5 г гидроортофосфата натрия растворяют в 500 см³ воды, добавляют 7,2 г гидроксида натрия и доводят до 1 дм³) и боратный буферный раствор (57,21 г буры растворяют в 1,5 дм³ воды, добавляют 100 см³ 1 М раствора соляной кислоты и доводят до 2 дм³), смесь состоит из компонентов в соотношении 1:2:2 и готовится в день анализа. Спиртовой раствор тимолфталеина; 1 М раствор ΝаОН; 0,01 М раствор тиосульфата натрия, 1 % раствор крахмала, 80 % уксусная кислота, 10 % раствор КJ или 1г КJ.
Мерная колба вместимостью 50 см³, коническая колба вместимостью 150 см³, воронка, фильтровальная бумага, пипетки вместимостью 10, 5, 2 см³, цилиндр вместимостью 50 см³.
Расход сусла 5 см³ на один анализ.
В мерную колбу вместимостью 50 см³ помещают 5 см³ сусла, прибавляют 2-3 капли тимолфталеина и 2-3 капли 1 М раствора ΝаОН до появления бледно-голубого окрашивания сусла. В несколько приемо, при перемешивании, добавляют 15 см³ суспензии фосфата меди, затем содержимое колбы доводят до метки дистиллированной водой. Смесь перемешивают и фильтруют через бумажный фильтр, возвращая на фильтр первые порции фильтрата.
10 см³ прозрачного фильтрата помещают в коническую колбу вместимостью 150 см³ и добавляют 0,5 см³ 80 % уксусной кислоты, 1г или 10 см³ 10 % раствора КJ. Содержимое колбы размешивают и выделившийся свободный йод оттитровывают 0,01 М раствором тиосульфата натрия, добавляя в конце титрования 1-2 капли 1 % раствора крахмала. Конец титрования определяют по исчезновению синей окраски раствора. Титрование заканчивается при переходе синего окрашивания раствора в безцветный. Содержание аминного азота рассчитывают по формулам:
Содержание аминного азота в 100 см³ сусла определяют по формуле 1.4:
х = 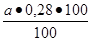
Содержание аминного азота в 100 г экстракта определяют по формуле 1.5:
х = 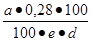
где: а- объем 0,01 М раствора тиосульфата натрия, пошедшего на
0,28- количество мг аминного азота, эквивалентное 1 см³ раствора
тиосульфата натрия концентрацией 0,01 М;
20 – перевод в 100 см³ сусла;
е — массовая доля сухих веществ в сусле, %;
d — относительная плотность сусла.
По количеству аминного азота в солоде судят о степени растворения белков. Солод считается перерастворенным, если содержит более 230 мг на 100 г экстракта аминного азота, очень хорошо растворен, если содержит 200-230 мг на 100 г экстракта аминного азота, хорошо растворен, если содержит 180-200 мг на 100 г экстракта аминного азота и плохо растворен, если содержит менее180 мг на 100 г экстракта аминного азота.
Источник
ГК «Униконс»
Продвижение и реализация комплексных пищевых добавок, антисептиков и др. продукции.
«Антисептики Септоцил»
Септоцил. Бытовая химия, антисептики.
«Петритест»
Микробиологические экспресс-тесты. Первые результаты уже через 4 часа.
«АльтерСтарт»
Закваски, стартовые культуры. Изготовление любых заквасок для любых целей.
- Вы здесь:
- Библиотека технолога
- Пиво и напитки
- Т.В. Меледина — Сырье и вспомогательные материалы в пивоварении
Приложение 5. Определение аминного азота
Определение аминного азота (медный способ)
Анализ проводится методом, который основан на способности большинства аминокислот и пептидов образовывать растворимые комплексные соединения с медью (медный способ). Избыток меди оттитровывают, а ее количество, эквивалентное аминному азоту, переводят в соль уксусной кислоты и определяют количественно йодометрическим титрованием.
Приборы: мерная колба вместимостью 50 мл; бумажный фильтр.
Реактивы: раствор хлорной меди (27,3 г хлорной меди растворяют в 1 л дистиллированной воды); раствор трехзамещенного фосфата натрия (64,5 г двухосновного фосфата натрия растворяют в 500 мл дистиллированной воды с удаленным СО2, добавляют 7,2 гидроксида натрия, после растворения доливают водой до 1 л); боратный буферный раствор (57,21 г буры растворяют в 1,5 л воды, добавляют 100 мл 1 н раствора соляной кислоты и доводят водой до 2 л); суспензия фосфорнокислой меди (1 объем хлорной меди смешивают с 2 объемами раствора боратного буфера; суспензию можно использовать в течение 2-3 суток); раствор тимолфталеина (0,25 г тимолфталеина растворяют в 100 мл 50%-ного этилового спирта); 0,01н раствор тиосульфата натрия (готовится ежедневно путем разбавления 0,1 н раствора тиосульфата натрия с последующей проверкой титра по К2JО3; 1%-ный раствор крахмала; 80% (ледяная) уксусная кислота.
Ход анализа. В мерную колбу вместимостью 50 мл помещают 10 мл прозрачного сусла, прибавляют 3-4 капли тимолфталеина и 1н раствор гидрооксида натрия до бледно-голубого окрашивания. Осторожно при перемешивании приливают 30 мл суспензии фосфорнокислой меди и доводят до метки дистиллированной водой. Полученную смесь после перемешивания фильтруют через бумажный фильтр, перефильтровывая первые порции фильтрата
Прозрачный фильтрат (10 мл) подкисляют 0,5 мл 80%-ной уксусной кислоты, прибавляют к нему 1 г йодистого калия и после размешивания оттитровывают выделившийся йод 0,01н раствором тиосульфата натрия. Под конец титрования добавляют 1-2 капли раствора крахмала. Титрование заканчивают при обесцвечивании раствора от одной капли тиосульфата натрия.
Количество пошедшего на титрование тиосульфата натрия, умноженное на 0,28, дает содержание аминного азота в 10 мл фильтрата, что соответствует 2 мл сусла с учетом разбавления.
Количество аминного азота Nа (в мг) в 100 мл сусла вычисляется по формуле:
где n – количество 0,01н раствора тиосульфата натрия, пошедшее на титрование выделившегося йода, мл.
Пример. На титрование пошло 1,8 мл тиосульфата. Содержание аминного азота в 100 мл сусла будет
Источник
Исследование содержания аминного азота



Аминный азот включает в себя азот аминокислот и пептидов. Его количество в солоде дает представление о распаде белков и степени растворения солода, а следовательно, и его качества. Считают, что солод перерастворен, если в 100 г экстракта содержится свыше 230 мг аминного азота, очень хорошо растворен – 230-200 мг, хорошо растворен –200-180 мг. Следует учитывать, что количество аминного азота повышается с увеличением содержания общего азота.
Содержание аминного азота колеблется для светлых сортов пива в пределах 13-30 мг, для пива с добавками несоложеного сырья 10-14 мг на 100 см 3 пива. Аминный азот составляет 28-32% общего азота.
Существует несколько способов определения аминного азота. Наиболее прост и удобен так называемый медный способ.
В основу метода положена способность аминокислот образовывать растворимые соединения с медью, количество которой определяют йодометрическим титрованием. Сущность метода заключается в том, что к слабощелочному раствору аминокислот прибавляют избыток суспензии ортофосфата меди Cu(РО4)2 в обратном буферном растворе. Для отделения образовавшихся при этом растворимых медных соединений от нерастворимого ортофорсфата меди смесь фильтруют. Затем к фильтрату прибавляют уксусную кислоту, которая отщепляет медь от комплексного соединения и превращается в ацетат меди.
Для определения количества меди, участвующей в реакциях, к раствору добавляют йодит калия: 2Cu (СН3СОО)2 + 4КJ = J2 +2 CuJ + 4СН3СООК. В результате реакции выделяется йод в количестве, эквивалентном количеству меди, а следовательно, и азоту аминокислот, который оттитровывают раствором тиосульфата натрия: J2 + Na2S2O3 = 2NaJ + Na 2S4O6. 1 см 3 0,01 н раствора тиосульфата натрия соответствует 0,28 мг аминного азота, так как один атом меди реагирует с двумя молекулами аминокислот, образуя соединения типа Cu (RСНNН2СОО)2.
Реактивы. Раствор хлорида меди (27,3 г соли растворяют в 1 дм 3 воды); раствор фосфата натрия (64,5 г гидроортофосфата натрия Na 2Н РО4 растворяют в 500 см 3 дистиллированной воды, освобожденной от СО2, добавляют 7,2 г гидроксида натрия и после растворения доливают водой до 1 дм 3 ); боратный буферный раствор (57,21 г буры растворяют в 1,5 дм 3 воды, добавляют 100 см 3 1н раствора соляной кислоты и доводят водой до 2 дм 3 ) суспензия фосфата меди (один объем раствора хлорида меди смешивают с двумя объемами раствора фосфата натрия и добавляют два объема боратного буферного раствора. Суспензия хранится не более 3 дней); раствор тимолфталеина (0,25 г индикатора в 100 см 3 50%-го спирта); 0,01 н раствор тиосульфата натрия; 1%-й раствор крахмала; 80%-я или ледяная уксусная кислота; 1н раствор гидроксида натрия; 10%-й раствор йодида калия.
Ход определения. В мерную колбу на 50 см 3 пипеткой вносят 5-10 см 3 исследуемого раствора, добавляют 3-4 капли тимолфталеина и по каплям 1 н раствор гидроксида натрия до появления бледно-голубой окраски. К слабощелочному раствору из цилиндра при помешивании приливают 30 см 3 суспензии фосфата меди, содержимое колбы доводят водой до метки, перемешивают и фильтруют через плотный фильтр. Фильтрат должен быть совершенно прозрачным.
Затем 10 см 3 фильтрата пипеткой переносят в коническую колбу, добавляют 0,5см 3 уксусной кислоты и 10 см 3 раствора йодита калия. После перемешивания выделившийся йод титруют из микробюретки 0,01 н раствором тиосульфата натрия, прибавляя в конце титрования 1-2 капли раствора крахмала. Конец титрования определяют по исчезновению синей окраски.
При принятом разбавлении количество аминного азота рассчитывают по уравнению
Х = а × 0,28 ×100 / 2, (21)
где а – количество 0,01 н раствор тиосульфата натрия, пошедшее на титрование, см 3 .
Пример.На анализ взято 10 см 3 пивного сусла. На титрование выделившегося йода в 10 см 3 фильтрата пошло 1,16 см 3 0,01 н. раствора тиосульфата натрия. В 100 см 3 пивного сусла содержится : Х = 1,16 × 0,28 × 100 / 2 = 16,24 мг аминного азота.
Таблица 8 – Содержание азота в сырье, полуфабрикатах и продуктах бродильных производств
Источник












