- Номенклатура и классификация ферментов
- 4. Локализация ферментов в клетке
- Номенклатура ферментов: описание, классификация, строение и принципы построения
- Общая характеристика ферментов
- Классификация энзимов
- Оксидоредуктазы
- Трансферазы
- Гидролазы
- Лиазы
- Лигазы
- Изомеразы
- Классификационный номер фермента
- Принципы номенклатуры ферментов
- Тривиальная номенклатура
- Рациональная номенклатура
- Рабочая номенклатура
- Систематическая номенклатура ферментов
Номенклатура и классификация ферментов
Ферментология очень долго не располагала строго научной номенклатурой ферментов. Наименования ферментам давали по случайным признакам (тривиальная номенклатура), по названию субстрата (рациональная), по химическому составу фермента, наконец, по типу катализируемой реакции и характеру субстрата.
Примерами тривиальной номенклатуры могут служить названия таких ферментов, как пепсин (от греч. пепсис — пищеварение), трипсин (от греч. трипсис — разжижаю) и папаин (от названия дынного дерева Carica papaja, из сока которого он выделен).
Согласно современной номенклатуре название ферментов составляют из химического названия субстрата и названия той реакции, которая осуществляется ферментом. Если химическая реакция, ускоряемая ферментом, сопровождается переносом группировки атомов от субстрата к акцептору, название фермента включает также химическое наименование акцептора. Все ферменты имеют окончание «аза», прибавленное к названию субстрата.
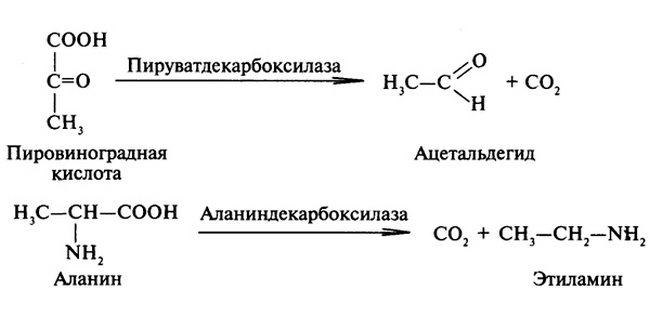
Например, пируват — декарбоксил — аза, сукцинат — дегидроген — аза
В принятой классификации ферменты объединены в группы по типу важнейших биохимических процессов, лежащих в основе жизнедеятельности любого организма. По этому принципу все ферменты делят на 6 классов.
Оксидоредуктазы — ускоряют реакции окисления — восстановления.
Трансферазы — ускоряют реакции переноса функциональных групп и молекулярных остатков.
Гидролазы — ускоряют реакции гидролитического распада.
Лиазы — ускоряют негидролитическое отщепление от субстратов определенных групп атомов с образованием двойной связи (или присоединяют группы атомов по двойной связи).
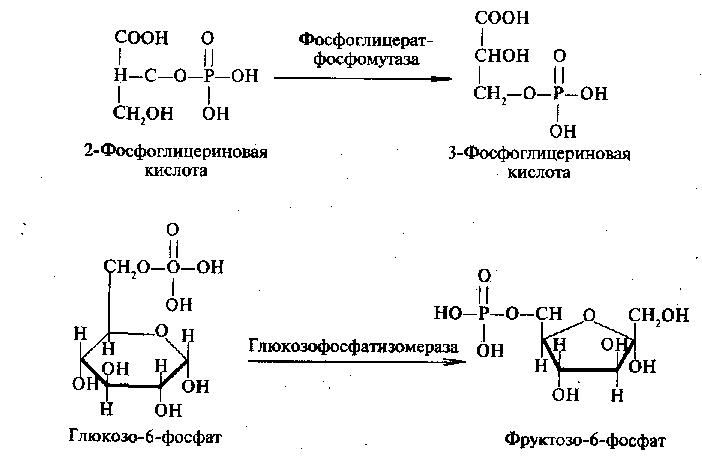
Изомеразы — ускоряют пространственные или структурные перестройки в пределах одной молекулы.
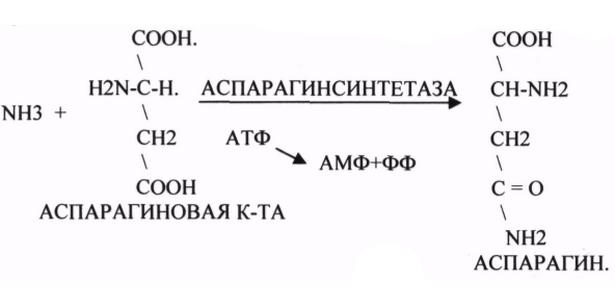
Лигазы — ускоряют реакции синтеза, сопряженные с распадом богатых энергией связей.
Эти классы и положены в основу новой научной классификации ферментов.
Каждому ферменту присваивается индивидуальный номер (шифр). Например, шифр уреазы выражается цифрами 3.5.1.5. Это означает, что уреаза относится к 3-му классу (первая цифра) ферментов, все представители которого катализируют реакции гидролиза. Вторая цифра (5) говорит о том, что уреаза принадлежит к 5-му подклассу этого класса, куда зачислены все ферменты, ускоряющие гидролиз С — N-связей, не являющихся пептидными. Третья цифра шифра (1) указывает на принадлежность уреазы к подподклассу 5-го подкласса, члены которого ускоряют гидролиз линейных амидов, а последняя цифра (5) — порядковый номер уреазы в этом подподклассе.
Таким образом, шифр абсолютно точно указывает место фермента в общем списке. В настоящее время принято в научных публикациях при первом упоминании фермента указывать в скобках его шифр.
4. Локализация ферментов в клетке
В клеточном содержимом ферменты распределены не хаотически, а строго упорядоченно. С современной точки зрения клетка представляется высокоорганизованной системой, в отдельных частях которой осуществляются строго определенные биохимические процессы. В соответствии с приуроченностью их к определенным субклеточным частицам или отсекам (компартментам) клетки в них локализованы те или иные индивидуальные ферменты, мультиэнзимные комплексы, полифункциональные ферменты или сложнейшие метаболоны.
Разнообразные гидролазы и лиазы сосредоточены преимущественно в лизосомах. Внутри этих сравнительно небольших (несколько нанометров в диаметре) пузырьков, ограниченных мембраной от гиалоплазмы клетки, протекают процессы деструкции различных органических соединений до тех простейших структурных единиц, из которых они построены.
Сложные ансамбли окислительно-восстановительных ферментов, такие, например, как цитохромная система, находятся в митохондриях. В этих же субклеточных частицах локализован набор ферментов цикла дикарбоновых и трикарбоновых кислот. Ферменты активирования аминокислот распределены в гиалоплазме, но они же есть и в ядре. В гиалоплазме присутствуют многочисленные метаболоны гликолиза, структурно объединенные с таковыми пентозофосфатного цикла, что обеспечивает взаимопереключение дихотомического и апотомического путей распада углеводов.
В то же время ферменты, ускоряющие перенос аминокислотных остатков на растущий конец полипептидной цепи и катализирующие некоторые другие реакции в процессе биосинтеза белка, сосредоточены в рибосомальном аппарате клетки. Нуклеотидилтрансферазы, ускоряющие реакцию переноса нуклеотидных остатков при новообразовании нуклеиновых кислот, локализованы в основном в ядерном аппарате клетки. Таким образом, системы ферментов, сосредоточенные в тех или иных структурах, участвуют в осуществлении отдельных циклов реакций. Будучи тонко координированы друг с другом, эти отдельные циклы реакций обеспечивают жизнедеятельность клеток, органов, тканей и организма в целом.
Нарушения структуры какого-либо фермента, ведущие к снижению его активности, приводят к нарушению метаболических путей, в которых участвует этот фермент. Такие нарушения почти всегда проявляются как болезни.
Повреждения ферментов бывают двух типов: наследственные дефекты строения фермента и повреждения, вызванные попадающими в организм токсическими веществами, ингибирующими фермент.
Нарушение синтеза фермента может привести к энзимопатиям, при которых недостаток одного фермента в метаболическом пути может вызвать нарушение образования конечного продукта. В силу взаимозависимости метаболических путей дефект одного фермента часто приводит к целому ряду нарушений в обмене веществ. Если фермент полностью отсутствует, то цепь реакций в таком месте разрывается. Существует вероятность, что избыточно накопленный субстрат может перейти на побочный путь метаболизма с образованием необычного и часто токсичного вещества.
Отдельные примеры энзимопатий (дисахаридозы, гликогенозы, агликогенозы, фенилпировиноградная олигофрения) будут рассмотрены при изучении следующих разделов.
Некоторые ферменты применяют как лечебные препараты:
— при их отсутствии или недостатке (наследственном или приобретенном), например, ферменты пищеварительного тракта (пепсин, трипсин, липаза) входят в состав лекарств, улучшающих переваривание;
— для специфического разрушения некоторых продуктов обмена (например, мочевины), тромбов, участков омертвевшей ткани на ранах.
Ферменты используют в клинико-диагностических лабораториях для измерения в крови концентрации глюкозы, жира, холестерина, активных форм кислорода и других веществ.
Такой анализ занимает несколько минут, при этом используется всего 10 мкл плазмы крови.
Для анализа часто используют иммобилизованные ферменты, которые искусственно связаны с нерастворимым в воде носителем, что повышает их стабильность.
В клинических лабораториях применяют готовые наборы реактивов, в состав которых входят ферменты, составляющие буфер соли, а также кофакторы. При использовании иммобилизованных ферментов для определения концентрации компонента крови достаточно нанести образец сыворотки на индикаторную пластинку и сравнить интенсивность окраски с эталоном.
В табл. 2 представлены основные направления и некоторые примеры использования ферментов в медицине.
В основе энзимодиагностики лежат следующие особенности состава и распределения фермент организме человека:
— Состав ферментов и их тканевое распределение у взрослого человека в основном постоянны, но могут измениться при болезнях.
— Для каждой ткани (органа) характерен свой качественный и количественный состав белков, что определяет функциональные особенности каждой ткани.
— Однако метаболические пути в разных тканей очень похожи, и есть лишь несколько тканеспецифических ферментов (например, кислая фосфатаза предстательной железы и гистидаза печени)
— Более специфичным для тканей является соотношение разных ферментов и изоферментов.
Почти все ферменты организма функционируют внутриклеточно. Исключение составляют пример, ферменты пищеварительного тракта, также ферменты свертывающей системы и ферменты межклеточного матрикса.
При повреждении тканей внутриклеточные ( появляются в сыворотке крови. Обнаружение тканеспецифических ферментов, специфических изоферментов или характерное количественное увеличение активности неспецифических ферментов воротке могут помочь поставить и уточнить диагноз.
Таблица 2. Применение ферментов в медицине.
Источник
Номенклатура ферментов: описание, классификация, строение и принципы построения
Стремительное открытие огромного числа энзимов (на сегодняшний день известно более 3 тысяч) вызвало необходимость их систематизировать, однако долгое время единый подход к этому вопросу отсутствовал. Современная номенклатура и классификация ферментов была разработана комиссией по ферментам международного биохимического союза и одобрена на пятом Всемирном биохимическом конгрессе в 1961 году.
Общая характеристика ферментов
Ферменты (иначе энзимы) — это уникальные биологические катализаторы, обеспечивающие осуществление огромного количества биохимических реакций, протекающих в клетке. Притом последние протекают в миллионы раз быстрее, чем могло происходить без участия энзимов. Каждый фермент имеет активный центр, предназначенный для связывания с субстратом.
Номенклатура и классификация ферментов в биохимии тесно связаны, поскольку название каждого энзима строится на основании его группы, вида субстрата и типа катализируемой химической реакции. Исключение составляет тривиальная номенклатура, которая базируется на исторических названиях и охватывает сравнительно небольшую часть ферментов.
Классификация энзимов
Современная классификация ферментов базируется на характеристике катализируемых химических реакций. На этом основании выделено 6 основных групп (классов) энзимов:
- Оксидоредуктазы осуществляют реакции окислительно-восстановительного характера, ответственны за перенос протонов и электронов. Реакции проходят по схеме А восстановлен + В окислен = А окислен + В восстановлен, где исходные вещества А и В являются субстратами фермента.
- Трасферазы катализируют межмолекулярный перенос химических групп (кроме атома водорода) с одного субстрата на другой (A-X + B = A + BX).
- Гидролазы ответственны за расщепление (гидролиз) внутримолекулярных химических связей, образованных с участием воды.
- Лиазы отщепляют от субстрата химические группы по негидролитическому механизму (без участия воды) с формированием двойных связей.
- Изомеразы осуществляют межизомерные превращения.
- Лигазы катализируют соединение двух молекул, которое сопряжено с разрушением макроэргических связей (например, АТФ).
В свою очередь, каждая из этих групп дополнительно делится на подклассы (от 4 до 13) и подподклассы, более конкретно описывающие разные типы химических превращений, осуществляемых ферментами. Здесь учитываются множество параметров, включая:
- донор и акцептор преобразуемых химических групп;
- химическую природу субстрата;
- участие в каталитической реакции дополнительных молекул.
Каждому классу соответствует закрепленный за ним порядковый номер, который используется в цифровом шифре ферментов.
Оксидоредуктазы
Деление оксидоредуктаз на подклассы происходит по донору окислительно-восстановительной реакции, а на подподклассы — по акцептору. К основным группам данного класса относят:
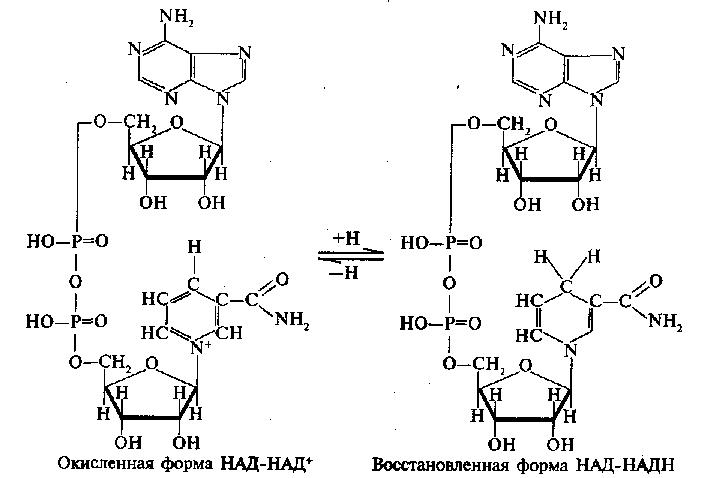
- Дегидрогеназы (иначе редуктазы или анаэробные дегидрогеназы) — наиболее распространенный вид оскидоредуктаз. Эти энзимы ускоряют реакции дегидрирования (отщепления атома водорода). В роли акцептора могут выступать различные соединения (NAD+, FMN и т.д.).
- оксидазы (аэробные дегидрогеназы) — в качестве акцептора выступает кислород;
- оксигеназы (гидроксилазы) — присоединяют один из атомов молекулы кислорода к субстрату.
Коферментом более половины оксидоредуктаз является соединение НАД+.
Трансферазы
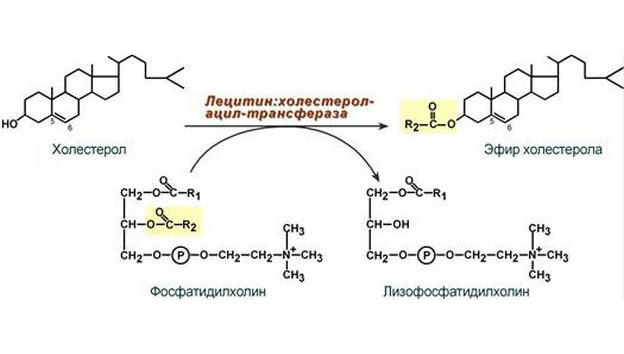
Данный класс насчитывает около пятисот ферментов, которые подразделяют в зависимости от вида переносимых групп. На этом основании выделены такие подклассы, как фосфотрансферазы (перенос остатков фосфорной кислоты), ацилтрансферазы (перенос ацилов), аминотрансферазы (реакции переаминирования), гликозилтрансферазы (перенос гликозильных остатков), метилтрансферазы (транспортирование одноуглеродных остатков) и др.
Гидролазы
Гидролазы делятся на подклассы по характеру субстрата. Наиболее важными из них являются:
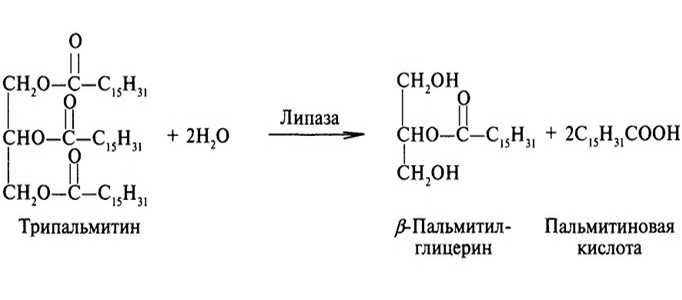
- эстеразы — ответственны за расщепление сложных эфиров;
- гликозидазы — гидролизируют гликозиды (включая углеводы);
- пептид-гидролазы — разрушают пептидные связи;
- ферменты, расщепляющие непептидные C-N-связи
В групппу гидролаз входит около 500 ферментов.
Лиазы
Негидролитическому отщеплению под действием лиаз могут подвергаться многие группы, включая CO2, NH2, H2O, SH2 и др. При этом происходит распад молекул по связям С-О, С-С, C-N и т.д. Одним из важнейших подклассов данной группы являются улерод-углерод-лиазы.
Некоторые реакции отщепления являются обратимыми. В таких случаях при определенных условиях лиазы могут катализировать не только распад, но и синтез.
Лигазы
Все лигазы подразделяются на две группы в зависимости от того, какое соединение дает энергию для образования ковалентной связи. Ферменты, использующие нуклеозидтрифосфаты (АТФ, ГТФ и т.д.), называют синтетазами. Лигазы, действие которых сопряжено с другими макроэргическими соединениями, именуют синтазами.
Изомеразы
Данный класс сравнительно немногочислен и включает около 90 ферментов, которые вызывают геометрические или структурные перестроения в молекуле субстрата. К важнейшим ферментам данной группы относят триозофосфатизомеразу, фосфоглицерат-фосфомутазу, альдозомутаротазу и изопентенил-пирофосфатизомеразу.
Классификационный номер фермента
Введение в биохимию ферментов номенклатуры кодового характера было осуществлено в 1972 году. Согласно этому нововведению каждый энзим получил классификационный шифр.
Индивидуальный номер фермента состоит из 4 цифр, первая из которых обозначает класс, вторая и третья — подкласс и подподкласс. Конечная цифра соответствует порядковому номеру конкретного энзима в подподклассе согласно алфавитному порядку. Числа шифра отделены друг от друга цифрами. В международном списке ферментов классификационный номер указывается в первой колонке таблицы.
Принципы номенклатуры ферментов
В настоящее время существует три подхода к формированию названий ферментов. В соответствии с ними выделяют следующие типы номенклатуры:
- тривиальная (самая старая система);
- рабочая — удобна в употреблении, очень часто используется в учебной литературе;
- систематическая (или научная) — наиболее подробно и точно характеризует механизм действия фермента, но слишком сложна для повседневного употребления.
Систематическая и рабочая номенклатуры ферментов имеют общую черту, которая заключается в присоединении к концу любого названия суффикса «аза». Последний является своего рода «визитной карточкой» энзимов, выделяющей их из ряда других групп биологических соединений.
Существует еще одна система составления наименований, основанная на строении фермента. Номенклатура в таком случае делает акцент не на тип химической реакции, а на пространственную структуру молекулы.
Кроме собственно названия частью номенклатуры энзимов является их индексация, согласно которой каждому энзиму соответствует свой классификационный номер. В базах данных ферментов обычно указываются их шифр, рабочее и научное названия, а также схема химической реакции.
Современные принципы построения номенклатуры ферментов основаны на трех характеристиках:
- особенности осуществляемой энзимом химической реакции;
- класс фермента;
- субстрат, к которому применяется каталитическая активность.
Особенности раскрытия этих пунктов зависят от типа номенклатуры (рабочая или систематическая) и подкласса фермента, к которому они применяются.
Тривиальная номенклатура
Тривиальная номенклатура ферментов появилась в самом начале развития энзимологии. В то время названия энзимам давали первооткрыватели. Поэтому данная номенклатура иначе называется исторической.
В основе тривиальных названий лежат произвольные признаки, связанные с особенностью действия фермента, но в них не содержится сведений о субстрате и типе химических реакций. Такие названия значительно короче рабочих и систематических.
Тривиальные наименования обычно отражают какую-то особенность действия фермента. Например, название энзима «лизоцим» отражает способность данного белка лизировать бактериальные клетки.
Классическими примерами тривиальной номенклатуры являются пепсин, трипсин, ренин, хемотрипсин, тромбин и другие.
Рациональная номенклатура
Рациональная номенклатура ферментов стала первым шагом к разработке единого принципа формирования названий энзимов. Она была разработана в 1898 году Е. Дюкло и базировалась на комбинировании названия субстрата с суффиксом «аза».
Так, фермент, катализирующий гидролиз мочевины, именовался уреазой, расщепляющий жиры — липазой и т. д.
Названия холоферментов (молекулярных комплексов белковой части сложных энзимов с кофактором) строились на основании природы кофермента.
Рабочая номенклатура
Получила такое название за удобство в повседневном использовании, так как содержит основную информацию о механизме действия энзима при сохранении относительной краткости наименований.
Рабочая номенклатура ферментов основана на сочетании химической природы субстрата с типом катализируемой реакции (ДНК-лигаза, лактатдегидрогеназа, фосфоглюкомутаза, аденилатциклаза, РНК-полимераза).
Иногда в качестве рабочих названий используют рациональные наименования (уреаза, нуклеаза) или сокращенные систематические. Например, сложное составное название «пептидил-пролил-цис-транс-изомераза» заменяется на упрощенное «пептидилпролилизомераза» с более коротким и слитным написанием.
Систематическая номенклатура ферментов
Так же как и рабочая, основана на характеристике субстрата и химической реакции, однако данные параметры раскрываются гораздо точнее и подробнее, с указанием таких вещей, как:
- вещество, выступающее в качестве субстрата;
- природа донора и акцептора;
- название подкласса фермента;
- описание сути химической реакции.
Последний пункт подразумевает уточняющую информацию (природа переносимой группы, тип изомеризации и т. д.).
Не для всех энзимов указывается полный набор вышеперечисленных характеристик. Каждому классу ферментов соответствует своя формула составления систематических названий.
| Группа фермента | Форма конструирования наименований | Пример |
| Оксидоредуктазы | Донор: акцептор-оксидоредуктаза | Дактат: НАД + -оксидоредуктаза |
| Трансферазы | Донор: акцептор-транспортируемая группа-трансфераза | Ацетил КоА: холин-О-ацетил-трансфераза |
| Гидролазы | Субстрат-гидролаза | Ацетилхолин-ацил-гидролаза |
| Лиазы | Субстрат-лиаза | L-малат-гидролиаза |
| Изомеразы | Составляется с учетом типа реакции. Например:
Если в ходе реакции осуществляется внутримолекулярный перенос химической группы, фермент называют мутазой. Другими возможными окончаниями наименований могут быть «эстераза» и «эпимераза» (в зависимости от подкласса фермента) |
|
| Лигазы | А: В лигаза (А и В — субстраты) | L-глутамат: аммиак лигаза |
Иногда в систематическом названии фермента содержится уточняющая информация, которую заключают в скобки. Например, энзиму, катализирующему окислительно-восстановительную реакцию L-малат + НАД + = пируват + СО2 + НАДН, соответствует наименование L-малат: НАД + -оксидоредуктаза (декарбоксилирующая).
Источник