- Оксид меди (I)
- Оксид меди (I)
- Способы получения оксида меди (I)
- Химические свойства оксида меди (I)
- Оксид меди (II)
- Оксид меди (II)
- Способы получения оксида меди (II)
- Химические свойства оксида меди (II)
- Формула оксида меди, свойства, риски и использование
- Физико-химические свойства оксида меди
- Реактивность и опасности
- приложений
- Получение меди
- Способы получения меди
- Получение меди электролизом
- Получение оксида меди
- Получение сульфата меди
- Получение хлорида меди
- Получение глицерата меди
- Получение нитрата меди
- Получение сульфида меди
Оксид меди (I)
Оксид меди (I)
Оксид меди (I) Cu2O – твердое кристаллическое вещество коричнево-красного цвета.
Способы получения оксида меди (I)
В лаборатории оксид меди (I) получают восстановлением свежеосажденного гидроксида меди (II), например , альдегидами или глюкозой:
Химические свойства оксида меди (I)
1. Оксид меди (I) обладает основными свойствами.
При действии на оксид меди (I) галогеноводородных кислот получают галогениды меди (I) и воду:
Например , соляная кислота с оксидом меди (I) образует хлорид меди (I):
Cu2O + 2HCl = 2CuCl↓ + H2O
2. При растворении Cu2O в концентрированной серной, азотной кислотах образуются только соли меди (II):
3. Устойчивыми соединениями меди (I) являются нерастворимые соединения (CuCl, Cu2S) или комплексные соединения [Cu(NH3)2] + . Последние получают растворением в концентрированном растворе аммиака оксида меди (I), хлорида меди (I):
Аммиачные растворы солей меди (I) взаимодействуют с ацетиленом :
СH ≡ CH + 2[Cu(NH3)2]Cl → СuC ≡ CCu + 2NH4Cl
4. В окислительно-восстановительных реакциях соединения меди (I) проявляют окислительно-восстановительную двойственность:
Например , при взаимодействии с угарным газом, более активными металлами или водородом оксид меди (II) проявляет свойства окислителя :
Cu2O + CO = 2Cu + CO2
А под действием окислителей, например, кислорода — свойства восстановителя :
Источник
Оксид меди (II)
Оксид меди (II)
Оксид меди (II) CuO – твердое кристаллическое вещество черного цвета.
Способы получения оксида меди (II)
Оксид меди (II) можно получить различными методами :
1. Термическим разложением гидроксида меди (II) при 200°С :
2. В лаборатории оксид меди (II) получают окислением меди при нагревании на воздухе при 400–500°С:
2Cu + O2 → 2CuO
3. В лаборатории оксид меди (II) также получают прокаливанием солей (CuOH)2CO3, Cu(NO3)2:
Химические свойства оксида меди (II)
Оксид меди (II) – основный оксид (при этом у него есть слабо выраженные амфотерные свойства) . При этом он является довольно сильным окислителем.
1. При взаимодействии оксида меди (II) с сильными и растворимыми кислотами образуются соли.
Например , оксид меди (II) взаимодействует с соляной кислотой:
СuO + 2HBr = CuBr2 + H2O
CuO + 2HCl = CuCl2 + H2O
2. Оксид меди (II) вступает в реакцию с кислотными оксидами.
Например , оксид меди (II) взаимодействует с оксидом серы (VI) с образованием сульфата меди (II):
3. Оксид меди (II) не взаимодействует с водой.
4. В окислительно-восстановительных реакциях соединения меди (II) проявляют окислительные свойства:
Например , оксид меди (II) окисляет аммиак :
3CuO + 2NH3 → 3Cu + N2 + 3H2O
Оксид меди (II) можно восстановить углеродом, водородом или угарным газом при нагревании:
СuO + C → Cu + CO
Более активные металлы вытесняют медь из оксида.
Например , алюминий восстанавливает оксид меди (II):
3CuO + 2Al = 3Cu + Al2O3
Источник
Формула оксида меди, свойства, риски и использование
оксид меди, также называется оксидом меди (II), представляет собой химическое соединение формулы CuO. Его структура показана на рисунке 1 (EMBL-EBI, 2017).
Оксид меди встречается в природе как один из компонентов минералов, таких как тенорит и паралаконит. Он добывается из полезных ископаемых по всему миру, в основном в Южной Америке, в таких странах, как Перу, Боливия.
Некоторые химические соединения, такие как карбонат аммония и аммиак, используются для стимулирования добычи полезных ископаемых..
Оксид меди получают в основном путем извлечения в минералах, однако существует определенный процесс его промышленного производства..
В промышленности оксид меди получают реакцией воспламенения тригидрата нитрата меди (100-20 ° C), гидроксида меди (100 ° C) или карбоната меди (250 ° C):
Его также получают синтетическим путем, нагревая металлическую медь на воздухе приблизительно при 800 ° С (формула оксида меди, S.F.).
Физико-химические свойства оксида меди
Оксид меди (II). Представляется в виде тонкого черного порошка с ионной структурой. Его внешний вид показан на рисунке 3.
Молекула образована двухвалентной катионной медью Cu + 2 и анионным кислородом O-2. Молекулы образуют моноклинную кристаллическую систему, где каждый атом меди координируется 4 атомами кислорода..
Он тесно связан с другим оксидом меди: оксидом меди Cu2O (Национальный центр биотехнологической информации, 2005)..
Его молекулярная масса составляет 79,545 г / моль, а плотность — 6,315 г / мл. Его температура плавления составляет 1326 ° C, где он разлагается с выделением кислорода, его температура кипения выше 2000 ° C.
Соединение нерастворим в воде, спирте, гидроксиде аммония, карбонате аммония и растворим в хлориде аммония и цианиде калия (Royal Society of Chemistry, 2015).
Оксид меди является амфотерным, поэтому он может растворяться в кислотах и щелочных растворах. В щелочном растворе реагирует с образованием других солей меди:
В кислотных растворах он также реагирует с образованием других солей меди:
Он взрывается при нагревании в контакте с алюминием, водородом или магнием. Кроме того, при нагревании образуются токсичные пары..
Реактивность и опасности
Оксид меди (II) чрезвычайно ядовит и токсичен при проглатывании. Вызывает повреждение центральной нервной системы и эндокринной системы (AZoM, 2013).
Это также раздражает глаза и кожу. Негорючий, стабильный и несовместимый с восстановителями, сероводородом, алюминием, щелочными металлами, тонкоизмельченными металлами (Fisher scientiffic, 2009).
В случае попадания в глаза, следует проверить, носите ли вы контактные линзы, и немедленно снять их..
Глаза следует промыть проточной водой не менее 15 минут, держа веки открытыми. Вы можете использовать холодную воду. Мазь не следует использовать для глаз.
Если химическое вещество попало на одежду, удалите его как можно быстрее, защищая свои руки и тело. Поместите жертву под безопасный душ.
Если химическое вещество накапливается на незащищенной коже жертвы, например на руках, аккуратно и осторожно промойте кожу, загрязненную проточной водой и неабразивным мылом..
Вы можете использовать холодную воду. Если раздражение не проходит, обратитесь к врачу. Выстирать загрязненную одежду перед повторным использованием.
Если контакт с кожей серьезный, его следует промыть дезинфицирующим мылом и покрыть кожу, загрязненную антибактериальным кремом..
В случае вдыхания пострадавшему должно быть разрешено отдыхать в хорошо проветриваемом помещении. Если вдыхание серьезное, пострадавшего следует как можно скорее эвакуировать в безопасное место..
Ослабьте тесную одежду, такую как воротник рубашки, ремни или галстук. Если пострадавшему трудно дышать, следует назначить кислород.
Если пострадавший не дышит, проводится реанимация из уст в уста. Всегда принимая во внимание, что человеку, оказывающему помощь в проведении реанимации изо рта в рот, может быть опасно, когда вдыхаемый материал токсичен, инфекционен или вызывает коррозию.
В случае проглатывания не вызывать рвоту. Ослабьте тесную одежду, такую как воротники рубашки, ремни или галстуки. Если пострадавший не дышит, проведите реанимацию из уст в уста.
Во всех случаях вам следует немедленно обратиться к врачу (паспорт безопасности материала Оксид меди, 2013 г.).
приложений
Оксид меди используется в качестве пигмента для кристаллов, фарфоровых эмалей и искусственных драгоценных камней. Оксид добавляет к таким материалам голубовато-зеленоватый оттенок.
Он также используется в качестве десульфурирующего агента для нефтяных газов и в качестве катализатора окисления и в гальванических электродах (Encyclopædia Britannica, 2017).
Оксид меди широко используется в химической и сельскохозяйственной химической промышленности для производства промежуточных продуктов в некоторых процессах..
Это широко используемый окислитель / восстановитель и регулятор процесса в химической реакции, особенно в производстве нефти..
Оксид меди используется для производства красок и покрытий, а также является компонентом некоторых продуктов по уходу за воздухом..
Редко используемый в качестве пищевой добавки у животных, он также имеет применение в качестве полупроводника p-типа из-за его узкой запрещенной зоны. Он используется в качестве альтернативы оксида железа в термитах.
Из-за своих фунгицидных и микробицидных свойств оксид меди (II) также находит применение в качестве инсектицида и фумиганта..
Он используется в основном при обработке растений картофеля и в качестве противообрастающего средства в корпусах судов. Средство против обрастания — это материал, предотвращающий образование ракушек и других организмов на дне лодки..
Когда эти организмы растут в корпусе корабля, они увеличивают трение, возникающее при прохождении корабля через воду, тем самым снижая его скорость..
Смесь также используется в качестве консерванта для древесины, для защиты столбов забора, стружки, настила, кровли, черепицы, морских стен и других пресноводных и морских сооружений от насекомых и грибков. (Томсон Гейл, 2006).
Источник
Получение меди
Медь или купрум, названа так в честь острова Кипр, где нашли крупное ее месторождение. Это один из первых металлов, освоенных человеком. Медный век – удивительная эпоха, в которую обиход человека был наполнен медными орудиями и предметами быта, он продолжался с IV до III тысячелетия до н. э.
Способы получения меди
Для извлечения меди из минералов и руд, в которых она находится, на сегодняшний день используют три метода:
- гидрометаллургический
- пирометаллургичекий
- электролиз.
Получение меди пирометаллургическим методом является наиболее распространенным. Сырьем для этого процесса выступает халькопирит. Чтобы получить из халькопирита чистую медь, необходимо осуществить ряд операций. Первая, из которых, заключается в обогащении медной руды, методом окислительного обжига или флотации.
В основе флотации лежит тот факт, что пустая порода и ее медесодержащие части, смачиваются по-разному. Если поместить всю массу породы в емкость с жидким составом, в котором имеются воздушные пузырьки, то часть с минеральными элементами, перемещается при помощи этих пузырьков на поверхность, и прилипает к ним. В результате на поверхности ванны наблюдается наличие концентрата или черновой меди. В этом составе присутствует от 10 до 35% чистой меди. Этот порошкообразный концентрат является сырьем для дальнейшего получения чистой меди.
Совсем по-другому протекают реакции получения меди методом окислительного обжига. Этим методом обогащают медные руды, в составе которых имеется существенное количество серы. Для реализации этой технологии необходимо нагреть руду до температуры 700–8000 градусов. Под действием таких высоких температур происходит окисление сульфидов, и объем серы в медной руде снижается почти в два раза. Следующим этапом является расплавление обогащенной руды в отражательных или шахтных печах при температуре 14500. Результатом этого расплава является образование штейна – сплава, который состоит из сульфидов меди и железа.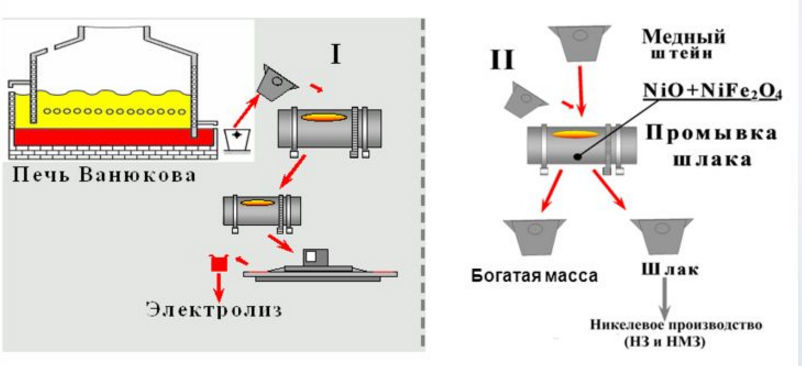
Черновая медь, полученная таким способом, имеет в своем составе около 91% меди. Для дополнительной очистки металла выполняется рафинирование меди, то есть удаление посторонних примесей. Это осуществляется благодаря технологии огневого рафинирования в присутствии подкисленного раствора медного купороса. Это рафинирование меди носит электролитический характер, и дает возможность получить металл с чистотой 99,9%.
Гидрометаллургический метод обогащения меди основан на процессе выщелачивания металла с помощью серной кислоты. Результатом такого процесса является получение раствора, из которого в дальнейшем выделяют чистую медь. Также этот метод подходит для выделения драгоценных металлов. Эту технологию применяют для обогащения руд, в которых присутствует крайне малое количество меди.
Получение меди электролизом
Электролиз меди является одним этапов химико-физических процессов, которому подвергают руду, чтобы получить медь. Примечательно, что для получения 1 тонны чистой меди, потребуется переработать как минимум 200 тонн медной руды.
Сама процедура обработки медной руды – это многоступенчатый и очень сложный процесс, который состоит из 7 стадий. Самой последней и является электролиз меди.
Руду после добычи необходимо измельчить в особых машинах. Далее происходит процесс флотации, в результате которого, как мы знаем, формируется концентрат с сохранением минералов меди. После этого происходит обжиг при высоких температурах в специальных печах. Шихту, полученную в процессе обжига, помещают в печь для плавки, где она становится штейном, который в свою очередь оправляют на конвертирование. Продукт, полученный после этих процессов, называют черновой медью, где 2-3% объема занимают примеси. В качестве примесей выступают цинк, железо, или сера. Их удаляют реакцией окисления. На этом этапе образуется «красная» медь, в которой присутствует 99,7-99,9% Cu. Последним этапом является непосредственно электролиз меди, который позволяет добиться получения максимально чистой меди.
Чтобы осуществить процесс электролиза меди понадобится специальное оборудование, а именно емкости, которые заполняют водным раствором сульфата меди с содержанием свободной серной кислоты. В результате проведения электролиза, мы получим осадок чистой меди на катодах. А все, что окажется на дне ванны, принято называть шламом. Он является сырьем для получения благородных металлов.
Получение оксида меди
Оксид меди (II) CuO представляет собой кристаллы черного цвета, которые подвергаются кристаллизации в моноклинной сингонии. Плотность соединения составляет 6,51 г/см3, а плавится он при температуре 1447°С в условиях высокого давления. В результате нагревания до 1100°С является выделение оксида меди (I):
В воде оксид меди не растворяется и не вступает в реакции с ней. Обладает слабыми амфотерными свойствами с преобладанием основных.
С водными растворами аммиака реагирует с образованием гидроксида тетраамминмеди (II):
Также легко вступает в реакции с разбавленными кислотами с выделением соли и воды:
Результатом сплавления оксида меди со щелочами является образование купратов:
Чистую медь из оксида можно получить методом восстановления водородом, угарным газом и активными металлами:
Реакция получения оксида меди методом прокаливания гидроксида меди (II) при температуре 200°С:
Также получить оксид меди можно в процессе окисления металлической меди на воздухе при температуре 400–500°С:
Получение сульфата меди
Получить сульфат меди можно тремя реакциями:
растворить CuO в H2SO4
в присутствии концентрированной серной кислоты с медью, обязательно при нагревании
методом взаимодействия Cu2O с разбавленной серной кислотой
Получение хлорида меди
В природе хлорид меди находится в составе очень редкого минерала эрнохальцита CuCl₂•2H₂O, который представляет собой кристаллы синего цвета.
Двухвалентный хлорид меди обладает важным практическим значением, и добычи его только лишь из природного минерала очень мало. Поэтому ученые придумали несколько способов искусственного получения данного соединения.
Главной реакцией промышленного синтеза CuCl₂ можно назвать реакцию хлорирования сульфида меди в условиях высокой температуры от 300 до 400 градусов °С. Выглядит реакция так
Еще одним вариантом синтеза хлорида двухвалентной меди является хлорирующий обжиг, который осуществляется при температуре более 500 С:
- CuS + 2NaCl + 2O₂ ―› CuCl₂ + Na₂SO₄
Обе реакции нуждаются в использовании специализированного оборудования и соблюдении повышенных мер безопасности, по этой причине данные реакции можно проводить только в условиях промышленного производства. В лабораторных условиях также можно получить хлорид меди следующими реакциями
- Cu + Cl₂ ―› CuCl₂
- CuO + 2HCl ―› CuCl₂ +H₂O
- Cu(OH)₂ + 2HCl ―› CuCl₂ + 2H₂O. Реакция нейтрализации
- CuCO₃ + 2HCL ―› CuCl₂ + H₂O + CO₂. В результате этой реакции более сильная кислота вытеснит кислотный остаток более слабой кислоты. Протекает реакция замещения
- 3Сu + 2HNO₃ + 6HCl ―› 3CuCl₂ + 2NO +4H₂0. Эта реакция является наиболее оригинальной. Она протекает только в присутствии смеси двух сильных кислот.
Получение глицерата меди
Качественная реакция для выявления присутствия глицерина в растворах осуществляется в присутствии сульфата меди (II) и раствора гидроксида натрия. В результате реакции образуется глицерат меди – комплексное соединение сине-василькового оттенка.
Химическую реакцию проводят следующим образом:
- к раствору сульфата меди (II) приливают раствор гидроксида натрия, в результате чего происходит окрашивание раствора в синий цвет. Таким образом, наблюдаем выпадения осадка гидроксида меди (II)
- после этого добавляем несколько мл глицерина и перемешиваем раствор. Образовавшийся осадок растворяется с образованием комплексного соединения оттенка индиго. Это и есть глицерат меди.
Получение нитрата меди
Получение нитрата меди Cu(NO3)2 довольно увлекательное занятие. А также очень полезное, поскольку он является довольно популярным красителем. Нитрат меди (II) можно получить в процессе растворения чистой меди, ее оксида или гидроксида в азотной кислоте. Уравнения выглядят следующим образом:
Получение сульфида меди
Сульфид меди(II) или моносульфид меди — CuS, является неорганическим бинарным соединением двухвалентной меди с серой. Он верного цвета, в воде не растворяется , также как и в разбавленных растворах кисло. В природе его можно встретить в виде редкого минерала ковеллина.
Получение сульфида меди осуществляется при помощи прямого взаимодействия элементов, а также в результате обменной реакции солей двухвалентной меди с водорастворимыми сульфидами.
- Na2S+CuSO4=CuS+Na2SO4
- CuCl2 + H2S —> CuS + 2HCl
- 2CuS + H2 —>Cu2S + H2S. Эта реакция протекает в условиях высокой температуры от 600 до 700 oC
Получение сухим методом дает сульфиду меди возможность проводить электрический ток. Когда отметка термометра достигает 400 °C, наблюдается заметное разложение сульфида.
Источник