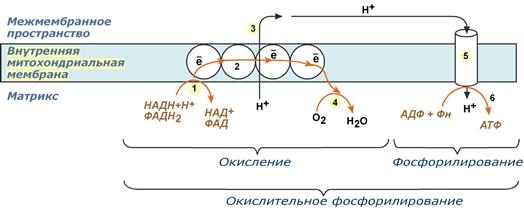
Синтез АТФ путем окислительного фосфорилирования
Окислительное фосфорилирование — это основной путь синтеза АТФ, за счет энергии окисления субстрата кислородом. Процесс окислительного фосфорилирования осуществляется вмитохондриях. Митохондрии справедливо называют «энергетическими станциями»клеток, так как они улавливают энергию внешних ресурсов и трансформируют ее в другие формы энергии. Условно можно разделить процесс окислительного фосфорилирования на 4 этапа.
1. Окисление энергетических субстратов в матриксе митохондрий.
2. Окисление НАДН и ФАДН2 в митохондриальной дыхательной цепи.
З. Генерирование протонного потенциала ΔμH + за счет энергии окисления энергетических субстратов.
4. Синтез АТФ за счет энергии протонного потенциала.
Окисление энергетических субстратов
В реакции дегидрирования при действии НАД + — и ФАД — зависимыхдегидрогеназ (ДГ)от энергетических субстратов отщепляются два атома водорода. Ферменты локализованы в матриксе митохондрий, за исключением ФАД-зависимой сукцинатдегидрогеназы, которая локализована на поверхности внутренней мембраны митохондрий.
Пиридинзависимые дегидрогеназы










α-KT АН2 А Сукцинил-S-КоА

β-гидроксиацил-КоА НАД + НАДН+Н + β-кетоацил-КоА
Флавинзависимые дегидрогеназы





В восстановленных коферментах 2ē находятся на более высоком энергетическом уровне, это высокоэргические электроны.
НАДН+Н + ↔ 2Н ↔ 2Н + + 2ē
Таким образом, химическая энергия субстратов (АН2) трансформировалась в энергию электронов атомов водорода (электрическую энергию).
Кофакторы дегидрогеназ (НАДН + Н + — и ФАДН2 –зависимых) являются переносчиками двух атомов водорода на другую ферментативную систему, а именно – на систему дыхательной цепи.
2.Окисление НАДН+Н + и ФАДН2 в митохондриальной дыхательной цепи (ЦПЭ).
Окисление НАДН+Н + и ФАДН2 осуществляется при участии окислительно-восстановительных ферментов митохондрий по реакции
НАДН+Н + + 1 /2 O2→НАД + + H2O
Изменение свободной энергии этого процесса составляет: ΔG° = -220 кДж/моль
( ΔG° = — 52,6 ккал/моль).
Сущность окисления заключается в последовательной передаче электронов от НАДН+Н + и ФАДН2 на кислород при помощи специальных переносчиков в электронтранспортной цепи.
Переносчики электронов в электронтранспортной цепи
Окислительно-восстановительные переносчики локализованы на поверхности или встроены во внутренней мембране митохондрий. Мерой сродства окислительно- восстановительной пары к электронам служит окислительно-восстановительный потенциал Е о , величина которого определяет направленность переноса электронов.
Типы переносчиков
ФМН-содержащий переносчик электронов. По структуре ФМН представляет моно-нуклеотид, у которого в качестве азотистого основания служит изоаллоксазин, соединенный через рибозу с остатком фосфорной кислоты. При восстановлении он приобретает не только электроны, но и протоны. Е о = +0,12
ФМН + 2Н + + 2ē ↔ ФМНН2
Железо-серные центры
Это белковые негемовые железосодержащие переносчики электронов. Имеются несколько типов железо-серных центров: Fe-S,Fe2-S2, Fe4-S4. Атомы железа комплексов могут отдавать и принимать электроны, поочередно переходя в ферро-(Fe 2+ ) — и ферри-(Fe 3+ ) — состояния. Все железо-серные центры отдают электроны убихинону.
Fe 3+ -S + 2ē ↔ Fe 2+ -S
Убихинон, кофермент-Q(KoQ) – единственный небелковый переносчик электронов.
КоQ (хинон) КоQ (семихинон) КоQН2 (гидрохинон)
Убихинон при восстановлении приобретает не только электроны, но и протоны. При одноэлектронном восстановлении он превращается в семихинон – органический свободный радикал. Е о =+0,01
Цитохромы– белковые переносчики электронов, в качестве простетической группы, содержащие гемовое железо. В основе функционирования цитохромов лежит изменение степени окисления атома железа Fe 3+ +ē ↔ Fe 2+ . Различные цитохромы обозначаются буквенными индексами: b, с1, с, a, a3. Отличаются цитохромы по структуре белковой части и боковых цепей гема, в связи с этим они имеют и различные величины редокс-потенциалов (окислительно-восстановительных потенциалов). Цитохром «b» Е о = +0,08 , «ci» Е о =+0,22, «с» Е о = +0,25,«ааз» Е о = +0,29.Отличительной особенностью цитохрома сявляется то,что он непрочно связан с внешней поверхностью внутренней мембраны митохондрий и легко покидает её.
Все эти переносчики электронов можно сгруппировать в четыре ферментативных комплекса, структурированные во внутренней мембране митохондрий, представляющие собой ферментативный ансамбль,получивший название «дыхательные ферменты»,«цитохромная система», «ЦПЭ»(цепь переноса электронов).
Комплекс I – НАДН-дегидрогеназа (НАДН-КоQ-редуктаза). Простетические группы -ФМН, FeS. Акцептор электронов – KoQ .
Комплекс III – КоQН2-дегидрогеназа (KoQH2-цит.с-редуктаза).Простетические группы: FeS, цитохромы b1, b2, с1. Акцептор электронов – цитохром — с .
Комплекс IV – цитохромокcидаза.Простетические группы: цитохромы ааз, Си 2+ . Акцептор электронов– кислород.
Комплекс II – сукцинатдегидрогеназа (Сукцинат-КоQ-редуктаза).Простетические группы ФАД, FeS. Акцептор электронов – KoQ .
Между комплексами электроны транспортируются при помощи подвижных переносчиков — убихинона и цитохрома-с.
Окислительно-восстановительные переносчики в ЦПЭ расположены в порядке увеличения стандартных окислительных потенциалов, что обеспечивает самопроизвольный транспорт двух электронов по дыхательной цепи от НАДН+Н + к кислороду — конечному акцептору электронов. Перенос двух электронов по ЦПЭ является полезной работой и сопровождается поэтапным высвобождением свободной энергии Гиббса (ΔG), которая далее используется в синтезе АТФ.Поэтапное высвобождение энергии приводит к тому, что электроны, которые восстанавливают кислород, находятся на более низком энергетическом уровне, по сравнению с электронами, находящимися в восстановленном НАДН +Н + в начале цепи.
З. Генерирование протонного потенциала ΔμН +
Каким же образом осуществляется сопряжение транспорта электронов по дыхательной цепи с трансформацией высвободившейся электрической энергии в энергию химических связей АТФ? На этот вопрос в 1961 году дал ответ английский ученый Питер Митчелл. Его концепция заключалась в том, что движущей силой синтеза АТФ является электрохимический потенциал, протонный потенциал – ΔμH + . ΔμH + . = Δ рН+ Δ φ
рН — градиент протонов, Δφ – разность электрического потенциала. В 1978 году
П. Митчеллу была присуждена Нобелевская премия и хемиосмотическая теория стала общепризнанной.
По теории П. Митчелла высвобождающаяся поэтапно энергия в процессе транспорта электронов по дыхательной цепи используется для выкачивания протонов из матрикса митохондрий в межмембранное пространство. Транспорт 2Н + из матрикса митохондрий в межмембранное пространство создает градиент концентрации протонов — ΔрН и приводит к возникновению отрицательного заряда на поверхности мембраны со стороны матрикса и положительного заряда со стороны межмембранного пространства, при этом создается разность электрических потенциалов – Δφ. Источником протонов в матриксе митохондрий является НАДН + Н + , ФАДН2, вода. Возможность генерирования протонного потенциала обеспечивается:
1) непроницаемостью внутренней мембраны митохондрий для ионов вообще и, особенно, для протонов.
2) раздельным транспортом протонов и электронов по дыхательной цепи. Это обеспечивается наличием переносчиков 2-х типов: только для электронов и электронов и протонов одновременно.
4. Синтез АТФ за счет протонного потенциала
Ферментативная система Н + — АТФ- синтазный комплекс, АТФ-синтаза, АТФ-азакатализирует реакцию фосфорилирования АДФ неорганическимфосфатом за счет энергии которая аккумулирована в электрохимическом потенциале.
Протонная АТФ-синтаза состоит из 2-х субкомплексов: F1 иFo. F1 — субъединица представлена 5 видами полипептидных цепей и отвечает за синтез и гидролиз АТФ. Имеет форму шляпки гриба, выступающего в матрикс митохондрий и связана с мембранной белковой субъединицей Fо. Fo — это гидрофобный сегмент из 4-х полипептидных цепей, который пронизывают всю мембрану митохондрий и образует протонный каналв ферментативном комплексе. Через протонные каналы АТФ-синтазы происходит, возвращение протонов обратно вматрикс митохондрий. Существует предположение,что прохождение протонов сопровождается конформационными изменениями активных центров АТФ-синтазы, что и стимулирует синтез АТФ.
В соответствии с механизмом сопряжения окислительного фосфорилирования, предложенным Митчеллом, перенос двух протонов через, протонный канал АТФ-синтазы сопровождается синтезом одной молекулы АТФ.
Реакции окисления,катализируемые пиридинзависимыми дегидрогеназами, сопряжены с I-м комплексом ЦПЭ,поэтому высвобождающаяся поэтапно энергия обеспечивает транслокацию в межмембранное пространство трех пар протонови следовательно, синтез 3-х молекул АТФ.
Реакции окисления, катализируемые флавинзависимыми дегидрогеназами, сопряжены с III-м комплексом ЦПЭ и в межмембранное пространство переносятся лишь две пары протонов,следовательно, синтезируется 2 АТФ.
Реакция окисления аскорбиновой кислотысопряжена на уровне семихинона,поэтому осуществляется транслокация только одной пары протонов и синтезируется лишь 1 молекула АТФ.
Рис.6-2. Схема «Дыхательной цепи»
Папиллярные узоры пальцев рук — маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.
Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.
Источник
Для чего образуются восстановленные НАД и ФАД?
Молекулы НАДН и ФАДН2, образуемые в реакциях окисления углеводов, жирных кислот, спиртов и аминокислот, далее поступают в митохондрии, где ферментами дыхательной цепи осуществляется процесс окислительного фосфорилирования.
Окислительное фосфорилирование
Окислительное фосфорилирование – это многоэтапный процесс, происходящий во внутренней мембране митохондрий и заключающийся в окислении восстановленных эквивалентов (НАДН и ФАДН2) ферментами дыхательной цепи и сопровождающийся синтезом АТФ.
Впервые механизм окислительного фосфорилирования был предложен Питером Митчеллом. Согласно этой гипотезе перенос электронов, происходящий во внутренней митохондриальной мембране, вызывает выкачивание ионов Н + из матрикса митохондрий в межмембранное пространство. Это создает градиент концентрации ионов Н + между цитозолем и замкнутым внутримитохондриальным пространством. Ионы водорода способны возвращаться в матрикс митохондрий через специальный фермент, образующий АТФ – АТФ-синтазу.
Принцип работы дыхательной цепи
В целом работа дыхательной цепи заключается в следующем:
- Образующиеся в реакциях катаболизма НАДН и ФАДН2 передают атомы водорода (т.е. протоны водорода и электроны) на ферменты дыхательной цепи.
- Электроны движутся по ферментам дыхательной цепи и теряют энергию.
- Эта энергия используется на выкачивание протонов Н + из матрикса в межмембранное пространство.
- В конце дыхательной цепи электроны попадают на кислород и восстанавливают его до воды.
- Протоны Н + стремятся обратно в матрикс и проходят через АТФ-синтазу.
- При этом они теряют энергию, которая используется для синтеза АТФ.
Источник