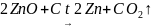- Общие способы получения металлов
- Пирометаллургия
- Гидрометаллургия
- Электрометаллургия
- Практическое значение электролиза.
- 2. Общие способы получения металлов. Практическое значение электролиза (на примере электролиза солей бескислородных кислот).
- Общие способы получения металлов практическое значения электролиза
Общие способы получения металлов
Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д. В свободном виде встречаются металлы, расположенные в ряду напряжений правее водорода (Аg, Нg, Рt,Аu, Сu), хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений.
Минералы и черные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами.
Получение металлов из руд — задача металлургии.
Металлургия — это и наука о промышленных способах получения металлов из руд, и отрасль промышленности.
Любой металлургический процесс — это процесс восстановления ионов металла с помощью различных восстановителей. Суть его можно выразить так:
Чтобы реализовать этот процесс, надо учесть активность металла, подобрать восстановитель, рассмотреть технологическую целесообразность, экономические и экологические факторы.
В соответствии с этим существуют следующие способы получения металлов:
Пирометаллургия
Пирометаллургия — восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, металлов — алюминия, магния.
Например, олово восстанавливают из касситерита SnО2, а медь — из куприта Cu2O
прокаливанием с углем (коксом):
SnО2+ 2С = Sn + 2СО ↑; Cu2O + С = 2Cu+ СО ↑
Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем:
2ZnS + 302 = 2ZnО + 2SO2 ↑; ZnО + С = Zn + СО ↑
сфалерит (цинковая обманка)
Из карбонатных руд металлы выделяют также путем прокаливания с углем, т. к. карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем:
FeСO3 = FеО + СO2 ↑ ; FеО + С = Fе + СО ↑
сидерит (шпатовый железняк)
Восстановлением углем можно получить Fе, Сu, Zn, Сd, Ge, Sn, Рb и другие металлы, не образующие прочных карбидов (соединений с углеродом).
В качестве восстановителя можно применять водород или активные металлы:
К достоинствам этого метода относится получение очень чистого металла.
2) TiO2+ 2Мg = Тi + 2МgO (магнийтермия)
Чаще всего в металлотермии используют алюминий, теплота образования оксида
которого очень велика (2А1 + 1,5 O2 = Аl2O3 + 1676 кДж/моль). Электрохимический ряд напряжений металлов нельзя использовать для определения возможности протекания реакций восстановления металлов из их оксидов. Приближенно установить возможность этого процесса можно на основании расчета теплового эффекта реакции (Q), зная значения теплот образования оксидов:
где Q1— теплота образования продукта, Q2 -теплота образования исходного вещества.
Доменный процесс (производство чугуна):
C + O2 = CO2, CO2 + C ↔ 2CO
3Fe2O3 + CO = 2(Fe 2 Fe 3 2)O4+ CO2
(Fe 2 Fe 3 2)O4+ CO= 3FeO + CO2
FeO + CO= Fe + CO2
(чугун содержит до 6,67% углерода в виде зерен графита и цементита Fe3C);

Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева. Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов. При этом оксиды либо улавливаются в виде отходящих газов (CO2, SO2), либо связываются в легко отделяемый шлак – смесь Ca3(PO4)2 и CaSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Гидрометаллургия
Гидрометаллургия — это восстановление металлов из их солей в растворе.
Процесс проходит в два этапа: 1) природное соединение растворяют в подходящем реагенте для получения раствора соли этого металла; 2) из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом. Например, чтобы получить медь из руды, содержащей оксид меди СuО, ее обрабатывают разбавленной серной кислотой:
Затем медь либо извлекают из раствора соли электролизом, либо вытесняют из сульфата железом:
Таким образом, получают серебро, цинк, молибден, золото, уран.
Электрометаллургия
Электрометаллургия — восстановление металлов в процессе электролиза растворов или расплавов их соединений.
Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы. При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов.
Примеры: 
Источник
Практическое значение электролиза.
Электролиз применяется для решения следующих технических задач: извлечение металлов, очистка металлов, нанесение гальванических покрытий.
Извлечение металлов 1-й и 2-й групп периодической системы осуществляется с помощью электролиза из расплавленных галогенидов этих металлов. Например, натрий получают электролизом расплава хлорида натрия. Сведения о металлах, получаемые таким способом приведены в таблице 1.
Электролитическое получение металлов
| Металл | Сырьё | Электролит |
| Алюминий | Бокситная руда | Al2O3, растворенный в расплавленном криолите |
| Натрий | Каменная соль | NaCl |
| Магний | Доломит и морская вода | MgCl2 |
| Цинк | ZnS – руда (цинковая обманка) | ZnSO4 |
Очистка металлов с помощью электролиза называется рафинирование. Рассмотрим данный процесс на примере меди. Для очистки меди используют два электрода, опущенных в раствор CuSO4. На аноде находится неочищенная медь, на катоде – чистая медь. При электролизе на аноде протекает реакция
Cu(тв.) → Сu 2+ (водн.) + 2е — (16).
Примеси, высвобождаемые при электрохимическом растворении неочищенной меди на аноде, опускаются на дно электролизёра, образуя анодный ил. Переходящие в раствор ионы меди разряжаются на чистом медном катоде
Cu 2+ (водн.) → Cu (тв) + 2е — (17).
Нанесение гальванических покрытий осуществляется на катоде, за счёт так называемого электроосаждения. Катод погружают в электролит, который содержит ионы электроосаждаемого металла. В качестве анода используется пластина, либо стержень из того металла, которым наносят покрытие (например, хром, никель).
Для нанесения покрытий также применяют анодирование. Анодирование – процесс покрытия алюминиевых предметов оксидом алюминия. В данном процессе покрываемый предмет является анодом, а в качестве электролита используется разбавленная серная кислота H2SO4.
Дата добавления: 2015-08-08 ; просмотров: 7259 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Источник
2. Общие способы получения металлов. Практическое значение электролиза (на примере электролиза солей бескислородных кислот).
Металлы широко применяются в современной технике, авиа-, авто-, судостроении и других отраслях хозяйства. Однако далеко не все металлы встречаются в природе в свободном состоянии. Самым распространенным металлом в земной коре является алюминий. В свободном состоянии в природе встречаются наименее активные металлы: золото, платина, серебро, медь, ртуть, олово. Большинство остальных металлов, в том числе и перечисленные, встречаются и в виде различных соединений. Природные минералы и горные породы, содержащие металлы и пригодные для их промышленного получения, называются рудами. По составу большинство руд представляют собой оксиды (Fe2O3 – красный железняк; Al2O3 – корунд и др.) или соли (FeS2 пирит; CaSO4*2H2O – гипс, Na3AlF6 – криолит и др.).
Получение металлов из руд – основная задача металлоргии.
Основной принцип получения металлов из природных соединений – их востановление из руд: Me n + +ne — — Me 0 .
Востановление металлов происходит разными способами.
1) Для восстановления металлов из их оксидов используют:
б) оксид углерода (II)
г) металлы. Востановление металов из их соединений другими металлыми называют металлотермией. В качестве востановителей используют алюминий, магний, кальций, натрий.
2) Металлы можно получить из раствора солей, образующихся при обработке руд, содержащих оксиды металлов. Из раствора соли металла или с помошью электрического тока. Таким образом получают более 25% добываемой меди, а также золото, серебро, цинк и другие металлы.
Например, руды, содержащие оксид меди (II), обрабатывают раствором кислоты и получают растворимую соль – сульфат меди (II):
Затем из раствора выделяют свободную медь вытеснением железными опилками или электролизом:
3) Для получения главным оразом легких металлов (Na, Kи других щелочных металлов, Al, Mg и т.д.) широко используют электролиз.
Электролизом называют окислительно-востановительныую реакцию, протекающую при прохождении электрического тока через раствор или расплав электролита. При этом отрицательный электрод – катод выступает в качестве востановителя, он забирает электроны. Положительный электрод – анод, наоборот, представляет собой окислитель, он забирает электроны. Так, если в расплав хлорида натрия поместить электроды и пропустить электрический ток, то на катоде выделиться натрий, а на аиоде – хлор.
Суммарный процесс электролиза может быть выражен схемой:
Таким образом, при электролизе расплава хлориида натрия одновременно получают натрий и газообразный хлор.
Чтобы показатьпродукты электролиза, можно провести еще один пример электролиза расплава солей, хлорида калия или бромида натрия:
на катоде: 
на аноде: 
суммарное уравнение электролиза:
Практическое значение электролиза очень большое. Так, электролизом раствора хлорида натрия в промышленности получают хлор и гидроксид натрия. Электролизом получают алюминий и все щелочные металлы. С его помощью очищают медь, никель и другие металлы (рафинирование). В этом случае используют анод, изготовленный из соответствующего металла. В процессе электролиза анод растворяется, а на катоде оседает более чистый металл.
Источник
Общие способы получения металлов практическое значения электролиза
Природные соединения металлов:
сильвинит КСl ∙ NaCl, каменная соль NaCl;
серный колчедан FeS2, киноварь HgS, цинковая обманка ZnS;
мел, мрамор, известняк СаСО3, магнезит MgCO3,
доломит CaCO3 ∙ MgCO3;
глауберова соль Na2SO4 ∙ 10 H2O, гипс CaSO4 ∙ 2Н2О;
магнитный железняк Fe3O4, красный железняк Fe2O3, бурый железняк Fe2O3 ∙ Н2О.
чилийская селитра NaNO3;
Минералы и горные породы, содержащие металлы и их соединения и пригодные для промышленного получения металлов, называются рудами.
Отрасль промышленности, которая занимается получением металлов из руд, называется металлургией.
Способы получения металлов из руд.
1. Электрометаллургический способ — это способы получения металлов с помощью электрического тока (электролиза). Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы.
При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов:
катод Na+ + e à Na0 ¦ 2
анод 2Cl — — 2e à Cl20 ¦ 1
суммарное уравнение: 2NaCl (распл.) – (э. ток)à 2Na + Cl2
Современный способ получения алюминия был изобретен в 1886 году. Он заключается в электролизе раствора оксида алюминия в расплавленном криолите. Расплавленный криолит растворяет Al2O3, как вода растворяет сахар.
катод Al3+ +3e à Al 0 ¦ 4
анод 4AlO33– –12 e à 2Al2O3 +3O2 ¦ 1
суммарное уравнение: 2Al2O3(распл.) – (э. ток)à 4Al + 3O2 .
2. Пирометаллургический способ — это восстановление металлов из их руд при высоких температурах с помощью восстановителей: неметаллических : кокс, оксид углерода (II), водород; металлических: алюминий, магний, кальций.
Fe+32O3 +2Al = 2Fe0 + Al2O3
Получают железо, хром.
Восстановление оксидов металлов водородом (водородотермия ):
Cu +2O + H2 –(t)à Cu0 + H2O
Получают малоактивные металлы – медь, вольфрам.
В вертикальной печи кокс окисляется до СО, затем происходит постепенное восстановление железа из руды:
3Fe2O3 + CO –(t)à 2Fe3O4 + CO2 ,
Fe3O4 + 4CO –(t)à 3FeО + 4CO2
FeO + CO –(t)à Fe+ CO2
Восстановление углём (коксом):
ZnO + C –(t)à Zn + CO
Получают цинк, никель.
3. Гидрометаллургический способ основан на растворении природного соединения с целью получения раствора соли этого металла и вытеснением данного металла более активным. Например, руда содержит оксид меди и ее растворяют в серной кислоте: CuO + H2SO4 = CuSO4 + H2O, затем проводят реакцию замещения:
CuSO4 + Fe = FeSO4 + Cu.
Таким способом получают серебро, цинк, молибден, золото, ванадий.
Если для восстановления требуется оксид металла, то в процессе переработки сначала получают оксид:
а) из сульфида – обжигом в кислороде: 2ZnS + 3O2 = 2ZnO + 2SO2
б) из карбоната – разложением: СаСО3 –(t)à СаО + СО2
Производство железа основано на карботермическом восстановлении оксидных металлсодержащих руд.
1) Сульфидные и другие руды вначале подвергают окислительному обжигу : 4FeS2 + 11O2 = 2Fe2O3 + 8SO2.
2)Восстановление оксидных руд осуществляется в доменных печах, при этом протекают следующие реакции:
3Fe2O3 + CO –(t)àCO2 + 2Fe3O4, Fe3O4 + CO–(t)àCO2 + 3FeO, FeO + CO–(t)àCO2 + Feили FeO + C –(t)àCO + Fe.
Полученное железо насыщено углеродом. 3)Затем происходит «выжигание» углерода в сталеплавильных или конверторных печах с образованием стали.
Источник