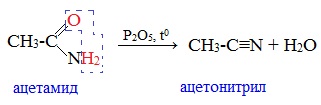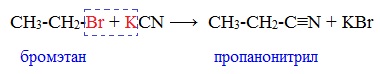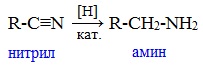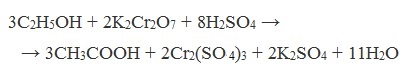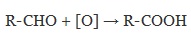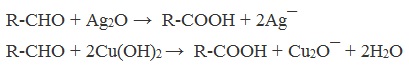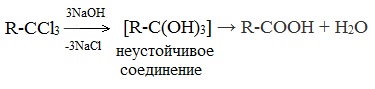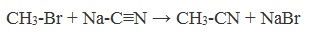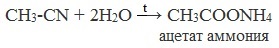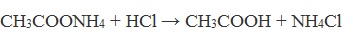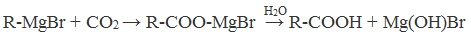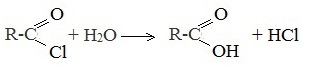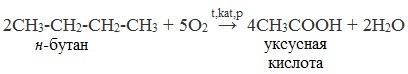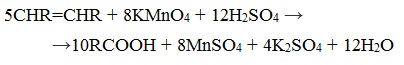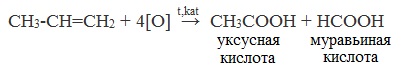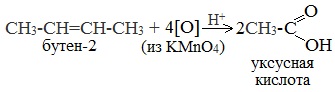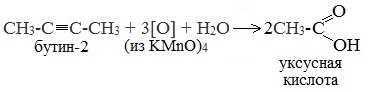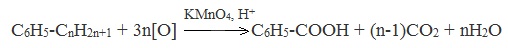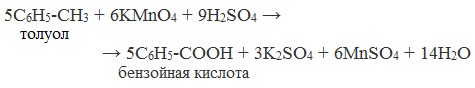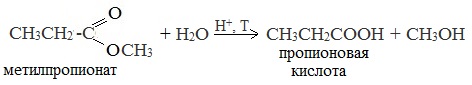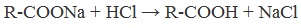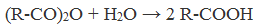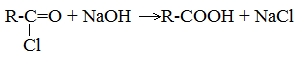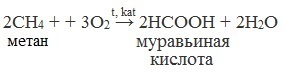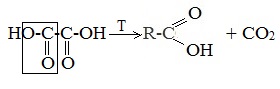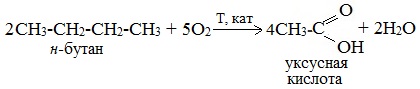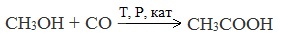- Нитрильный способ получения карбоновых кислот
- Номенклатура
- Способы получения
- Характеристика реакционной способности
- Химические свойства
- Отдельные представители
- Нитрильный способ получения карбоновых кислот
- Общие способы получения карбоновых кислот
- В промышленности
- В лаборатории
- Специфические способы получения важнейших кислот
Нитрильный способ получения карбоновых кислот
Нитрилами называют органические соединения, содержащие одну или несколько цианогрупп -С≡N, связанных с углеводородным радикалом.
От других функциональных производных карбоновых кислот нитрилы отличаются отсутствием карбонильной группы.
Общая формула нитрилов — R-С≡N
Номенклатура
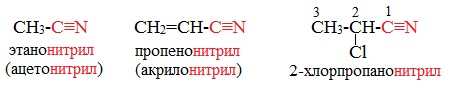
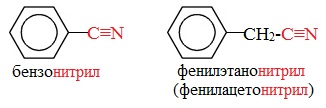
Ациклические соединения R-CN называют по названию углеводорода с соответствующим количеством углеродных атомов, включая углеродный атом группы -С≡N, к которому добавляют суффикс – нитрил . А также от названий ацильных остатков карбоновых кислот, к которым добавляется суффикс — нитрил :
Названия нитрилов также можно образовывать из названий карбоновых кислот заменой окончания – карбоновая кислота на – карбонитрил :
Способы получения
1. Дегидратация амидов
Нитрилы получают дегидратацией амидов при нагревании с сильными водоотнимающими средствами — оксидом фосфора (V) P2O5 или трихлороксидом фосфора POCl3:
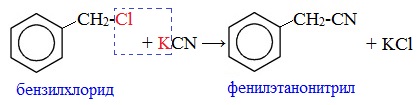
2. Взаимодействие галогеналканов с цианидами щелочных металлов
Нитрилы можно получить при взаимодействии галогеналканов с солями циановодородной кислоты:
Характеристика реакционной способности
Реакционная способность нитрилов обусловлена наличием в их структуре цианогруппы -С≡N. Цианогруппа имеет линейное строение, атомы углерода и азота находятся в sp-гибридизации и образуют между собой полярную тройную связь, электронная плотность которой смещена к атому азота.
Проявляя отрицательный индуктивный эффект (-I-эффект), цианогруппа смещает на себя электронную плотность с углеводородного радикала и тем самым увеличивает подвижность атомов водорода при α— углеродном атоме (СН-кислотность).
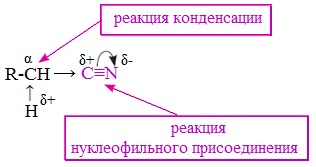
По месту разрыва тройной связи нитрилы вступают в реакции нуклеофильного присоединения , за счет α-углеродных атомов для них характерны реакции конденсации.
Химические свойства
1. Гидролиз нитрилов
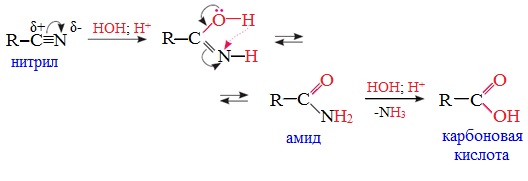
При нагревании с водными растворами щелочей или кислот нитрилы гид-ролизуются с образованием карбоновых кислот.
Гидролиз идет в две стадии. Вначале по месту разрыва кратной связи присоединяется одна молекула воды, в результате чего образуются амиды, которые могут быть выделены в индивидуальном состоянии. Дальнейший гидролиз амидов приводит к карбоновым кислотам:
2. Восстановление нитрилов
При восстановлении нитрилов алюмогидридом лития (LiAlH4) или водородом в присутствии катализатора образуются первичные амины:
Отдельные представители
Ацетонитрил используется для растворения масел, жиров, лаков, эфиров целлюлозы, различных синтетических полимеров и неорганических солей, используется в производстве витамина B1.
Токсичен, всасывается через неповрежденную кожу, опасен при попадании в глаза.
Используют в производстве синтетического волокна (нитрон), бутадиен-нитрильного каучука, широко применяется в органическом синтезе.

Акрилонитрил необратимо связывается с белками, РНК и ДНК различных тканей. Опасен при вдыхании, ядовит при приёме внутрь — вплоть до летального исхода. Пары вызывают раздражение слизистых оболочек и кожи. Действует через неповреждённую кожу. При горении образуются ядовитые газы.
Малононитрил обладает высокой реакционной способностью, широко применяется в органическом синтезе для получения гетероциклических соединений. Используют в производстве витаминов B1 и B6, пестицидов, красителей. Его используют также как сшивающий агент для полимеров, добавку к смазочным маслам, стабилизирующую их вязкость, и комплексообразователь при извлечении золота.

Причиняет вред головному мозгу и сердцу, связанный с недостатком клеточного кислорода.
Источник
Нитрильный способ получения карбоновых кислот
Некоторые карбоновые кислоты встречаются в природе в свободном состоянии (муравьиная, уксусная, масляная, валериановая и др.). Однако, основным источником карбоновых кислот является органический синтез. Рассмотрим основные способы получения карбоновых кислот
Общие способы получения карбоновых кислот
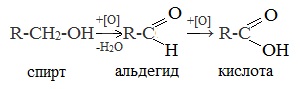
1. Окисление первичных спиртов и альдегидов под действием различных окислителей
В качестве окислителей применяют KMnO4 и K2Cr2O7.
Например:
Для окисления альдегидов используются те же реагенты, что и для спиртов.
При окислении перманганатом калия происходит обесцвечивание фиолетово-розового раствора.
При окислении дихроматом калия — цвет меняется с оранжевого на зеленый.
А также для них характерны реакции «серебряного зеркала» и окисление гидроксидом меди (II) – качественные реакции альдегидов:
2. Гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода
В результате реакции образуются спирты, содержащие три группы ОН у одного атома углерода. Такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:
3. Получение карбоновых кислот из цианидов (нитрилов)
Этот способ позволяет наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия:
Образующийся нитрил уксусной кислоты CH3-CN (ацетонитрил, метилцианид) при нагревании гидролизуется с образованием ацетата аммония:
При подкислении раствора выделяется кислота:
4. Использование реактива Гриньяра (по схеме)
5. Гидролиз галогенангидридов кислот
С водой низшие хлорангидриды реагируют чрезвычайно энергично, образуя соответствующую карбоновую кислоту и соляную кислоту:
В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
2. Окисление алканов кислородом воздуха ( в присутствии катализаторов – солей марганца или при нагревании под давлением)
Обычно образуется смесь кислот. При окислении бутана единственным продуктом является уксусная кислота:
3. Окисление алкенов и алкинов
При жестком окислении алкенов кипящим раствором KMnO4 в кислой среде происходит полный разрыв двойной связи:
При жестком окислении (нагревание, концентрированные растворы, кислая среда) происходит расщепление углеродного скелета молекулы алкина по тройной связи и образуются карбоновые кислоты:
4. Окисление гомологов бензола (получение бензойной кислоты)
Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия:
В лаборатории
1. Гидролиз сложных эфиров
При кислотном гидролизе получают карбоновые кислоты и спирты (реакция обратная этерификации):
2. Из солей карбоновых кислот
3. Гидролиз ангидридов кислот
При легком нагревании с водой ангидриды образуют соответствующие карбоновые кислоты:
4. Щелочной гидролиз галоген производных карбоновых кислот
Специфические способы получения важнейших кислот
Способы получения НСООН
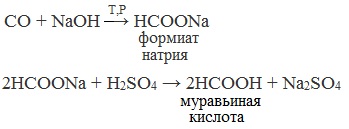
1. Взаимодействие оксида углерода (II) с гидроксидом натрия
Муравьиную кислоту получают нагреванием под давлением гидроксида натрия и оксида углерода (II) под давлением и обработкой полученного формиата натрия серной кислотой:
2. Каталитическое окисление метана
3. Декарбоксилирование щавелевой кислоты
Муравьиную кислоту можно получить при нагревании щавелевой кислоты:
Способы получения СН3СООН
Получение уксусной кислоты для химических целей
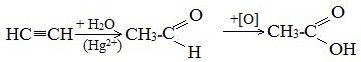
1. Синтез из ацетилена
Данный способ получения уксусной кислоты основан на окислении уксусного альдегида, который в свою очередь получают из ацетилена по реакции Кучерова (ацетилен получают из очень доступного сырья — метана):
2. Каталитическое окисление бутана
Большое значение имеет способ получения уксусной кислоты, основанный на окислении бутана кислородом воздуха:
Процесс получения уксусной кислоты из метана является многостадийным (метан – ацетилен – уксусный альдегид – уксусная кислота). Ее получение окислениям будана сокращает число стадий, что дает большой экономический эффект.
3. Каталитическое карбонилирование метанола
Получение уксусной кислоты для пищевых целей
4. Уксуснокислое брожение этанола
Уксусную кислоту для пищевых целей получают уксуснокислым брожением жидкостей, содержащих спирт (вино. пиво):
Источник