- Нитрат кальция: способы получения и химические свойства
- Способ получения
- Качественная реакция
- Химические свойства
- Нитрат кальция ГОСТ 4142-77
- Содержание
- Свойства
- Физические свойства
- Химические свойства
- Получение
- Реакции с получением нитрата кальция
- Применение
- В сельском хозяйстве
- В пиротехнике
- Нитрат кальция, характеристика, свойства и получение, химические реакции
- Нитрат кальция, характеристика, свойства и получение, химические реакции.
- Краткая характеристика нитрата кальция:
- Физические свойства нитрата кальция:
- Получение нитрата кальция:
- Химические свойства нитрата кальция. Химические реакции нитрата кальция:
- Применение и использование нитрата кальция:
- Мировая экономика
- Справочники
- Востребованные технологии
- Поиск технологий
- О чём данный сайт?
- О Второй индустриализации
Нитрат кальция: способы получения и химические свойства
Нитрат кальция Ca(NO3)2 — соль щелочного металла кальция и азотной кислоты. Белый, при нагревании разлагается. Хорошо растворяется в воде (гидролиза нет).
Относительная молекулярная масса Mr = 164,09; относительная плотность для тв. и ж. состояния d = 2,36; tпл = 561º C (разлагается).
Способ получения
1. Нитрат кальция можно путем взаимодействия кальция и разбавленной азотной кислоты, образуется нитрат кальция, оксид азота (I) и вода:
если кальций будет взаимодействовать с очень разбавленной азотной кислотой , то на выходе будет образовываться нитрат кальция, нитрат аммония и вода:
2. В результате взаимодействия сульфида кальция и концентрированной азотной кислоты образуется нитрат кальция, сера, оксид азота (IV) и вода:
Качественная реакция
Качественная реакция на нитрат кальция — взаимодействие с медью при нагревании в присутствии концентрированной кислоты:
1. При взаимодействии с серной кислотой и медью, нитрат кальция образует сульфат кальция, нитрат меди, бурый газ оксид азота и воду:
Химические свойства
1. Hитрат кальция разлагается при температуре 450 — 500º С с образованием нитрита кальция и кислорода:
а если температуре поднимется выше 561 о С, то на выходе реакции будут образовываться оксид кальция, оксид азота (IV) и кислород:
2. Нитрат кальция реагирует с простыми веществами :
2.1. Нитрат кальция вступает в реакцию с атомным водородом (цинком и в присутствии соляной кислоты). В результате реакции образуется нитрат кальция и вода :
3. Возможны реакции между нитратом кальция и сложными веществами :
Нитрат кальция вступает в реакцию с cолями :
В результате реакции между нитратом кальция и гидрофосфатом натрия при кипении образуется фосфат кальция, азотная кислота и нитрат натрия:
Источник
Нитрат кальция ГОСТ 4142-77
| Нитрат кальция | |
|---|---|
 | |
 | |
 | |
| Традиционные названия | кальциевая селитра, норвежская селитра, азотнокислый кальций |
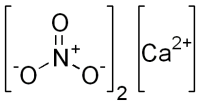
| Хим. формула | Ca(NO3)2 |
| Состояние | гранулы сферической формы белого, светло-серого, светло-бежевого цвета |
| Молярная масса | |
| Т. всп. | негорючая °C |
| Мол. теплоёмк. | 149,33 Дж/(моль·К) |
| Энтальпия образования | -937,2 кДж/моль |
| Растворимость в воде | Безводной: 121,2 г/100 мл (20 °C); 271,0 г/100 мл (40 °C); 359 г/100 мл (51,6 °C). Тетрагидрата: 102 г/100 мл (0 °C); 129 г/100 мл (20 °C); (100 °C) 363 г/100 мл |
| Растворимость в | спирте и ацетоне |
| Кристаллическая структура | |
| Рег. номер CAS | |
| PubChem | 24963 |
| Рег. номер EINECS | 233-332-1 |
| SMILES | |
| RTECS | EW2985000 |
| ChEBI | 64205 |
| Номер ООН | 1454 |
| ChemSpider | 23336 и 21500286 |
| ГОСТ | ГОСТ 4142-77 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
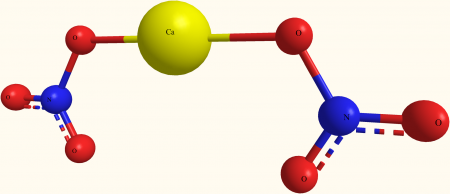
Кальция нитрат (кальциевая селитра, азотнокислый кальций) — неорганическая соль азотной кислоты. Соединение сильно гигроскопично, поэтому его хранят без доступа влаги. Химическая формула Ca(NO3)2.
Содержание
- 1 Свойства
- 1.1 Физические свойства
- 1.2 Химические свойства
- 2 Получение
- 2.1 Реакции с получением нитрата кальция
- 3 Применение
- 3.1 В сельском хозяйстве
- 3.2 В пиротехнике
Свойства
Физические свойства
Химические свойства
При 500 °C начинает разлагаться с выделением O2 и образованием сначала Ca(NO2)2, а затем CaO и NO2. Кальциевая селитра при нормальных условиях негорючая, пожаро- и взрывобезопасная, устойчивая в интервале температур от −60 °C до +155 °C.
Получение
Получают кальция нитрат действием HNO3 на известняк или поглощением нитрозных газов (в основном NO2) известковым молоком. Применяют кальция нитрат как азотное удобрение и для получения особо чистого CaO.
Для получения гранулированной кальциевой селитры используется способ низкотемпературной нейтрализации азотной кислоты природным известняком или продуктами переработки известняка.
Реакции с получением нитрата кальция
Нитрат кальция производится путём обработки известняка с азотной кислотой, после нейтрализации аммиака:
Он также является побочным продуктом процесса Оддо при добыче фосфата кальция:
Так же как нитраты других щелочноземельных металлов и LiNO3, кальциевая селитра при нагревании разлагается на выпуске диоксида азота:
Также нитрат кальция можно получить проделав следующие реакции:
Также образование нитрата кальция возможно и за счет атмосферных явлений:
Применение
Гранулированный, безводный нитрат кальция, применяется как добавка в бетон, в качестве удобрения, для приготовления рассола в холодильной технике, в производстве реактивов, стеклопластиков, а также как один из компонентов для производства взрывчатки.
В сельском хозяйстве
Нитрат кальция является физиологическим щелочным удобрением, пригодным для всех почв и прежде всего для закисленных почв. В сельском хозяйстве применяют как азотное удобрение. Выпускают в гранулированном виде; товарный продукт должен содержать не менее 15,5 % азота, кроме того, к нему добавляют в процессе производства 4—7 % нитрата аммония для уменьшения гигроскопичности удобрения; содержание влаги не должно превышать 15 %. Нитрат кальция вносят под все культуры. Наиболее эффективен на кислых почвах, особенно для весенней подкормки озимых.
В пиротехнике
Несмотря на то, что нитрат кальция в смеси с горючими веществами способен давать недорогой источник кирпично-красного пламени, применение его в этом качестве крайне ограничено из-за сильной гигроскопичности.
Источник
Нитрат кальция, характеристика, свойства и получение, химические реакции
Нитрат кальция, характеристика, свойства и получение, химические реакции.
Нитрат кальция – неорганическое вещество, имеет химическую формулу Ca(NO3)2.
Краткая характеристика нитрата кальция:
Нитрат кальция – неорганическое вещество белого цвета.
Химическая формула нитрата кальция Ca(NO3)2.
Нитрат кальция – неорганическое химическое соединение, соль азотной кислоты и кальция.
Хорошо растворяется в воде, жидком аммиаке, ацетоне, метаноле, этаноле, пропаноле, жидком аммиаке.
Обладает высокой гигроскопичностью, поэтому его хранят без доступа влаги.
С водой нитрат кальция образует кристаллогидрат – тетрагидрат Ca(NO3)2·4H2O.
Негорюч, пожаро- и взрывобезопасен.
Физические свойства нитрата кальция:
| Наименование параметра: | Значение: |
| Химическая формула | Ca(NO3)2 |
| Синонимы и названия иностранном языке | calcium nitrate (англ.) |
кальций азотнокислый (рус.)
кальциевая селитра (рус.)
Получение нитрата кальция:
Нитрат кальция получают в результате следующих химических реакций:
- 1. взаимодействия хлорида кальция и нитрата серебра:
- 2. взаимодействия гидроксида кальция и азотной кислоты:
- 3. взаимодействия оксида кальция и азотной кислоты:
- 4. взаимодействия оксида кальция и тетраоксида диазота:
Реакция протекает в жидком тетраоксиде диазота.
- 5. взаимодействия оксида кальция, оксида азота (IV) и кислорода:
В ходе реакции гидроксид кальция используется в виде суспензии. Реакция представляет собой поглощение оксида азота (IV) известковым молоком.
- 6. взаимодействия сульфита кальция и азотной кислоты:
Химические свойства нитрата кальция. Химические реакции нитрата кальция:
Химические свойства нитрата кальция аналогичны свойствам нитратов других металлов . Поэтому для него характерны следующие химические реакции:
1. реакция взаимодействия нитрата кальция и атомарного водорода:
В результате реакции образуются нитрит кальция и вода .
2. реакция взаимодействия нитрата кальция и кислорода:
В результате реакции образуются оксид кальция и оксид азота (IV) .
3. реакция взаимодействия нитрата кальция и гидроксида натрия :
В результате реакции образуются нитрат натрия и гидроксид кальция . В ходе реакции используется концентрированный раствор гидроксида натрия.
4. реакция взаимодействия нитрата кальция и сульфата меди :
В результате реакции образуются сульфат кальция и нитрат меди.
5. реакция взаимодействия нитрата кальция и молибдата натрия:
В результате реакции образуются молибдат кальция и нитрат натрия.
реакция взаимодействия нитрата кальция и гидроортофосфата натрия:
В результате реакции образуются фосфат кальция , нитрат натрия и азотная кислота. Реакция протекает при кипении.
реакция взаимодействия нитрата кальция и вольфрамата натрия:
В результате реакции образуются вольфрамат кальция и нитрат натрия.
реакция термического разложения нитрата кальция:
В результате реакции образуются в первом случае – нитрит кальция и кислород , во втором – оксид кальция, оксид азота (IV) и вода .
реакция термического разложения тетрагидрата нитрата кальция:
В результате реакции образуются нитрат натрия и вода .
Применение и использование нитрата кальция:
Нитрат кальция используется во множестве отраслей промышленности и для бытовых нужд:
– в сельском хозяйстве в качестве азотного удобрения . Наиболее эффективен на кислых почвах ;
– в строительстве как добавка в бетон ;
– в производстве стеклопластиков.
Примечание: © Фото https://www.pexels.com, https://pixabay.com

нитрат кальция реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие нитрата кальция
реакции
Мировая экономика
Справочники
Востребованные технологии
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (106 553)
- Экономика Второй индустриализации России (102 555)
- Программа искусственного интеллекта ЭЛИС (27 791)
- Метан, получение, свойства, химические реакции (24 252)
- Этилен (этен), получение, свойства, химические реакции (24 154)
- Природный газ, свойства, химический состав, добыча и применение (21 619)
- Крахмал, свойства, получение и применение (20 934)
- Пропилен (пропен), получение, свойства, химические реакции (20 114)
- Целлюлоза, свойства, получение и применение (19 780)
- Прямоугольный треугольник, свойства, признаки и формулы (19 037)
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник


















