- Химические свойства и способы получения муравьиного альдегида
- Реакции присоединения
- Реакции окисления
- Реакции полимеризации
- Получение формальдегида:
- Промышленные методы получения формальдегида
- Лабораторные способы получения формальдегида
- Муравьиный альдегид
- Содержание
- Токсические свойства
- Канцерогенность
- Получение
- Применение
- Муравьиный альдегид. Получение муравьиного альдегида
- Химические свойства
- Производственное получение
- Применение
- Токсические свойства
- Воздействие муравьиного альдегида на организм человека
- Отравление парами формальдегида
- Использование формальдегида в косметических средствах
- Канцерогенность муравьиного альдегида
Химические свойства и способы получения муравьиного альдегида
Задача 4.
Опишите химические свойства муравьиного альдегида. Приведите промышленные и лабораторные способы получения этого соединения.
Решение:
Атом углерода в карбонильной группе находится в состоянии sp 2 -гибридизации и образует 3 сигма-связи (две связи С-Н и одну связь С-О). Сигма-связь образована р-электронами атомов углерода и кислорода. Двойная связь С = О является сочетанием пи- и сигма-связей. Электронная плотность смещена в сторону атома кислорода.
В молекулах альдегидов имеется несколько реакционных центров: электрофильный центр (карбонильный атом углерода), участвующий в реакциях нуклеофильного присоединения; основный центр – атом кислорода с неподеленными электронными парами; Н-С(О)-Н кислотный центр, отвечающий за реакции конденсации; связь С-Н, разрывающаяся в реакциях окисления.
Реакции присоединения
1. Присоединение водорода (восстановление):
Н-CH=O + H2 (t,Ni) → Н-CH2-OH (метиловый спирт);
2. Присоединение аммиака:
3. Присоединение бисульфита натрия:
4. Присоединение циановодородной кислоты (синильной):
Н-CH=O + H-CN → H-CH(CN)-OH;
5. Присоединение гидразина с образованием гидразона:
6. Присоединение аминов с образованием N-замещенного имина:
7. Присоединение тиола с образованием дитиоацеталя (в кислой среде):
8. Присоединение воды с образованием гем-диола:
Н-CH=O + Н-ОН → Н-CH(OH)-OH.
При действии щелочи на формалин получаются метиловый спирт и муравьиная кислота:
2Н-CH=O + Н-ОН → СН3-ОН + Н-СООН.
В присутствии щелочей в водном растворе может идти и другая реакция: формальдегид конденсируется, причем в числе прочих продуктов получается один из простейших сахаров, или гексоз:
6Н-CH=O → C6H12O6 (Реакция Бутлерова: 2Н-CH → O + RbOH = -CH=O);
9. Присоединение спирта с образованием полуацеталя:
10. При взаимодействии формальдегида с ацетальдегидом в газовой фазе в присутствии катализаторов (окись алюминия, ацетат свинца на силикагеле и др.) образуется акролеин:
В водном растворе при большом избытке формальдегида под влиянием гидроокиси кальция конденсация с ацетальдегидом приводит к пентаэритриту:
Высшие алифатические альдегиды дают в этих условиях окси-или диоксиальдегиды (в зависимости от числа H-водородных атомов):
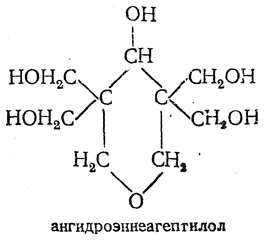
Формальдегид при взаимодействии с ацетоном образует ангидроэннеагептилол:
Реакции окисления
1. Альдегиды – довольно сильные восстановители, и поэтому легко окисляются различными окислителями, например: KMnO4, K2Cr2O7, [Ag(NH3)2]OH, Cu(OH)2. Все реакции идут при нагревании:
Реакции полимеризации
1. Реакция с фенолом с образованием фенолформальдегидных смол:
Получение формальдегида:
Промышленные методы получения формальдегида
1. Окисление метанола.
Реакция проводится в присутствии серебряного катализатороа и при нагревании (около 650—720 °C) или при 400 °C в присутствиии железо-никилиевых катализаторов:
2. Реакция дегидрирования метанола.
Процесс проводится на цинк-медных катализаторах при 600 °C:
3. Окисление метана.
Реакцию проводят при температуре 450 °C и давлении 1—2 МПа на катализаторе AlPO4.
Лабораторные способы получения формальдегида
1. Восстановление метанола:
Реакцию проводят, опуская раскаленную медную проволоку в пробирку с метанолом, образуется резкий запах альдегида. Если процесс окисления повторить несколько раз, то можно получить значительную концентрацию формальдегида.
2. Реакция метанола с перманганатом калия:
Смесь слабого раствора марганцовки и метанола нагревают до кипения. Появляется запах формальдегида, а фиолетовая окраска перманганата исчезает.
3. Реакция метанола с бихроматом калия:
В насыщенный раствор бихромата калия К2Сг2О7 добавляют такой же объем концентрированной серной кислоты. Затем по каплям вводят метанол. Очень осторожно подогревают смесь (отверстие пробирки направляют в сторону!). Реакция идет с выделением тепла. Желтая окраска хромовой смеси исчезает, и появляется зеленая окраска сульфата хрома.
Источник
Муравьиный альдегид
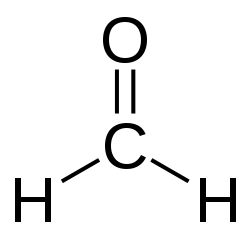
Муравьиный альдегид
| Формальдегид | |
|---|---|
 | |
| Общие | |
| Другие названия | Муравьиный альдегид Метаналь |
| Молекулярная формула | CH2O |
| Молярная масса | 30,03 г/моль |
| Вид | газ с острым запахом |
| Свойства | |
| Плотность | 0,9151 г/см³ (при −80 °C) |
| Растворимость в воде | до 37% |
| Температура плавления | −92 °C |
| Температура кипения | −19,2 °C (в др. источниках, −19,3 °C) |
| Опасность | |
| Описание | Обладает токсичными, канцерогенными свойствами Оказывает сильное влияние на ЦНС Опасен для окружающей среды |
| Категория взрывоопасности | II B |
| Группа взрывоопасности | Т2 |
| Концентрационные пределы воспламенения | 7-73% об. |
| Температура самовоспламенения | 435 °C |
| Термодинамические свойства | |
| Ст. энтальпия образования ΔH | −115,9 кДж/моль (г) |
| Ст. энергия Гиббса образования ΔG | −110 кДж/моль (г) |
| Ст. энтропия образования S | 218,66 Дж/моль·K (г) |
| Ст. мольная теплоёмкость Cp | 35,35 Дж/моль·K (г) |
| Энтальпия кипения ΔHкип | 23,3 кДж/моль |
| Если не указано другое, параметры даны для 25 °C, 100 кПа | |
Формальдегид (от лат. formica — муравей), рекомендуемое международное название метаналь, устаревшее — муравьиный альдегид (CH2=O) — газообразное бесцветное вещество с острым запахом, первый член гомологического ряда алифатических альдегидов.
Содержание
Токсические свойства
Обладает токсичностью, негативно воздействует на генетический материал, репродуктивные органы, дыхательные пути, глаза, кожный покров. Оказывает сильное действие на центральную нервную систему.
Смертельная доза 35 % водного раствора формальдегида (формалина) составляет 10 — 50 г.
Канцерогенность
Формальдегид внесен в список канцерогенных веществ [1] [2] [3] .
Получение
Основной способ получения формальдегида — окисление метанола:
Окисление метанола в формальдегид проводится с использованием серебряного катализатора при температуре 650 °C и атмосферном давлении. Это хорошо освоенный технологический процесс, и 80 % формальдегида получается именно по этому методу. Недавно разработан более перспективный способ, основанный на использовании железо-молибденовых катализаторов. При этом реакция проводится при 300 °C. В обоих процессах степень превращения составляет 99 %.
Процесс дегидрирования метанола, осуществленный на цинк-медных катализаторах при 600 °C, пока не получил широкого развития, однако он является очень перспективным, поскольку позволяет получать формальдегид, не содержащий воды.
Существует также промышленный способ получения формальдегида окислением метана:
Процесс проводят при температуре 450 °C и давлении 1—2 МПа, в качестве катализатора применяется фосфат алюминия AlPO4
Применение
Водный раствор формальдегида — формалин — свёртывает белки, поэтому он применяется для дубления желатина при производстве кинофотоплёнки, для консервации биологических материалов (создание анатомических и других биомоделей), а также как антисептик.
Формальдегид широко применяется при изготовлении пластмасс (таких, как фенопласт и аминопласты), искусственных волокон, из него получают пентаэритрит (сырьё для производства взрывчатых веществ и пластификаторов), триметилопропан. Основная часть формальдегида идет на изготовление древесностружечных материалов, где он используется для получения карбамидной смолы.
Также формальдегид широко используется в качестве консерванта в различных вакцинах, вводимых человеку, последствия чего до сих пор не изучены.
Источник
Муравьиный альдегид. Получение муравьиного альдегида
Муравьиный альдегид, или формальдегид, – это бесцветный газ, обладающий резким, неприятным, специфическим запахом. Он хорошо растворяется в воде, а также в спиртах. Формальдегид очень токсичен и способен вызвать в организме человека патологические изменения. Кроме того, его считают канцерогеном.
Формальдегид – первый член целого гомологического ряда, в который входит алифатический муравьиный альдегид. Муравьиная кислота также проявляет свойства этой группы.
Химические свойства
Формальдегид способен вступать во все реакции, которые свойственны гомологическому ряду алифатических альдегидов. В том числе и с нуклеофилами. Также он связывается с восстановительными реагентами. Это происходит главным образом по причине того, что у формальдегида низкая электронная плотность на атомах углерода. Благодаря этой особенности строения он очень легко вступает в химические реакции даже с самыми слабыми нуклеофилами. Этим объясняет тот факт, что в водных растворах муравьиный альдегид обнаруживается в гидратированном состоянии.
Производственное получение
У этого вещества довольно простая формула. Муравьиный альдегид на химическом языке выглядит так: HCHO. Основной промышленный метод его получения — это окисление метанола. Эта реакция осуществляется с применением серебряного катализатора. Необходимая температура — 650 градусов. Окисление метанола происходит при атмосферном давлении.
Этот технологический процесс уже достаточно длительное время используется повсеместно. Он хорошо освоен. Примерно 80% формальдегида получают благодаря окислительной реакции метанола. Однако это не единственный способ. Недавно был разработан еще более перспективный метод. Он основывается на применении железо-молибденовых катализаторов. В этом случае снижается уровень необходимой температуры до 300 градусов, а это практически вдвое меньше.
Также известен еще один промышленный способ – окисление метана. У реакции этой довольно простая формула: муравьиный альдегид получается при давлении 1-2 МПа при температуре 450 градусов. В качестве катализатора берется фосфат алюминия.
Применение
Метандиол – водный раствор формальдегида, вызывающий денатурацию белков. Это его качество позволяет использовать данное вещество в качестве дубителя при производстве кожаных вещей. Также он нашел широкое применение при изготовлении кинофотопленки. Из-за сильных дубильных свойств формальдегид известен как антисептик. Он повсеместно используется в медицине. На его основе производят такие антисептические препараты, как «Формагель» и «Формидрон». Уже достаточно долгое время муравьиный альдегид применяют в биологии для хранения биоматериалов, например, органов или трупов животных.
В настоящее время получение муравьиного альдегида выгодно деревообрабатывающей и, конечно, мебельной промышленности. Его используют для производства меламинокарбамидоформальдегидных смол. Они применяются при изготовлении ДСП, фанеры и прочих строительных материалов.
При хранении муравьиного альдегида следует учитывать, что при температуре ниже 10 градусов раствор мутнеет и появляется белый осадок. Также формальдегид взаимодействует с кислородом. В результате образуются по причине вырожденного разветвления дополнительные инициаторы цепи.
Токсические свойства
Итак, формальдегид получают методом окисления метанола и метана. Несомненно, он обладает достаточно высокой степенью токсичности. Муравьиный альдегид в первую очередь воздействует на генетический материал. От этого вещества страдают и репродуктивные органы. Но, конечно, чаще отмечается поражение дыхательных путей, кожных покровов и слизистой глаз.
Опасен формальдегид еще и тем, что он оказывает негативное действие на ЦНС.
Муравьиный альдегид не просто токсичен — 60-90 мл вещества (в зависимости от массы тела), попавшие внутрь, вызовут смерть. Симптомы отравления следующие:
- общий упадок сил;
- бледность кожных покровов;
- бессознательное состояние;
- угнетение ЦНС;
- затрудненное дыхание;
- сильная головная боль;
- судороги, особенно в ночное время.
Воздействие муравьиного альдегида на организм человека
Применение муравьиного альдегида в производстве нередко вызывает разные степени отравления у работников предприятия. При сильном ингаляционном поражении, то есть при вдыхании вещества, наблюдаются конъюнктивит и острая форма бронхита, которая иногда приводит к отеку легкого. Симптоматика при длительном воздействии формальдегида будет только нарастать. Спустя непродолжительное время появятся признаки поражения и угнетения ЦНС. Это будет выражаться в постоянном головокружении, возникнет чувство страха, походка станет шаткой, а в ночное время у человека могут быть даже судороги.
Если отравление произошло через рот, то первым симптомом будет ожог слизистой оболочки пищеварительного тракта. Он будет проявляться в виде боли, жжения в горле и по ходу пищевода. Человек ощущает сильные рвотные позывы, масса, отторгаемая желудком, будет содержать кровь. В тяжелых случаях развивается отек гортани и наблюдается рефлекторная остановка дыхания.
При хроническом отравлении малыми концентрациями у человека отмечаются сильная потеря веса, психическое возбуждение, расстройство зрения, бессонница и постоянные головные боли.
Отравление парами формальдегида
Муравьиный альдегид чаще всего обнаруживается в воздухе. У работников предприятий, занятых в работе, связанной с изготовлением искусственных смол, при наличии постоянного и длительного контакта с парами формальдегида возможно отравление. Нередко уже в первые рабочие дни у человека появляются заметные дерматиты на лице, руках. Присутствие формальдегида в организме видно по ухудшению состояния ногтей — они размягчаются и становятся ломкими.
Экземы и дерматиты могут носить аллергический характер. После того как человек перенес отравление, у него формируется к муравьиному альдегиду сильная чувствительность. Имеются сведения о том, что формальдегид неблагоприятно влияет на функционирование репродуктивной системы женского организма.
Использование формальдегида в косметических средствах
Содержание формальдегида допускается в качестве консерванта в косметических средствах, но его концентрация не должна превышать 0,1%. Муравьиный альдегид может присутствовать в зубной пасте, кремах для тела, лица и рук.
Также в фармакологии, в некоторых средствах, препятствующих обильному потоотделению, может находится формальдегид. Его допустимая концентрация — 0,5%. Это вещество — хороший антисептик, даже в столь малых количествах он способен уничтожать микроорганизмы. Строго запрещается наносить на лицо любую мазь, если в ее составе находится 5% формальдегида. Это чревато появлением дерматитов и аллергических реакций. Также муравьиный альдегид не используют для консервации косметических средств, если они будут продаваться в качестве аэрозолей и спреев.
Вся продукция на своей этикетке должна содержать информацию относительно содержания этого опасного вещества, даже если его количество 0,05%. В действительности до сегодняшнего дня не выяснено, как влияет раствор формальдегида на кожу, но известно, что у животных она краснеет и шелушится.
Канцерогенность муравьиного альдегида
Известно, что формальдегид взаимодействует с селеном при участии высококонцентрированной серной кислоты. В результате образуется сульфоэфир-4-тетрадецилидиоксан. Это вещество со сложным названием после обработки гидратом окиси бария становится прекрасным моющим средством. Казалось бы, в чем опасность? Но формальдегид внесен в список веществ, обладающих канцерогенными качествами. Хотя степень его опасности пока не установлена, нельзя не принимать во внимание тот факт, что муравьиный альдегид смертельно опасен для животных. По официальным данным многих научных центров мира, связь между применением формальдегида при производстве красок, смол, текстиля, пластика и возникновением онкологических новообразований у человека доказана. Особенно высок риск развития рака носоглотки.
Источник