Ортофосфат магния
| Ортофосфат магния | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Фосфат магния |
| Традиционные названия | Фосфорнокислый магний |
| Химическая формула | Mg3(PO4)2 |
| Физические свойства | |
| Молярная масса | 262,855 г/моль |
| Термические свойства | |
| Температура плавления | 1357 °C |
| Классификация | |
| Рег. номер CAS | 7757-87-1 |
Ортофосфат магния — неорганическое соединение, соль магния и ортофосфорной кислоты с формулой Mg3(PO4)2. Бесцветные кристаллы. Образует несколько кристаллогидратов.
Содержание
Получение
- Действием разбавленной ортофосфорной кислоты на оксид магния, его гидроксид или карбонат можно получить кристаллогидраты фосфата магния:
- Из водных растворов кристаллизуется в виде кристаллогидратов вида Mg3(PO4)2•4H2O, Mg3(PO4)2•6H2O и Mg3(PO4)2•8H2O.
- Спеканием оксида магния и пирофосфата натрия получается безводная соль:
Применение
- В продуктах питания в качестве пищевой добавки E343 как регулятор кислотности, добавки, препятствующей слёживанию и комкованию сыпучих веществ, а также разрыхлителя.
- В аналитической химии [1] .
Ссылки
Примечания
- ↑В.Н.Тихонов Аналитическая химия магния. — Москва: «Наука», 1973. — С. 61-63.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое «Ортофосфат магния» в других словарях:
Ортофосфат аммония-магния — Общие Систематическое наименование Ортофосфат аммония магния Химическая формула NH4MgPO4 Физические свойства Состояние (ст. ус … Википедия
Ортофосфат стронция — Общие Химическая формула Sr3(PO4)2 Физические свойства Состояние (ст. усл.) бесцветные ромбоэдрические кристаллы Молярная масса 452.8 … Википедия
магния ортофосфат — magnio ortofosfatas statusas T sritis chemija formulė Mg₃(PO₄)₂ atitikmenys: angl. magnesium orthophosphate rus. магний ортофосфорнокислый; магния ортофосфат ryšiai: sinonimas – trimagnio bis(tetraoksofosfatas) … Chemijos terminų aiškinamasis žodynas
Гидроортофосфат магния — Гидроортофосфат магния … Википедия
Цитрат магния — Общие Системати … Википедия
Хлорид магния — Хлорид магния … Википедия
Карбонат магния — См. также: Магния карбонат (лекарственное средство) Карбонат магния … Википедия
Гидроксид магния — Гидроксид магния … Википедия
Сульфат магния — Общие Систематическое наименование Сульфат магния Традиционные названия Сернокислый магния, эпсомская соль Химическая формула MgSO4 Физические свойства Мол … Википедия
Бромид магния — Общие Систематическое наименование Бромид магния Традиционные названия Бромистый магний Химическая формула MgBr2 Физические свойства Состояние (ст. усл … Википедия
Источник
Структура, свойства и применение фосфата магния (Mg3 (PO4) 2)
фосфат магния это термин, используемый для обозначения семейства неорганических соединений, образованных магнием, щелочноземельным металлом и оксоанионфосфатом. Простейший фосфат магния имеет химическую формулу Mg3(РО4)2. Формула указывает, что для каждых двух анионов PO4 3- Есть три катиона Mg 2+ взаимодействуя с этими.
Также эти соединения могут быть описаны как соли магния, полученные из ортофосфорной кислоты (H3ПО4). Другими словами, магний «покрывает» фосфатные анионы независимо от их неорганического или органического представления (MgO, Mg (NO).3)2, MgCl2, Mg (OH)2, и т.д.).
По этим причинам фосфаты магния можно найти в виде нескольких минералов. Вот некоторые из них: catheita -Mg3(РО4)2 · 22H2О-, струвите — (NH4) MgPO4· 6H2Или, чьи микрокристаллы представлены на верхнем изображении, холедалит -Mg2(РО4) (OH) — и боберрита -Mg3(РО4)2· 8H2О-.
В случае бобиерриты ее кристаллическая структура является моноклинной, с кристаллическими агрегатами с веерными формами и массивными розетками. Однако фосфаты магния характеризуются богатой структурной химией, что означает, что их ионы принимают множество кристаллических структур..
- 1 Формы фосфата магния и нейтральность его зарядов
- 1.1 Фосфаты магния с другими катионами
- 2 Структура
- 3 свойства
- 4 использования
- 5 ссылок
Формы фосфата магния и нейтральность его зарядов
Фосфаты магния получают путем замещения протонов H3ПО4. Когда ортофосфорная кислота теряет протон, она остается в виде иона дигидрофосфата, H2ПО4 — .
Как нейтрализовать отрицательный заряд с образованием магниевой соли? Да Mg 2+ приходится два положительных заряда, тогда нужно два Н2ПО4 — . Таким образом, дикислотный фосфат магния Mg (H) получается2ПО4)2.
Затем, когда кислота теряет два протона, остается ион гидрофосфата, HPO4 2- . Теперь, как нейтрализовать эти два отрицательных заряда? Как и Mg 2+ для нейтрализации нужны только два отрицательных заряда, взаимодействует с одним ионом HPO4 2- . Таким способом получают фосфат магниевой кислоты: MgHPO4.
Наконец, когда все протоны потеряны, фосфат-анион PO остается4 3- . Это требует трех катионов Mg 2+ и другой фосфат для сборки в кристаллическое твердое вещество. Математическое уравнение 2 (-3) + 3 (+2) = 0 помогает понять эти стехиометрические соотношения для магния и фосфата.
В результате этих взаимодействий получается трехосновный фосфат магния: Mg3(РО4)2. Почему это трибаза? Потому что он способен принимать три эквивалента Н + чтобы сформировать H снова3ПО4:
Магний фосфаты с другими катионами
Компенсация отрицательных зарядов также может быть достигнута с участием других положительных видов.
Например, чтобы нейтрализовать ПО4 3- , ионы К + , не доступно + , Rb + , Нью-Гемпшир4 + , и т.д., также могут вступать в реакцию, образуя соединение (X) MgPO4. Если X равен NH4 + , образуется безводный струвитный минерал, (NH4) MgPO4.
Учитывая ситуацию, когда другой фосфат вмешивается и отрицательные заряды увеличиваются, другие дополнительные катионы могут быть добавлены к взаимодействиям, чтобы нейтрализовать их. Благодаря этому можно синтезировать многочисленные кристаллы фосфата магния (Na3RBMG7(РО4)6, например).
структура
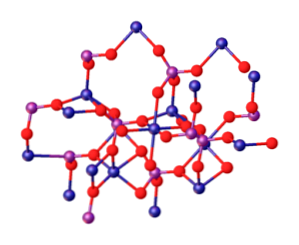
Верхнее изображение иллюстрирует взаимодействие между ионами Mg 2+ и ПО4 3- которые определяют кристаллическую структуру. Однако это только изображение, которое демонстрирует скорее тетраэдрическую геометрию фосфатов. Тогда кристаллическая структура включает тетраэдры фосфатов и сферы магния.
Для случая Mg3(РО4)2 Безводные ионы принимают ромбоэдрическую структуру, в которой Mg 2+ координируется с шестью атомами кислорода.
Выше показано на изображении ниже, с пометкой, что синие сферы являются кобальтом, достаточно заменить их на зеленые сферы магния:
Прямо в центре структуры может быть расположен октаэдр, образованный шестью красными сферами вокруг синеватой сферы..
Кроме того, эти кристаллические структуры способны принимать молекулы воды, образуя гидраты фосфата магния..
Это потому, что они образуют водородные связи с фосфат-ионами (HOH-O-PO3 3- ). Кроме того, каждый фосфат-ион способен принимать до четырех водородных связей; то есть четыре молекулы воды.
Как и Mg3(РО4)2 имеет два фосфата, может принимать восемь молекул воды (что происходит с минералом бобиеррита). В свою очередь, эти молекулы воды могут образовывать водородные связи с другими или взаимодействовать с положительными центрами Mg 2+ .
свойства
Это белое твердое вещество, образующее кристаллические ромбические пластины. Кроме того, он не имеет запаха и вкуса.
Он очень нерастворим в воде, даже когда он горячий, благодаря большой энергии кристаллической решетки; это продукт сильных электростатических взаимодействий между поливалентными ионами Mg 2+ и ПО4 3- .
То есть, когда ионы поливалентны и их ионные радиусы не сильно различаются по размеру, твердое вещество проявляет устойчивость к его растворению.
Он плавится при 1184 ° C, что также свидетельствует о сильных электростатических взаимодействиях. Эти свойства варьируются в зависимости от того, сколько молекул воды он поглощает, и если фосфат обнаружен в некоторых его протонированных формах (HPO4 2- или Н2ПО4 — ).
приложений
Он был использован в качестве слабительного для запоров и желудочной кислотности. Однако его вредные побочные эффекты, проявляющиеся в виде диареи и рвоты, ограничивают его применение. Кроме того, это может привести к повреждению желудочно-кишечного тракта.
Использование фосфата магния для восстановления костной ткани в настоящее время изучается, изучая применение Mg (H)2ПО4)2 как цемент.
Эта форма фосфата магния отвечает следующим требованиям: она является биоразлагаемой и гистосовместимой. Кроме того, его использование в регенерации костной ткани рекомендуется для его силы и быстрого урегулирования.
Оценивается использование аморфного фосфата магния (AMP) в качестве биоразлагаемого и не экзотермического ортопедического цемента. Для получения этого цемента смешайте порошок AMP с поливиниловым спиртом, чтобы образовалась замазка..
Основная функция фосфата магния заключается в обеспечении вклада Mg в живые существа. Этот элемент вмешивается в многочисленные ферментативные реакции в качестве катализатора или посредника, являясь необходимым для жизни.
Дефицит Mg у людей связан со следующими эффектами: снижение уровня Ca, сердечная недостаточность, задержка Na, снижение уровней K, аритмия, длительные сокращения мышц, рвота, тошнота, низкий уровень циркулирующего вещества. Гормон паращитовидной железы и желудка и менструальные судороги, среди других.
Источник