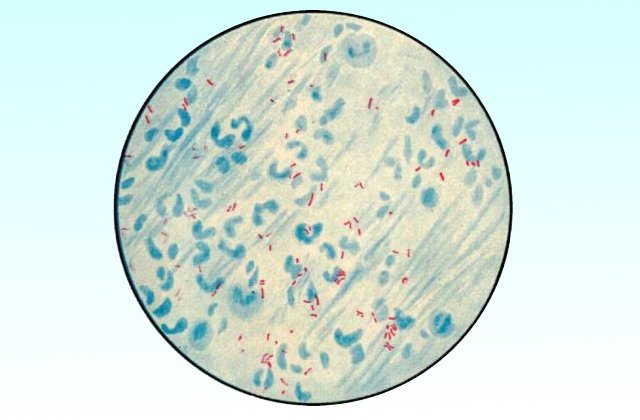
Механизмы окрасок по Граму и Цилю-Нильсену



Метод Грама (Gram). Относится к сложным методам окраски и позволяет дифференцировать грамположительные и грамотрицательные бактерии, что является важным таксономическим признаком. Результат окраски определяется особенностями строения клеточной стенки бактерий. При окраске генцианвиолетом и последующем воздействии раствора Люголя образуется комплексное соединение генцианвиолета и йода с пептидогликаном, которое при обработке спиртом удерживается в клетках грамположительных бактерий, имеющий многослойный пептидогликан и вымывается из грамотрицательных бактерий, имеющих тонкий слой пептидогликана. При дополнительной окраске водным раствором фуксина грамотрицательные бактерии приобретают красный цвет.
Таблица 4 Метод Грама
| Этапы окраски | Цвет бактерий | |
| 1. | На фиксированный мазок поместить фильтровальную бумажку, пропитанную генцианвиолетом, смочить водой, 2-3 минуты | Все бактерии окрашиваются в фиолетовый цвет |
| 2. | Снять бумажку, слить с препарата оставшуюся краску и налить раствор Люголя на 1 минуту | Все бактерии остаются фиолетовыми |
| 3. | Для дифференцирования нанести на мазок этиловый спирт в течение 3-6 с, промыть водой | Грамположительные бактерии остаются фиолетовыми, грамотрицательные обесцвечиваются |
| 4. | Нанести фуксин Пффейфера (водный раствор фуксина) на 1-2 мин, промыть водой, высушить | Грамположительные остаются фиолетовыми, грамотрицательные окрашиваются в красный цвет |
Метод Циля-Нильсена. Относится к сложным методам окраски и позволяет дифференцировать кислотоустойчивые и некислотоустойчивые бактерии.
Таблица 5 Метод Циля-Нильсена
| Этапы окраски | Цвет бактерий | |
| 1. | На фиксированный мазок нанести карболовый раствор фуксина Циля через полоску фильтровальной бумаги и подогреть препарат в пламени горелки до появления паров (повторить 3-4 раза) | Все бактерии окрашиваются в красный цвет |
| 2. | Снять бумагу, промыть мазок водой | Все бактерии остаются красными |
| 3. | Для дифференцирования нанести 5% раствор серной кислоты на 1-2 минуты | Кислотоустойчивые бактерии остаются красными, некислотоустойчивые обесцвечиваются |
| 4. | Нанести водный раствор метиленового синего и докрасить 3-5 мин, промыть водой, высушить | Кислотоустойчивые остаются красными, некислотоустойчивые окрашиваются в синий цвет |
Кислотоустойчивые бактерии имеют особое строение клеточной стенки, содержащей большое количество сложных липидов (миколовая и фтиоловая кислоты, воск D, глико- и фосфолипидовы), что делает эти бактерии кислото-, щелоче- и спиртоустойчивыми. Клеточная стенка этих бактерий плохо воспринимает анилиновые красители и обычные способы окраски. Высокая температура в процессе окраски методом Циля-Нильсена расплавляет липиды, фенол разрыхляет клеточную стенку и краситель проникает внутрь клетки. После остывания препарата липиды вновь затвердевают, прочно удерживая краситель, поэтому кислотоустойчивые бактерии не обесцвечиваются серной кислотой и остаются красными. Некислотоустойчивые бактерии обесцвечиваются и их докрашивают контрастным красителем — метиленовым синим. В основном, метод используется для окраски бактерий, относящихся к роду Мусоbacterium (М.tuberculosis, М.bovis, М.leprae и др.)
III. План практической работы
1. Изучить механизм и этапы окраски по Граму, приготовить мазок из смеси бактерий и окрасить по Граму, заполнить таблицу в рабочей тетради.
2. Изучить механизм и этапы окраски по Цилю-Нильсену, приготовить мазок из сапрофитных микобактерий, окрасить по Цилю-Нильсену, заполнить таблицу в рабочей тетради.
3. Сравнить строение прокариотической и эукариотической клетки по ряду признаков, заполнить таблицу в рабочей тетради.
4. Изучить и перечислить в таблице основные таксономические категории на примере С.tetani и Т.pallidum или других бактерий.
Источник
Кислотоустойчивые бактерии и их окраска по методу Циля-Нильсена
Метод назван именами немецких медиков — микробиолога Франца Циля (1857—1926) и патологоанатома Фридриха Нельсена (1854—1898), которые разработали его в 1882—1883 гг.
Метод окраски микроорганизмов для выявления кислотоустойчивых микобактерий (возбудителей туберкулёза, микобактериозов, лепры), актиномицетов и других кислотоустойчивых микроорганизмов.
— Фиксированный на пламени горелки мазок окрашивают в течение 3 – 5 мин. раствором карболового фуксина Циля или окрашенной фуксином бумажкой с подогреванием до появления паров, но не доводя краситель до кипения.
— Дают препарату остыть, бумажку снимают, сливают избыток красителя, препарат промывают водой.
— Окрашенный препарат обесцвечивают 5%-ным раствором серной кислоты в течение 3 – 5 с или 96° этиловым спиртом, содержащим 3% по объему хлористоводородной кислоты, несколько раз погружая стекло с мазком в стаканчик с солянокислым спиртом.
— После обесцвечивания остаток кислоты сливают и тщательно промывают препарат водой.
— Докрашивают дополнительно метиленовым синим Леффлера 3 – 5 мин.
— Окрашенный препарат промывают водой, подсушивают и микроскопируют.
При окраске препаратов кислоустойчивые бактерии окрашиваются фуксином в рубиново-красный цвет и не обесцвечиваются кислотой.
Некислотоустойчивые бактерии, а также элементы ткани и лейкоциты под действием кислоты обесцвечиваются и приобретают цвет дополнительного красителя.
Механизм взаимодействия антигена и антитела.
В н в предложены 2 гипотезы, объясняющие мехнизм реакции между антигеном и антителом: гипотеза Маррека (теория «решетки») и гипотеза Полинга (теория «фермы»).
Маррек полагает, что при соединении антигена с антителом их молекулы располагаются в чередующемся порядке, образуя решетчатые агломераты. Он предложил схему возможных соединений антигена с антителом. При оптимальных соотношениях антигена и антитела образуются прочные комплексы, которые, постепенно увеличиваясь в размерах, становятся видимыми невооруженным глазом. При избытке антигена образуются мелкие, растворимые, невидимые глазом соединения, так как каждый активный центр антитела: «заполнен» молекулой антигена. При избытке антител образующиеся мелкие комплексы также не могут быть связаны вместе из-за отсутствия антигена в достаточном количестве, вследствие чего образование больших агломератов отсутствует.
Гипотеза Полинга основана на предположении, что антитела имеют только две специфические полярные группы (двухвалентны), а антиген поливалентен, т.е. имеет несколько детерминантных групп. Поэтому при соединении антигена с антителом образуются агломераты, напоминающие «фермы». При оптимальных соотношениях антигена и антитела происходит полное насыщение всех их валентностей, в результате чего образуются прочные комплексы, выпадающие в осадка. При избытке антигена в зависимости от его количества образуются мелкие или рыхлые агломераты и выпадение осадка задерживается. При избытке антител многие валентности их остаются незаполненными и образование комплексов становится невозможным.
Соединение антигена и антитела не носит характера прочной химической реакции, поскольку после получения комплекса антиген — антитело его можно разделить на составные части.
Возбудитель возвратного тифа (эпидемического и эндемического), его характеристика и свойства. Источник инфекции и пути заражения. Методы лабораторной диагностики. Препараты для лечения и профилактики.
Эпидемический возвратный тиф Borellia reccurentis
Эндемический возвратный тиф B.dutoni, B.hispanica, B.persica, B.caucasica
Извитые бактерии, имеющие кр неравномерные завитки и заостренные концы. Спор и капсул не имеют. Подвижны за счет микрофибрилл. По Романовскому-Гимзе окрашиваются в сине-фиолетовый цвет.
| Эпидемиология | Эпидемический возвратный тиф Borellia reccurentis ИИ-больной человек Механизм передачи Пути передачи Гемоконтактный Трансмисивный Переносчики –головные и платянные вши. Эндемический возвратный тиф B.dutoni, B.hispanica, B.persica, B.caucasica Резервуар инфекции в природных очагах – грызуны, хищники, а также аргасовые клещи. Механизм передачи Пути передачи Гемоконтактный Трансмисивный |
| Микробиологическая диагностика | Батериологический -обнаружение в мазках крови бореллий в окраске по Романовскому-Гимзе |
| Специфическая профилактика Спец лечение | Не разработаны |
Билет №10
Дата добавления: 2018-04-04 ; просмотров: 1478 ; Мы поможем в написании вашей работы!
Источник
Окраска по методу Циля-Нильсена и Грама
Окраска по Цилю-Нильсену – это один из методов, используемый для обнаружения при исследовании анализов больного различных заболеваний. В случае изучения мокроты пациента на предмет наличия возбудителей, к примеру, туберкулеза широко используется данный метод. В этой статье пойдет речь о нюансах его проведения, а также о некоторых аналогичных методах.
Область применения метода
Этот метод окрашивания используется в тех случаях, когда необходимо выявить в образце кислотоустойчивые микроорганизмы, к которым относятся возбудители туберкулеза, проказы и микробактериозов. Такие бактерии характеризуются, прежде всего, медленной скоростью роста, общими морфологическими особенностями, а также устойчивостью к кислотам и некоторым другим химическим веществам. Из-за последнего свойства такие бактерии плохо поддаются окраске обычными разведенными красителями. Для окрашивания таких бактерий на препарат наносится и в дальнейшем поджигается фуксин Циля, причем полученная окраска не исчезает под воздействием спирта и кислот.
Необходимые реактивы и оборудование
Для проведения окраски образца по методу Циля-Нильсена необходимы следующие реактивы:
- Метиленовый синий с 10%-ным содержанием спирта;
- Раствор солянокислого спирта;
- Фуксин Циля, состоящий из фенола, фуксина и этилового спирта в количестве 50 г, 10 г и 10 г соответственно.
Также потребуется следующие инструменты:
- Газовая горелка;
- Часы для слежения за временем;
- Вода;
- 96%-ный этиловый спирт;
- Перчатки.
Ход процедуры
Окрашивание по методу Циля-Нильсена состоит из следующих этапов:
- На мазок, находящийся на предметном стекле, накладывается фильтровальная бумага, на которую затем наносится небольшое количество фуксина Циля.
- Затем предметное стекло нагревается до появления характерного пара. После появления пара стеклу нужно дать остыть. Затем нужно повторить эту процедуру еще 2 раза, а затем дать подогретому мазку остыть.
- После этого нужно смыть фуксин с приборного стекла, предварительно убрав бумагу, с помощью дистиллированной воды.
- Затем стекло помещается в раствор соляной или серной кислоты до полного обесцвечивания.
- Наконец, на обесцвеченный препарат наносится раствор метиленового синего. Стекло промывается дистиллированной водой и высушивается для дальнейшего исследования образца под микроскопом.
Липиды, которые содержатся в клеточной стенке кислотоустойчивых бактерий, хорошо удерживают цвет основного красителя. В некислотоустойчивых бактериях стабильно удерживается цвет как основного красителя, так и дополнительного.
Показания к применению метода
При подозрениях на туберкулез исследуется мокрота больного. Длительный кашель с обильными выделениями является показанием для проведения подобного исследования. Визуально наличие возбудителей туберкулеза в организме может выдать мокрота характерной жидкой, пенистой консистенции и признаками гноя, а также мокрота, смешанная с кровью. Обнаружение возбудителей туберкулеза – рисовидных телец, известных также как линзы Коха, облегчается при использовании методов окраски образца. Таких как вышеописанный метод Циля-Нильсена или метод Грама, суть которого будет описана ниже.
Метод Грама
Окраска препарата по методу Грама проводится следующим образом:
- Сперва препарат обрабатывается раствором Люголя на протяжении минуты;
- Затем препарат обесцвечивается с использованием спирта;
- Наконец, препарат промывается с использованием воды и дополнительно окрашивается фуксином.
Классификацию бактерий на грамположительные и на грамотрицательные можно наглядно увидеть при проведении подобной окраски. Первый тип бактерий окрашивается в темно-фиолетовый цвет, тогда как второй тип – в красный цвет. Исходя из такой классификации, можно судить о химическом составе клеточной стенки бактерии и о других ее характерных свойствах.
Заключение
Анализ мокроты пациента является жизненно необходимым для своевременного выявления заболеваний, затрагивающих дыхательные пути, в том числе и туберкулеза. Окрашивание по методу Циля-Нильсена помогает выявить микроорганизмы и возбудители подобных болезней. В том числе и в случаях, когда речь идет об атипичных бактериях. Тем самым позволяет производить более точную и качественную диагностику подобных болезней.
Если вы сталкивались с подобными заболеваниями, знакомы с техниками исследования анализов больного на предмет наличия в них возбудителей инфекции или же у вас есть вопрос по теме, вы можете оставить свой комментарий.
Источник