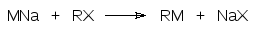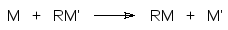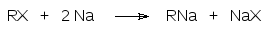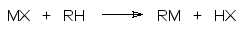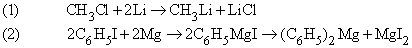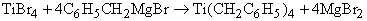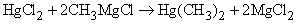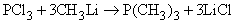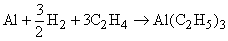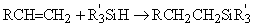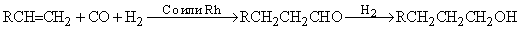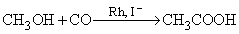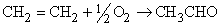1 Способы получения металлорганических соединений
Известно множество способов получения металлорганических соединений. Далее будут представлены наиболее общие и практически важные из них.
1. Прямое алкилирование или арилирование металлов (М) алкилгалогенидами и арилгалогенидами. Реакция протекает в соответствии с общей схемой:
Этим уравнением представлена самая важная реакция в химии металлорганических соединений. В соответствии с этим уравнением или с участием представленной этим уравнением реакции можно получить практически все металлорганические соединения.
Если металл реагирует с галогенидом очень медленно или совсем не реагирует с ним, то можно использовать в качестве исходного соединения его сплав (интерметаллическое соединение) с щелочным или щелочноземельным металлом. Чаще всего используют сплавы с натрием:
Похожая реакция, в которой в роли органической компоненты выступают простые эфиры, идёт только с некоторыми простыми эфирами с участием щелочных металлов.
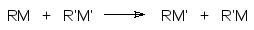
2. Замещение металла в металлорганическом соединении другим металлом. Реакция металлорганического соединения с другим металлом в соответствии с уравнением
подходит для получения более реакционноспособного соединения из менее реакционноспособного. Так, например, действием металлического лития или натрия на диалкилртуть или диарилртуть можно получить соответствующее литий- или натрийорганическое соединение.
3. Реакция металла с углеводородом.
а) замещение атома водорода металлом по схеме:
может быть реализовано только с участием очень активного металла при действии на углеводород с активированным атомом водорода;
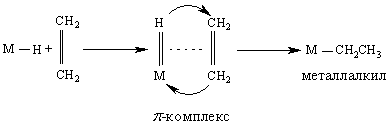
б) присоединение активного (щелочного) металла по двойной С=С-связи;
в) расщепление С–С-связи щелочным металлом.
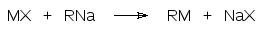
4. Реакции солей металлов с другими металлорганическими соединениями. Это взаимодействие представляет собой один из самых важных и широко используемых способов получения металлорганических соединений:
Этот способ можно использовать для синтеза практически всех типов металлорганических соединений. Равновесие сдвинуто в сторону образования менее реакционноспособной компоненты реакции. В качестве исходных соединений чаще всего используют реактивы Гриньяра и литийорганические соединения.
По этой схеме протекает также реакция галогенидов металлов и органических галогенидов с металлическим натрием:
В этом случае реакция протекает в две стадии: сначала металлический натрий реагирует с органическим галогенидом с образованием натрийорганического соединения, которое сразу взаимодействует с галогенидом другого металла:
Эту двухстадийную реакцию чаще всего используют для получения кремнийорганических соединений, а также органических производных цинка, олова, мышьяка и сурьмы.
5. Реакции солей металлов с углеводородами. Образование металлорганических соединений при взаимодействии углеводородов с солями металлов по схеме:
может идти, в частности, с ароматическими соединениями. Например, самые разные типы органических соединений могут превращаться в ртутьорганические соединения в реакции с ацетатом двухвалентной ртути, а соли меди и серебра могут превращаться в ацетилениды в реакции с ацетиленом.
6. Реакции солей металлов с диазониевыми соединениями. Один из важных способов получения интересных в фармакологическом отношении ариларсониевых солей представлен взаимодействием хлоридов арилдиазония с арсенитами натрия (реакция Барта, H. Bart, 1910 г.):
По аналогичной схеме могут быть получены и арильные производные сурьмы.
Реакция Барта сопровождается окислительным превращением вступающего в реакцию с солью диазония атома металла. Для металлов, которые не могут повышать свою валентность в окислительных превращениях, А. Н. Несмеяновым (1929 г.) был предложен способ арилирования солями диазония в присутствии металла восстановителя. В соответствии с реакцией Несмеянова арильные металлорганические соединения образуются при разложении солей арилдиазония с солями металлов или при разложении комплексных соединений из солей арилдиазония и солей металлов в присутствии, например, дисперсной меди, порошкового железа и других металлов:
Многие галогениды металлов реагируют с диазометаном с образованием галогенметильных производных:
7. Действие на металлы свободных радикалов. Многими исследователями отмечалось образование металлорганических соединений в реакциях короткоживущих метильных и этильных радикалов с мышьяком, сурьмой и висмутом. Показано, например, что в отличие от реакции Несмеянова, разложение хлоридов арилдиазония в присутствии таких металлов, как ртуть, сурьма, свинец и олово, также протекает с участием свободных радикалов.
8. Некоторые металлорганические соединения могут быть синтезированы по реакции специально для этого полученных металлорганических соединений с другими органическими или металлорганическими соединениями.
а) Реакция между двумя металлорганическими соединениями протекает по схеме:
При этом более электроотрицательный органический остаток соединяется с более электроположительным металлом. Кроме того, желательно, чтобы один из продуктов реакции имел низкую растворимость в используемом растворителе и выпадал в осадок.
б) Атом водорода в углеводородах может обмениваться на металл в реакциях с очень активными металлорганическими соединениями, например, по схеме:
Кроме того, металлорганические соединения на основе щелочных металлов могут присоединяться к непредельной С=С-связи несимметричных олефинов.
в) Действием металлорганического соединения на галогенированное органическое соединение можно замещать атом галогена на металл. В частности, бутиллитий переводит некоторые ароматические бромиды и иодиды в литийорганические производные:
Кроме того, органические галогениды могут реагировать с некоторыми металлорганическими соединениями с образованием производных, в которых валентность металла увеличена:
9. Присоединение неорганических или металлорганических гидридов по кратным С=С-связям. Этот способ получения металлорганических соединений находит применение при синтезе органических производных кремния. Так, например, трихлорсилан присоединяется по двойным связям с образованием алкилтрихлорсиланов:
Кроме того, разработаны промышленные способы получения алюминийорганических соединений из гидрида алюминия и олефинов. Так, например, из гидрида алюминия и этилена получают триэтилалюминий, используемый в качестве катализатора полимеризации олефинов.
Источник
МЕТАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
МЕТАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ, химические соединения, в которых углеродные атомы или органические группы связаны непосредственно с атомами металлов. Металлоорганические соединения играют важную роль в химии, во-первых, поскольку удобны для синтеза других соединений, во-вторых, потому что структуры некоторых из них привели химиков к новым полезным концепциям химической связи и, в-третьих, благодаря тому, что участвуют как нестойкие промежуточные соединения (интермедиаты) в каталитических реакциях.
Первое металлоорганическое соединение, диэтилцинк (C2H5)2 Zn, выделено в 1847 английским химиком Э.Франклендом, который пытался удалить атом иода из этилиодида C2H5I посредством реакции с цинком. В действительности реакция протекала по уравнению
и Франкленд получил бесцветную жидкость, диэтилцинк, которая самовоспламенялась при контакте с воздухом и бурно реагировала с водой. (Большинство металлоорганических соединений чрезвычайно реакционноспособны и обычно возгораются на воздухе.) Примерно в то же время в Копенгагене датский химик В.Цейзе также случайно получил соль K[PtCl3C2H4] (соль Цейзе), содержащую, как стало известно позднее, этилен, связанный с платиной.
Эти вещества являются представителями двух главных классов металлоорганических соединений: тех, у которых связи металла с углеродом (M–C) локализованы, и тех, где они делокализованы (в случае переходных металлов). В соединениях первого класса, образуемых всеми металлами, органические группы объединены простыми связями, например, M–CH3 или M–C6H5. Существуют также соединения типов M=CR2 и MєCR, с двойными и тройными металл-углеродными связями, – это карбеновые и карбиновые соединения соответственно.
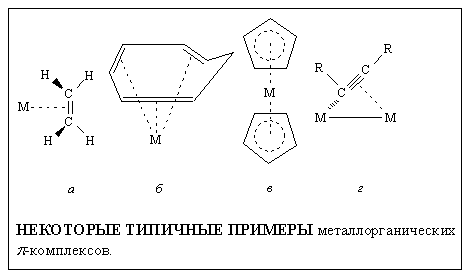
Другой большой класс металлоорганических соединений – p-комплексы. Их называют так потому, что в химическом связывании с d-орбиталями переходных металлов участвуют p-электроны и p-орбитали ненасыщенных органических соединений с C=C-, CєC-, C=N- и т.п. связями (см. также ХИМИЯ ОРГАНИЧЕСКАЯ; МОЛЕКУЛ СТРОЕНИЕ). p-Комплексы включают все соединения, где органическая группа с кратными углерод-углеродными связями присоединена к переходному металлу.
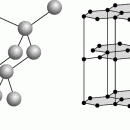
p-Комплексы.
У этилена связь направлена перпендикулярно оси связи C=C (а); циклические олефины могут быть связаны по схеме б; ароматические кольца – нейтральные, как в бензоле C6H6, или заряженные, как у циклопентадиенил-аниона C5H5 – , — могут быть связаны по схеме в. Первое и наиболее известное из таких «сандвичевых» соединений — ферроцен (C5H5)2Fe — имеет структуру типа в. Ацетилены могут быть связаны с двумя атомами металлов по схеме г. Известны тысячи p-комплексов, многие из них — со сложными структурами.
СИНТЕЗ И ПРИМЕНЕНИЕ
Синтез.
Металлоорганические соединения щелочных металлов и магния широко используются как реагенты в органическом синтезе. Их можно приготовить в виде эфирных растворов по реакциям типа (1) и (2):
Смешанные магнийорганические соединения типа RMgX, где X = Cl, Br или I, известны под названием «реактивы Гриньяра» по имени французского химика В.Гриньяра, разработавшего условия их применения для органического синтеза (впервые их получил в 1899 Ф.Барбье – учитель Гриньяра). Реактивы Гриньяра вступают в многочисленные реакции и могут быть использованы, в частности, для синтеза других металлоорганических соединений, например:
Литийорганические соединения типа RLi широко применяются в фармацевтической промышленности для получения разнообразных органических соединений. Примером может служить синтез P(CH3)3:
Алюминийорганические соединения можно получить по реакции типа:
Применение.
Относительно немногие металлоорганические соединения используются как таковые; это, в основном, — кремнийорганические соединения (см. также КРЕМНИЙОРГАНИЧЕСКИЕ ПОЛИМЕРЫ) и тетраэтилсвинец Pb(C2H5)4, применявшийся как антидетонатор для бензина (см. также НЕФТЬ И ГАЗ). Оловоорганические соединения используются в красках, препятствующих биологическому обрастанию судов и подводных сооружений, и как катализаторы в производстве некоторых пластмасс. Ртутьорганические соединения применялись в сельском хозяйстве в качестве фунгицидов, но их использование запрещено во многих странах по экологическим соображениям, т.к. ртутьорганические соединения превращаются микроорганизмами в водорастворимый и токсичный ион метилртути CH3Hg + (послуживший причиной экологического бедствия в Минамате в Японии). В природе важную роль играет витамин B12, кобальторганическое соединение, дефицит которого в организме приводит к анемии; его действие, по-видимому, заключается в переносе органических групп путем образования Co–C-связей (см. также ПЛАСТМАССЫ; ВИТАМИНЫ).
Катализ.
В промышленности большое значение имеют каталитические реакции, в которых металлоорганические соединения возникают в виде нестойких интермедиатов. Эти реакции могут протекать гомогенно в растворах или гетерогенно, с участием металлоорганических частиц на таких носителях, как оксид алюминия, силикагель или уголь (см. также КАТАЛИЗ). Ниже приводятся примеры катализируемых металлами реакций, имеющих важное промышленное значение.
Полимеризация олефинов.
Полимеризация этилена и пропилена протекает с участием каталитической смеси алкилалюминия и хлорида титана. Катализаторы этого типа называются катализаторами Циглера – Натта, так как процесс был разработан К.Циглером (ФРГ) и Д.Натта (Италия), которые получили в 1963 Нобелевскую премию за эту работу. Бутадиен и сходные непредельные соединения могут быть заполимеризованы в каучук в присутствии алкиллития или алкилнатрия.
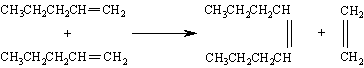
Соединения молибдена и вольфрама катализируют родственную реакцию, называемую реакцией метатезиса (диспропорционирования) олефинов:
Гидрирование кратных связей.
Эта важная реакция может быть гетерогенной или гомогенной. Гомогенная реакция с катализатором Уилкинсона RhCl[P(C6H5)3]3 применяется в фармацевтической промышленности; используя оптически активные фосфиновые лиганды, можно осуществить экономичный асимметрический синтез таких лекарственных средств, как L-ДОФА (L-3,4-дигидроксифенилаланин).
Родственная реакция, называемая гидросилилированием, состоит в присоединении триалкилсилана к олефину:
Реакции оксида углерода
CO. Промышленный синтез на основе оксида углерода(II) проводят с участием кобальторганических или родийорганических промежуточных соединений, в которых ацильная группа связана с металлом, R–CO–M. Реакция состоит в превращении M–R в M–COR путем «внедрения» оксида углерода по связи углерод – металл. Соединение M–R в некоторых случаях можно получить по реакции гидрида металла с олефином, например:
Важное место в промышленном синтезе занимают реакция гидроксиформилирования (оксо-синтез):
продуктами которой являются альдегиды или спирты, и процесс Монсанто – превращение метанола в уксусную кислоту с участием иодида родия:
В этих процессах металлоорганические соединения возникают на поверхности катализатора как интермедиаты.
Реакции окисления.
Многие реакции окисления органических соединений катализируются металлами, как, например, вакер-процесс – превращение этилена в ацетальдегид при помощи медно-палладиевого катализатора:
Интермедиатом в этом процессе служит этиленовый p-комплекс, сходный с солью Цейзе.
Коттон Ф., Уилкинсон Дж. Основы неорганической химии. М., 1979
Металлоорганическая химия переходных металлов. Основы и применения. М., 1989
Источник