- Химия, Биология, подготовка к ГИА и ЕГЭ
- Получение бензола и его
- получения бензола
- Способы получения аренов
- Получение аренов
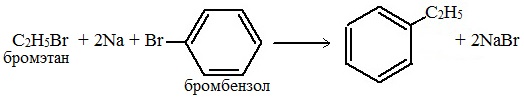
- 1. Реакция Вюрца-Фиттига
- 2. Дегидроциклизация алканов
- 3. Дегидрирование циклоалканов
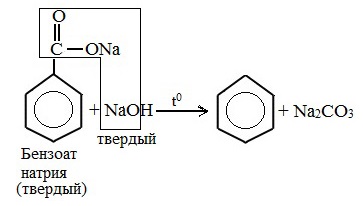
- 4. Декарбоксилирование солей бензойной кислоты
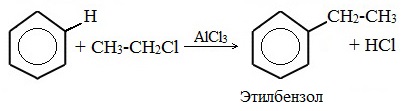
- 5. Алкилирование бензола и его гомологов
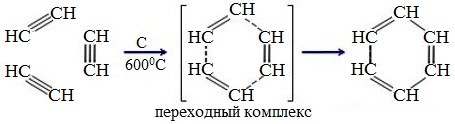
- 6. Тримеризация ацетилена
- 7. Получение стирола
- Лабораторные способы получения бензола
- Лабораторные способы получения бензола
Химия, Биология, подготовка к ГИА и ЕГЭ
Получение бензола и его
Мы рассмотрим «классические» методы получения бензола — те, которые описаны в каждом учебнике по химии, и рассмотрим получение из разных классов органических соединений, т.к. цепочки реакций, которые предлагаются в ЕГЭ, подразумевают умение получать бензол «из всего» 🙂
«Классические» реакции
получения бензола
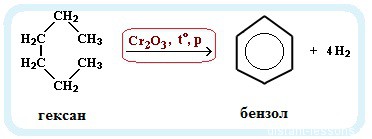
- Ароматизация нефти. Точнее, это реакция циклизации гексана. Называется метод «ароматизация нефти», т.к. из нее получают гексан:
С6H14 → C6H6 + 4H2
Обратите внимание на условия реакции — давление, температуру и катализатор. Они означают, что при обычных условиях гексан не вступит в такую реакцию. Алканы вообще довольно нереакционноспособные вещества.
С6H12 → C6H6 + 3H2
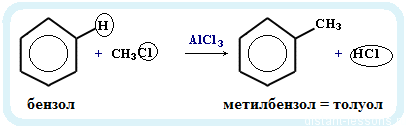
- Получение гомологов бензола: алкилирование бензола:
реакция проводится в присутствии катализатора — галогенидов алюминия, например, AlCl3:
C6H6 + CH3Cl → C6H5CH3 + HCl
Именная реакция — реакция Зелинского. Получение бензола из ацетилена:
3С2H2 → C6H6
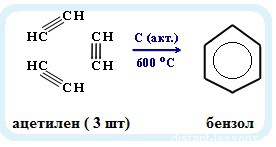
1. Получение бензола из неорганических веществ:
- 1 вариант:
Исходное вещество — карбид кальция СaC2:
CaC2 + 2H2O → Ca(OH)2 + C2H2 — ацетилен
дальше — реакция Зелинского : 3С2H2 → C6H6 Это самый короткий путь получения. - 2 вариант:
Исходное вещество — карбид алюминия Al4C3:
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4 — метан
2СH4 (1500 °C) → C2H2 + 3H2
дальше — реакция Зелинского
2. Получение бензола и его гомологов из других неорганических веществ:
1) получение бензола из алканов:
СH4 (1500 °C) → C2H2 (С, 600ºС) → С6H6
2) получение бензола и его гомологов из алкенов:
С2H4 → C2H2 →C6H6
Схема: алкен → дибромалкан → циклоалкан → гомолог бензола
CH2=CH-(CH2)4-CH3 + HBr → CH3-CH( Br )-(CH2)4-CH3
CH3-CH(Br)-(CH2)4-CH3 + Br2 → CH3-CH( Br )-(CH2)4-CH2 Br
CH3-CH( Br )-(CH2)4-CH2 Br + Zn → C6H13-СH3 — метилциклогексан + ZnBr2
C6H13-СH3 → С6H5-CH3 + 4H2
Источник
Способы получения аренов
Арены (ароматические углеводороды) – это непредельные (ненасыщенные) циклические углеводороды, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Общая формула: CnH2n–6 при n ≥ 6.
Получение аренов
1. Реакция Вюрца-Фиттига
Хлорбензол реагирует с хлорметаном и натрием. При этом образуется смесь продуктов, одним из которых является толуол:
2. Дегидроциклизация алканов
Алканы с углеродной цепью, содержащей 6 и более атомов углерода в главной цепи, при дегидрировании образуют устойчивые шестиатомные циклы, т. е. циклогексан и его гомологи, которые далее превращаются в ароматические углеводороды.
Гексан при нагревании в присутствии оксида хрома (III) в зависимости от условий может образовать циклогексан и потом бензол:
Гептан при дегидрировании в присутствии катализатора образует метилциклогексан и далее толуол:
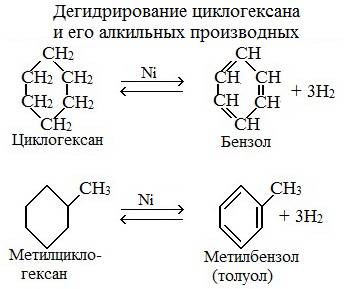
3. Дегидрирование циклоалканов
При дегидрировании циклогексана и его гомологов при нагревании в присутствии катализатора образуется бензол или соответствующие гомологи бензола.
| Например, при нагревании циклогексана в присутствии палладия образуется бензол и водород |
| Например, при нагревании метилциклогексана в присутствии палладия образуется толуол и водород |
4. Декарбоксилирование солей бензойной кислоты
Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении.
R–COONa + NaOH → R–H + Na2CO3
Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты.
Взаимодействие бензоата натрия с гидроксидом натрия в расплаве протекает аналогично реакции получения алканов по реакции Дюма с образованием бензола и карбоната натрия:
5. Алкилирование бензола и его гомологов
- Арены взаимодействуют с галогеналканами в присутствии катализаторов (AlCl3, FeBr3 и др.) с образованием гомологов бензола.
| Например, бензол реагирует с хлорэтаном с образованием этилбензола |
- Ароматические углеводороды взаимодействуют с алкенами в присутствии хлорида алюминия, бромида железа (III), фосфорной кислоты и др.
| Например, бензол реагирует с этиленом с образованием этилбензола |
| Например, бензол реагирует с пропиленом с образованием изопропилбензола (кумола) |
- Алкилирование спиртами протекает в присутствии концентрированной серной кислоты.
| Например, бензол реагирует с этанолом с образованием этилбензола и воды |
6. Тримеризация ацетилена
При нагревании ацетилена под давлением над активированным углем молекулы ацетилена соединяются, образуя бензол.
При тримеризации пропина образуется 1,3,5-триметилбензол.
7. Получение стирола
Стирол можно получить дегидрированием этилбензола:
Стирол можно также получить действием спиртового раствора щелочи на продукт галогенирования этилбензола (1-хлор-1-фенилэтан):
Источник
Лабораторные способы получения бензола
Основным природным источником ароматических углеводородов является нефть и каменный уголь.
В промышленности
1.При коксовании (сухая перегонка) каменного угля образуется каменноугольная смола, из которой выделяют бензол, толуол, ксилолы, нафталин и многие другие органические соединения.
2.Ароматизация нефти
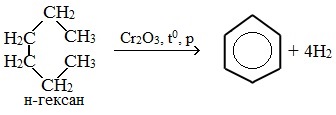
а) дегидроциклизация (дегидрирование и циклизация) алканов в присутствии катализатора (с числом атомов углерода больше 6):
б) дегидрирование циклоалканов и его гомологов:
При пропускании ацетилена над активированным углем образуется бензол (реакция Зелинского):
В лаборатории
1.Декарбоксилирование солей бензойной кислоты (сплавление солей бензойной кислоты с твердой щелочью)
Соли бензойной кислоты называются бензоаты.
2.Гомологи бензола получают из галогенпроизводных (реакция Вюрца- Фиттига)
Реакции получения аренов указывают на взаимосвязь между различными группами углеводородов и на взаимное превращение их друг в друга.
3.Алкилирование бензола (получение гомологов бензола)
Гомологи бензола получают его взаимодействием с галогеналканами или алкенами в присутствии безводного хлорида алюминия (реакция Фриделя-Крафтса):
При дегидрировании этилбензола образуется производное бензола с непредельной боковой цепью – винилбензол (стирол) C6H5-CН=СН2 (исходное вещество для получения ценного полимера полистирола).
Источник
Лабораторные способы получения бензола
4.1.4. Получение бензола
4.1.4.1. Источники бензола
В настоящее время основными источниками ароматических соединений, в том числе и бензола, являются продукты коксования каменного угля (коксовый газ и каменноугольная смола) и продукты переработки нефти.
Продукты коксования каменного угля
Коксование каменного угля проводится с целью получения кокса для металлургической промышленности. Измельченные до зерен размером 3 мм и тщательно перемешанные угли (шихту) нагревают в специальных коксовых печах или коксовых батареях без доступа воздуха при 1000–1250 °С в течение 14–16 ч. В процессе коксования уголь разлагается с образованием твердого остатка — кокса (75–80 %) и летучих веществ, так называемого прямого коксового газа (схема 4.1.1).
В выделяющихся летучих продуктах содержатся пары каменноугольной смолы (80–130 г/м 3 ), низкокипящие ароматические углеводороды, в основном бензол и его ближайшие гомологи — толуол и ксилолы (30–40 г/м 3 ), а также пары воды, сероводород, аммиак, оксид и диоксид углерода, метан, этан и др. Обычно из 1 т. сухой шихты образуется 340–350 м 3 коксового газа.
Полученный коксовый газ пропускают через эффективную систему конденсаторов и скрубберов для разделения продуктов, входящих в его состав (рис. 4.1.3.)
Летучие продукты коксования (прямой коксовый газ) из печи 1 попадают по стоякам в газосборную трубу 2. Там происходят первичное охлаждение и конденсация газа за счет испарения аммиачной воды, которая впрыскивается в трубу через специальные разбрызгиватели. Продукты коксования при этом охлаждаются до 85–90 °С, и некоторая их часть конденсируется. Из газосборной трубы коксовый газ поступает в холодильник 3, в котором охлаждается до 30–35 °С, при этом конденсируется дополнительное количество смолы. Выходящий из холодильника газ содержит смоляной туман и для его отделения проходит электрофильтр 4, после чего газодувкой 5 направляется на установку 7 для улавливания аммиака и пиридиновых оснований.

Схема 4.1.1. Коксование каменного угля

Рис. 4.1.3. Технологическая схема конденсации и улавливания летучих продуктов коксования каменного угля:
1 — коксовая печь; 2 — газосборная труба; 3, 8, 12 — холодильники; 4 — электрофильтр;
5 — газодувка; 6 — сепаратор; 7 — установка для улавливания аммиака и пиридиновых снований;
9 — абсорбер; 10 — теплообменник; 11 — десорбер
Конденсат из газосборной трубы 2, холодильника 3 и электрофильтра 4 разделяют в сепараторе 6 на органический и водный слои. Органический слой представляет собой каменноугольную смолу, содержащую более высококипящие органические вещества; ее направляют на переработку в «смолоперегонный» цех. Водный слой (аммиачная вода) частично возвращается в газосборную трубу 2 для первичного охлаждения продуктов коксования, а частично направляется туда же, куда попадает и коксовый газ после электрофильтра: на установку 7. На этой установке имеются испаритель аммиака из аммиачной воды, сатуратор для поглощения азотистых оснований серной кислотой, кристаллизатор для сульфата аммония и аппарат для вытеснения пиридиновых оснований аммиаком из их сульфатов.
Газ после установки 7 еще содержит пары летучих органических соединений (бензол, толуол). Для их улавливания газ охлаждают водой в холодильнике 8 непосредственного смешения и направляют в абсорбер 9, орошаемый поглотительным маслом. Выходящий из абсорбера так называемый обратный коксовый газ используют для обогревания коксовых печей. Значительная часть газа направляется на химическую переработку. Насыщенное поглотительное масло, выходящее из нижней части абсорбера, проходит теплообменник 10, в котором подогревается обратным регенерированным маслом, и поступает в десорбер 11. Там происходит ректификация, в результате которой отгоняется смесь легких ароматических соединений (сырой бензол). Освобожденное от сырого бензола поглотительное масло отдает тепло насыщенному маслу в теплообменнике 10, дополнительно охлаждается в холодильнике 12 и вновь используется для абсорбции бензольных углеводородов из коксового газа.
Ароматические соединения, образовавшиеся при коксовании, находятся в каменноугольной смоле и сыром бензоле. Выход каменноугольной смолы составляет 32–34 кг, а сырого бензола 10–11 кг на 1 т. сухого угля.
Каменноугольная смола. Выход и состав каменноугольной смолы зависят от характера угля и условий сухой перегонки, причем важнейшими факторами являются форма и размеры аппаратуры, скорость нагревания, температура и продолжительность процесса. В целом выход смолы небольшой (
3–4 %), однако она вырабатывается в огромных количествах, т. к. масштабы коксохимического производства, обслуживающего металлургию, достаточно велики.
Каменноугольная смола представляет собой вязкую жидкость черного цвета с запахом фенола (плотность 1200–1300 кг/м 3 ). Она является сложной смесью органических соединений, в основном ароматических. Состав ее до конца не изучен. В настоящее время идентифицировано около 500 соединений (
60 % от общей массы смолы). Большое количество соединений образуется также в процессе переработки смолы.
Переработка каменноугольной смолы состоит в разделении ее ректификацией на отдельные фракции с последующей кристаллизацией, экстракцией и повторной ректификацией полученных фракций. Ректификацию осуществляют таким образом, чтобы получить фракции, содержащие максимально возможное количество подлежащего выделению вещества. В результате смолу разделяют на ряд следующих первичных фракций:
1) до 170 °С — легкая (0,6 % от массы смолы), состоит преимущественно из низкокипящих ароматических углеводородов (сырой бензол);
2) 170–210 °С — фенольная (2,5 % от массы смолы), содержит в больших количествах фенолы;
3) 210–230 °С — нафталиновая (10 % от массы смолы), содержит 80–85 % нафталина;
4) 230–290 °С — поглотительная (9,5 % от массы смолы), содержит большое количество различных ароматических веществ. Эту фракцию после отделения фенольных соединений и пиридиновых оснований используют как поглотительное масло для извлечения сырого бензола из коксового газа.
5) 290–410 °С — антраценовая (25,4 % от массы смолы), содержит преимущественно полициклические соединения;
6) остаток — пек (около 52 % от массы смолы).
Каждую из фракций обрабатывают щелочью для удаления кислых составных частей (преимущественно фенолов) и кислотой для выделения азотистых оснований. После этого очищенные фракции вновь перегоняют. Твердые углеводороды (нафталин, антрацен) отжимают от масла. Из легкой фракции (после обработки щелочью для удаления фенолов и экстракции оснований серной кислотой) отделяют перегонкой сырой бензол, который объединяют с выделенным из коксового газа.
Сырой бензол. Сырой бензол представляет собой в основном смесь низкокипящих ароматических углеводородов. Его подвергают переработке с целью выделения бензола, толуола, ксилолов и сольвента (сольвент-нафты). Переработка сырого бензола осложнена присутствием в нем непредельных соединений и соединений, содержащих серу (тиофен и его гомологи), температуры кипения которых близки к температурам кипения основных веществ. Поэтому переработка сырого бензола состоит из двух основных процессов: 1) очистки ароматических углеводородов от примесей непредельных и содержащих серу соединений и 2) разделения смеси очищенных ароматических соединений ректификацией.
Основным методом очистки является промывка концентрированной серной кислотой с последующей нейтрализацией раствором щелочи. При этом в результате процессов полимеризации, сополимеризации, конденсации и сульфирования образуются так называемая кислая смолка, продукты, растворимые в воде и серной кислоте и легко отделяемые от углеводородов, и вещества, частично растворимые в углеводородах ряда бензола и выделяющиеся при последующей ректификации в виде кубовых остатков.
С целью сокращения потерь очистке подвергают не весь сырой бензол, а выделяемые из него в результате предварительной ректификации более или менее узкие фракции ароматических углеводородов: так называемые фракции БТК (бензол—толуол—ксилол) и БТКС (бензол—толуол—ксилол—сольвент).
Широкое распространение получил также метод каталитической гидроочистки, который заключается в обработке сырого бензола и его фракций водородом или коксовым газом. При этом ароматические углеводороды освобождаются от примесей непредельных соединений; соединений, содержащих серу; азот и кислород, из которых в результате гидрирования и гидрогенолиза образуются насыщенные углеводороды, сероводород, аммиак и вода. Каталитическая гидроочистка протекает при 300–500 °С и давлении водорода 2–2,5 МПа. При дальнейшей ректификации сырого бензола получают бензол, толуол, ксилолы, сольвент.
Коксохимическая промышленность в течение длительного времени являлась единственным поставщиком ароматического сырья. Она сохраняет свое монопольное положение и в настоящее время по производству полициклических ароматических соединений, используемых в промышленности, хотя из каменноугольной смолы извлекается не более 0,1 % их общего количества. Однако в производстве бензола и его гомологов в послевоенные годы на первое место выдвинулась нефтехимическая промышленность.
Продукты переработки нефти
Нефть является важным источником ароматических соединений. Некоторые нефти, например уральские и среднеазиатские, содержат значительные количества ароматических углеводородов, которые могут быть выделены перегонкой или химическими способами. Однако во многих нефтях содержание ароматических соединений крайне низкое. И тем не менее, ароматические углеводороды можно получать из любой нефти, т. к. углеводороды других классов при высоких температурах, и особенно в присутствии катализаторов, могут частично превращаться в ароматические. Особенно легко образуются ароматические соединения из полиметиленовых углеводородов с шестичленными циклами, которые в больших количествах содержатся, например, в кавказских нефтях.
Ароматические углеводороды образуются в процессе высокотемпературного крекинга нефтепродуктов при 650–750 °С и давлении, близком к атмосферному. В процессе крекинга образуются: 1) газообразные продукты (до 50 % от массы сырья), содержащие до 30 % этилена, водород и предельные углеводороды; 2) жидкие продукты — смола (40–60 %, а в некоторых случаях 80–90 % от массы сырья), содержащая бензол, толуол, ксилолы и др.; 3) кокс (небольшое количество). Недостатком этого способа является сравнительно малый выход ароматических углеводородов.
Использование катализаторов при крекинге нефтепродуктов позволяет снизить температуру процесса и увеличить выход ароматических соединений.
Каталитический риформинг. Наибольшее количество ароматических углеводородов в настоящее время получают методом каталитического риформинга. Промышленный процесс протекает при 470–550 °С. В этих условиях все углеводороды, присутствующие в исходном сырье, претерпевают те или иные превращения. Ароматические углеводороды образуются в основном в результате дегидрирования шестичленных циклоалканов (уравнение (4.1.1)) и дегидроизомеризации пятичленных алкилциклоалканов (уравнение (4.1.2)). В меньшей степени они образуются вследствие дегидроциклизации парафиновых углеводородов (уравнение (4.1.3)). Одновременно протекают и другие реакции. Выход и состав продуктов риформинга зависит от природы используемого катализатора, состава исходного сырья, а также параметров процесса.
Как видно из рис. 4.1.4, превращение циклогексана (2) в бензол (1) термодинамически возможно уже при 520–570 К (250–300 °С), причем равновесие реакции в значительной степени смещается вправо при дальнейшем повышении температуры.
Пятичленные углеводороды сначала превращаются в циклогексан и его гомологи, а при последующем дегидрировании также образуют ароматические соединения (уравнение (4.1.2)).
Термодинамические данные показывают, что равновесие данной изомеризации при высокой температуре неблагоприятно для образования циклогексана (2). Однако, благодаря последующему дегидрированию и превращению циклогексана в бензол, циклогексан непрерывно выводится из системы, что способствует высокой степени конверсии метилциклопентана (3).
При более жестком режиме риформинга в образовании циклических соединений возрастает роль реакции дегидроциклизации парафинов (уравнение (4.1.3)).
Первоначально процесс риформинга проводили на алюмосиликатном катализаторе, который в основном способствовал дегидрированию. Выход ароматических углеводородов был низким (25–30 %). Затем перешли к использованию платиновых катализаторов на алюмооксидных носителях (платформинг). Это привело к увеличению доли реакции дегидроциклизации парафиновых углеводородов и повышению выхода ароматических углеводородов до 35–40 %. В последнее время стали использовать платинорениевый катализатор на носителе кислотного типа (рениформинг). Состав смеси, образующейся при каталитическом риформинге на алюмоплатиновых и платинорениевых катализаторах, значительно отличается от состава исходной смеси (табл. 4.1.1).
Углеводородный состав исходной смеси и продуктов риформинга
Источник