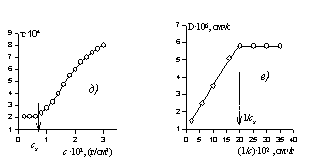6.3. Определение критической концентрации мицеллообразования
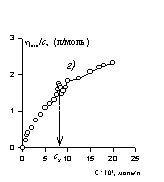
Определение ККМ может осуществляться при изучении практически любого свойства растворов в зависимости от изменения их концентрации. Наиболее часто в исследовательской практике используются зависимости мутности растворов, поверхностного натяжения, электрической проводимости, коэффициента преломления света и вязкости от общей концентрации растворов. Примеры получающихся зависимостей приведены на рис. 2.56.
Критическую концентрацию мицеллообразования определяют по той точке, которая соответствует излому на кривых зависимостей свойств растворов от концентрации. Считается, что при концентрациях, меньших ККМ в растворах ПАВ, присутствуют лишь молекулы и зависимость любого свойства определяется именно концентрацией молекул. При образовании мицелл в растворах свойство будет претерпевать резкое изменение в связи со скачкообразным увеличением размера растворенных частиц. Так, например, молекулярные растворы ионогенных ПАВ проявляют электрические свойства, характерные для сильных электролитов, а мицеллярные – характерные для слабых электролитов. Это проявляется в том, что эквивалентная электрическая проводимость в растворах ионогенных ПАВ при концентрациях ниже ККМ в зависимости от корня квадратного из концентрации растворов оказывается линейной, что характерно для сильных электролитов, а после ККМ – зависимость ее оказывается типичной для слабых электролитов.
Аналогичное изменение наблюдается и на зависимостях практически любого свойства растворов ПАВ от их концентрации.
Водные растворы многих поверхностно-активных веществ обладают особыми свойствами, отличающими их как от истинных растворов низкомолекулярных веществ, так и от коллоидных систем. Одной из отличительных особенностей растворов ПАВ является возможность существования их как в виде молекулярно-истинных растворов, так и в виде мицеллярных — коллоидных.
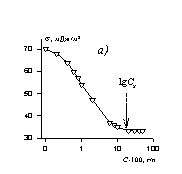
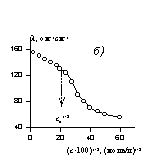
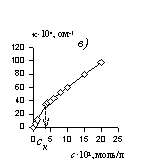
Рис. 2.56. Зависимость свойств растворов ПАВ от концентрации. Свойство: а – поверхностное натяжение (s) растворов додецилсульфата натрия при 25 о С ; б – эквивалентная электрическая проводимость (l) растворов децилтриметиламмоний бромида при 40 о С ; в – удельная электрическая проводимость (k) растворов децилсульфата натрия при 40 о С; г – вязкость (hотн/с) растворов додецилсульфата натрия при 30 о С; д- мутность (t) растворов 6-оксиэтилированного октанола при 20 0 С; е-коэффициент диффузии растворов оксидиметиддодециламина при 30 о С(D).
Переход из молекулярного состояния в мицеллярное происходит, как правило, в достаточно узкой области концентраций, ограниченной, так называемыми, граничными концентрациями. Впервые наличие таких граничных концентраций обнаружил шведский ученый Экваль. Он установил, что при граничных концентрациях многие свойства растворов резко меняются. Эти граничные концентрации лежат ниже и выше средней ККМ; только при концентрациях, меньших минимальной граничной концентрации, растворы ПАВ аналогичны истинным растворам низкомолекулярных веществ.
В принципе, исследование любого свойства растворов ПАВ от его концентрации позволяет определить среднюю концентрацию, при которой система совершает переход в коллоидное состояние. К настоящему моменту описано более сотни разнообразных методов определения критической концентрации мицеллообразования; некоторые из них, кроме ККМ, позволяют также получать богатую информацию о структуре растворов, величине и форме мицелл, их гидратации и т.д. Мы остановимся только на тех методах определения ККМ, которые используются наиболее часто.
Для определения ККМ по изменению поверхностного натяжения растворов ПАВ часто используются методы максимального давления в газовом пузырьке, сталагмометра, отрыва кольца или уравновешивания пластины, измерения объема или формы висящей или лежащей капли, взвешивания капель и др.
Определение ККМ этими методами основано на прекращении изменения поверхностного натяжения раствора при предельном насыщении адсорбционного слоя на поверхности раздела «вода — воздух», «углеводород — вода», «раствор — твердая фаза».
Наряду с определением ККМ эти методы позволяют найти величину предельной адсорбции, поверхностную активность, минимальную площадь, приходящуюся на молекулу в адсорбционном слое. На основании экспериментальных значений поверхностной активности на границе «раствор-воздух» и предельных площадей, приходящихся на молекулу в насыщенном адсорбционном слое, может быть определена также длина полиоксиэтиленовой цепи неионогенных ПАВ и величина углеводородного радикала. Определение ККМ при различных температурах часто используют для расчета термодинамических функций мицеллообразования.
Исследования показывают, что наиболее точные результаты получаются при измерении поверхностного натяжения растворов ПАВ методом уравновешивания пластины. Достаточно хорошо воспроизводятся результаты, найденные сталогмометрическим методом. Менее точные, но достаточно корректные данные получаются при использовании метода отрыва кольца. Плохо воспроизводятся результаты чисто динамических методов.
При определении ККМ вискозиметричесим методом экспериментальные данные выражают обычно в виде зависимости приведенной вязкости от концентрации растворов ПАВ. Вискозиметрический метод также позволяет определить наличие граничных концентраций мицеллообразования и гидратацию мицелл по характеристической вязкости. Этот метод особенно удобен для неионогенных ПАВ в связи с тем, что у них отсутствует электровязкостный эффект.
Определение ККМ по светорассеянию основано на том, что при образовании мицелл в растворах ПАВ резко возрастает рассеяние света частицами и увеличивается мутность системы. По резкому изменению мутности раствора и определяют ККМ. При измерении оптической плотности или светорассеяния растворов ПАВ часто наблюдают аномальное изменение мутности, особенно в том случае, если ПАВ содержит некоторое количество примесей. Данные светорассеяния используют для определения мицеллярной массы, чисел агрегации мицелл и их формы.
Определение ККМ по диффузии проводят измеряя коэффициенты диффузии, которые связаны как с размером мицелл в растворах, так и с их формой и гидратацией. Обычно значение ККМ определяют по пересечению двух линейных участков зависимости коэффициента диффузии от разведения растворов. Определение коэффициента диффузии позволяет рассчитать гидратацию мицелл или их размер. Совмещая данные измерения коэффициента диффузии и коэффициента седиментации в ультрацентрифуге, можно определить мицеллярную массу. Если измерить гидратацию мицелл независимым методом, то по коэффициенту диффузии можно определить форму мицелл. Наблюдение за диффузией проводится обычно при введении в растворы ПАВ дополнительного компонента – метки мицелл, поэтому метод может дать искаженные результаты при определении ККМ, если произойдет смещение мицеллярного равновесия. В последнее время коэффициент диффузии измеряют при использовании радиоактивных меток на молекулах ПАВ. Такой способ не смещает мицеллярного равновесия и дает наиболее точные результаты.
Определение ККМ рефрактометрическим методом основано на изменении коэффициента преломления растворов ПАВ при мицеллообразовании. Этот метод удобен тем, что не требует введения дополнительных компонентов или применения сильного внешнего поля, которые могут сместить равновесие «мицеллы-молекулы», и оценивает свойства системы практически в статических условиях. Он требует, однако, тщательного термостатирования и точного определения концентрации растворов, а также необходимости учета времени эксперимента в связи с изменением коэффициента преломления стекла за счет адсорбции ПАВ. Метод дает хорошие результаты для неионогенных ПАВ с невысокой степенью оксиэтилирования.
В основе определения ККМ ультраакустическим методом лежит изменение характера прохождения ультразвука через раствор при образовании мицелл. При изучении ионогенных ПАВ этот метод удобен даже для весьма разбавленных растворов. Растворы неионогенных веществ труднее поддаются характеристике этим методом, особенно если растворенное вещество имеет малую степень оксиэтилирования. С помощью ультраакустического метода можно определить гидратацию молекул ПАВ как в мицеллах, так и в разбавленных растворах.
Широко распространенный кондуктометрический метод ограничен только растворами ионогенных веществ. Кроме ККМ он позволяет определить степень диссоциации молекул ПАВ в мицеллах, что необходимо знать для корректировки мицеллярных масс, найденных по светорассеянию, а также для введения поправки на электровязкостный эффект при расчете гидратации и чисел ассоциации методами, связанными с явлениями переноса.
Иногда используются такие методы, как ядерный магнитный резонанс или электронный парамагнитный резонанс, которые дают возможность кроме ККМ измерять «время жизни» молекул в мицеллах, а также как ультрафиолетовая и инфракрасная спектроскопия, которые позволяют выявить расположение молекул солюбилизата в мицеллах.
Полярографические исследования, так же как и измерения рН растворов, часто связаны с необходимостью введения третьего компонента в систему, что, естественно, искажает результаты определения ККМ. Методы солюбилизации красителя, солюбилизационного титрования и хроматографии на бумаге, к сожалению оказываются недостаточно точными для измерения ККМ, но зато позволяют судить о структурных изменениях мицелл в относительно концентрированных растворах.
Источник
X Международная студенческая научная конференция Студенческий научный форум — 2018
ОПРЕДЕЛЕНИЕ КРИТИЧЕСКОЙ КОНЦЕНТРАЦИИ МИЦЕЛЛООБРАЗОВАНИЯ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ РАЗЛИЧНОЙ ПРИРОДЫ
Согласно проведенным исследованиям мицеллярные структуры имеют широкую область применения. В настоящее время данные структуры активно используются в космецевтике, пищевой промышленности, фармакологии, хозяйственной промышленности и др. Это связано со способность мицелл инкапсулировать внутрь активные компоненты и осуществлять адресную доставку мицеллированного компонента. Кроме того, мицеллы считаются биоразлагаемыми и уменьшают агрессивное действие некоторых ПАВ. Одной из важнейших характеристик ПАВов является критическая концентрация мицеллообразования (ККМ). В данной работе было произведено определение критических концентраций мицеллообразования следующих ПАВов: децил глюкозид, твин-80, кокоил изеотионат натрия.
Поверхностно-активными называют вещества, с увеличением концентрации которых в растворе поверхностное натяжение на границе раздела фаз понижается. Поверхностно-активные вещества имеют дифильное строение. Молекулы ПАВ состоят из гидрофильной и гидрофобной (олеофильной) частей, что является характерной отличительной особенностью их строения. Гидрофильная часть представлена полярными группами: − СООН; −NH2; −ОН; −SO3H; −NO2 и др. Гидрофобную часть образуют углеводородные радикалы парафиновых, нафтеновых и ароматиче-ских углеводородов.
По способности к диссоциации в водных растворах ПАВ делят на ионогенные и неионогенные. Ионогенные ПАВ подразделяют на анионные, катионные и амфолитные.
Анионные ПАВ диссоциируют в воде с образованием поверхностно активного аниона. К ПАВ этого типа относят:
а) карбоновые кислоты и их соли с общей формулой R−COOM (где М — металл), например, олеат натрия С17Н35СOONa;
б) алкилсульфаты ROSO2OM, например, n-Додецилбензол- триметиламмонийхлорид;
в) арилсульфонаты ArSO2OM — додецилбензолсульфонат натрия C12H25C6H4SO3Na;
г) вещества, содержащие другие типы поверхностно — активных анионов, например, фосфаты, тиосульфаты.
Катионные ПАВ диссоциируют в воде с образованием поверхностно — активного катиона. К ним относятся:
а) соли алкилзамещенных аммониевых оснований, например додециламмонийхлорид C12H25N + H3Cl − ;
б) соли первичных, вторичных и третичных алифатических и ароматических аминов, например, додецилпиридинийхлорид C12H25N + C5H5Cl − .
Амфолитные ПАВ содержат две функциональные группы, одна из которых имеет кислый, а другая — основный характер:
Неионогенные ПАВ не диссоциируют в растворах на ионы, например, додециловый эфир тетраэтиленгликоля С12Н25О(С2Н4О)4Н. Гидрофильные свойства неионогенных ПАВ определяются наличием полиоксиэтиленовой цепи (С2Н4О)n.
Все дифильные ПАВ делят на истинно растворимые и коллоидные. К первой группе относят растворимые в воде дифильные органические соединения с небольшим углеводородным радикалом, например, низшие спирты, фенолы, кислоты и их соли, амины. Эти вещества находятся в растворе в виде молекул или ионов. Они применяются в качестве смачивателей, вспенивателей, гидрофобизаторов при флотации, диспергаторов и т.д.
Ко второй группе относят коллоидные ПАВ. Главной отличительной особенностью этих веществ является способность образовывать термодинамически устойчивые (лиофильные) гетерогенные дисперсные системы — мицеллярные коллоиды.
Основными характерными свойствами коллоидных ПАВ являются:
высокая поверхностная активность;
способность к самопроизвольному мицеллообразованию при концентрации ПАВ выше некоторого определенного значения, называемого критической концентрацией мицеллообразования (ККМ);
способность растворов ПАВ к солюбилизации;
высокая способность к стабилизации дисперсных систем [1].
Мицелла – подвижный молекулярный ассоциат, существующий в равновесии с соответствующим мономером, причем молекулы мономера постоянно присоединяются к мицелле и отщепляются от нее (10 –8 –10 –3 с). Радиус мицелл 2–4 нм, агрегируются 50–100 молекул.
Мицеллообразование – процесс, аналогичный фазовому переходу, при котором происходит резкий переход от молекулярно-дисперсного состояния ПАВ в растворителе к ассоциированному в мицеллы ПАВ при достижении критической концентрации мицеллообразования (ККМ).
Мицеллообразование в водных растворах (прямые мицеллы) обусловлено равенством сил притяжения неполярных (углеводородных) частей молекул и отталкивания полярных (ионогенных) групп. Полярные группы ориентированы в сторону водной фазы. Процесс мицеллообразования имеет энтропийную природу и связан с гидрофобными взаимодействиями углеводородных цепей с водой: объединение углеводородных цепей молекул ПАВ в мицеллу ведет к росту энтропии из-за разрушения структуры воды [2].
Рис. 2. Обращенная и прямая мицелла
При формировании обратных мицелл полярные группы объединяются в гидрофильное ядро, а углеводородные радикалы образуют гидрофобную оболочку. Энергетический выигрыш мицеллообразования в неполярных средах обусловлен выгодностью замены связи «полярная группа – углеводород» на связь между полярными группами при их объединении в ядро мицеллы.
Движущими силами образования мицелл являются межмолекулярные взаимодействия:
гидрофобное отталкивание между углеводородными цепями и водным окружением;
отталкивание одноименно заряженных ионных групп;
вандерваальсово притяжение между алкильными цепями [3].
Критическая концентрация мицеллообразования
Значение ККМ соответствует истинной растворимости ПАВ. При более высокой концентрации образуется мицеллярная коллоидная система. Под мицеллой ПАВ понимают агрегат дифильных молекул. Число молекул, составляющих мицеллу, называют числом агрегации, а общую сумму молекулярных масс молекул мицеллы — мицеллярной массой. С ростом концентрации ПАВ в растворе форма мицелл изменяется от сферической (мицелла Гартли), которой соответствует ККМ1, до цилиндрической, дискообразной (ККМ2) и до пластинчатой (ККМ3). Затем может образоваться жидкокристаллическая структура.
Рис. 2. Схема образования мицелл: а — сферические, б — цилиндрические, в – дискообразные
Исследования водных растворов коллоидных ПАВ показали, что мицеллообразование может происходить только выше некоторой температуры Тк, называемой точкой Крафта.
Ниже температуры Тк растворимость ПАВ мала, и в этой области температур существует равновесие между кристаллами и истинным раствором ПАВ. В результате возникновения мицелл общая концентрация ПАВ при увеличении температуры резко возрастает. Истинная (молекулярная) растворимость ПАВ определяется величиной ККМ и практически не изменяется.
Рис. 3. Фазовая диаграмма растворов ПАВ вблизи точки Крафта
Значение ККМ соответствует истинной растворимости ПАВ. При более высокой концентрации образуется мицеллярная коллоидная система. Под мицеллой ПАВ понимают агрегат дифильных молекул. Число молекул, составляющих мицеллу, называют числом агрегации, а общую сумму молекулярных масс молекул мицеллы — мицеллярной массой. С ростом концентрации ПАВ в растворе форма мицелл изменяется от сферической (мицелла Гартли), которой соответствует ККМ1, до цилиндрической, дискообразной (ККМ2) и до пластинчатой (ККМ3). Затем может образоваться жидкокристаллическая структура.
Увеличение содержания ПАВ в растворе обусловлено ростом числа мицелл. При этом мицеллярная растворимость растет с повышением температуры. Поэтому вблизи точки Крафта возможен непрерывный переход от чистого растворителя и истинного раствора к мицеллярному раствору и через него к разного типа жидкокристаллическим системам.
Для неионогенных ПАВ, являющихся жидкостями, точка Крафта отсутствует. Более характерной для них является другая температурная граница — точка помутнения. Помутнение связано с увеличением размера мицелл и расслоением системы на две фазы из-за дегидратации полярных групп мицелл с повышением температуры.
Основными факторами, влияющими на критическую концентрацию мицеллообразования, являются: строение углеводородного радикала, характер полярной группы, наличие в растворе электролитов и неэлектролитов, температура.
Известно, что энергия растворения органических соединений в воде линейно уменьшается с увеличением длины радикала. Чем больше размер углеводородного радикала ПАВ, тем меньше растворимость ПАВ в воде и тем ниже точка ККМ. Для органической среды с увеличением длины углеводородного радикала растворимость ПАВ повышается и ККМ возрастает.
Роль гидрофильных групп в водных растворах ПАВ заключается в том, чтобы удержать образующиеся агрегаты в воде и регулировать их размер.
Сравнение свойств ионогенных и неионогенных ПАВ, имеющих одинаковые углеводородные цепи, показывает, что мицеллярная масса ионогенных ПАВ намного меньше, чем для неионогенных. Для неионогенных ПАВ значения ККМ в водных растворах обычно лежат в пределах 10 -5 — 10 -4 моль/л, для ионогенных они смещены в область более высоких концентраций 10 -3 — 10 -2 моль/л.
При добавлении индифферентного электролита мицеллярная масса ионогенных ПАВ растет и ККМ снижается, а мицеллярная масса неионогенных ПАВ практически не изменяется [4].
Методы определения критической концентрации мицеллообразования
Методы определения ККМ основаны на резком изменении физико-химических свойств растворов ПАВ при переходе от молекулярного раствора к мицеллярному.
Наиболее часто в исследовательской практике используются зависимости мутности растворов, поверхностного натяжения, электрической проводимости, коэффициента преломления света и вязкости от общей концентрации растворов.
Критическую концентрацию мицеллообразования определяют по той точке, которая соответствует излому на кривых зависимостей свойств растворов от концентрации. Считается, что при концентрациях, меньших ККМ в растворах ПАВ, присутствуют лишь молекулы и зависимость любого свойства определяется именно концентрацией молекул. При образовании мицелл в растворах свойство будет претерпевать резкое изменение в связи со скачкообразным увеличением размера растворенных частиц. Так, например, молекулярные растворы ионогенных ПАВ проявляют электрические свойства, характерные для сильных электролитов, а мицеллярные – характерные для слабых электролитов. Это проявляется в том, что эквивалентная электрическая проводимость в растворах ионогенных ПАВ при концентрациях ниже ККМ в зависимости от корня квадратного из концентрации растворов оказывается линейной, что характерно для сильных электролитов, а после ККМ – зависимость ее оказывается типичной для слабых электролитов.
Аналогичное изменение наблюдается и на зависимостях практически любого свойства растворов ПАВ от их концентрации [5].
1. Определение ККМ по изменения поверхностного натяжения.
Для определения ККМ по изменению поверхностного натяжения растворов ПАВ часто используются методы максимального давления в газовом пузырьке, сталагмометра, отрыва кольца или уравновешивания пластины, измерения объема или формы висящей или лежащей капли, взвешивания капель и др.
Определение ККМ этими методами основано на прекращении изменения поверхностного натяжения раствора при предельном насыщении адсорбционного слоя на поверхности раздела «вода — воздух», «углеводород — вода», «раствор — твердая фаза».
Исследования показывают, что наиболее точные результаты получаются при измерении поверхностного натяжения растворов ПАВ методом уравновешивания пластины.
Рис. 4. Зависимость поверхностного натяжения раствора ПАВ от концентрации.
2. Определение ККМ по вязкости.
При определении ККМ вискозиметрическим методом экспериментальные данные выражают обычно в виде зависимости относительной вязкости от концентрации растворов ПАВ. Вискозиметрический метод также позволяет определить наличие граничных концентраций мицеллообразования и гидратацию мицелл по характеристической вязкости. Этот метод особенно удобен для неионогенных ПАВ в связи с тем, что у них отсутствует электровязкостный эффект [6].
Рис. 5 .Зависимость относительной вязкости водных растворов ДПХ от концентрации при температуре 303К (а) и 308К (б).
2. Определение ККМ кондуктометрическим методом.
Широко распространенный кондуктометрический метод ограничен только растворами ионогенных веществ. Кроме ККМ он позволяет определить степень диссоциации молекул ПАВ в мицеллах, что необходимо знать для корректировки мицеллярных масс, найденных по светорассеянию, а также для введения поправки на электровязкостный эффект при расчете гидратации и чисел ассоциации методами, связанными с явлениями переноса.
Рис. 6. Зависимость электропроводности раствора ПАВ от концентрации.
4. Определение ККМ по светорассеянию.
Определение ККМ по светорассеянию основано на том, что при образовании мицелл в растворах ПАВ резко возрастает рассеяние света частицами и увеличивается мутность системы. По резкому изменению мутности раствора и определяют ККМ. При измерении оптической плотности или светорассеяния растворов ПАВ часто наблюдают аномальное изменение мутности, особенно в том случае, если ПАВ содержит некоторое количество примесей. Данные светорассеяния используют для определения мицеллярной массы, чисел агрегации мицелл и их формы.
Рис. 7. Зависимость мутности растворов ПАВ от концентрации.
5. Определение ККМ рефрактометрическим методом.
Определение ККМ рефрактометрическим методом основано на изменении коэффициента преломления растворов ПАВ при мицеллообразовании. Этот метод удобен тем, что не требует введения дополнительных компонентов или применения сильного внешнего поля, которые могут сместить равновесие «мицеллы-молекулы», и оценивает свойства системы практически в статических условиях. Он требует, однако, тщательного термостатирования и точного определения концентрации растворов, а также необходимости учета времени эксперимента в связи с изменением коэффициента преломления стекла за счет адсорбции ПАВ. Метод дает хорошие результаты для неионогенных ПАВ с невысокой степенью оксиэтилирования [7].
Рис. 8. Зависимость показателя преломления от объема толуола, добавленного к 100 мл водного раствора НПАВ.
Определение ККМ различных растворов ПАВ по вязкости
Децил глюкозид – неионогенный ПАВ,состоящий из сахаров (глюкозы), полученных из кукурузного крахмала, и жирных кислот (деканол – дециловый спирт) кокосового ореха.
Рис. 9. Структурная формула децил глюкозида.
Для определения вязкости данного вида ПАВ была приготовлена серия растворов различной концентрации: 0,1%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 10%.
Полученные результаты представлены в таблице 1.
Таблица 1. Вязкость растворов децил глюкозида различной концентрации.
Концентрация, %
Концентрация, М
Кинематическая вязкость, мм 2 /c
Источник