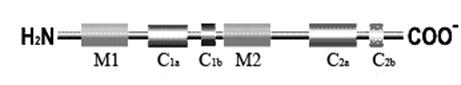
5. Обратимая ковалентная модификация
Ковалентная (химическая) модификация — это регуляторный механизм повышения или снижения активности одних ферментов под действием других ферментов, посредством изменения их химической структуры в результате аденилирования, фосфорилирования, ацетилирования и других воздействий.
В то время как при аллостерической регуляции низкомолекулярное соединение (метаболит) связывается с ферментом или освобождается из комплекса с ферментом, при данном типе регуляции фермент подвергается ковалентному изменению в реакции, катализируемой специальным ферментом. Принцип такого регуляторного механизма ясен из следующих уравнений:
У ряда ферментов активность изменяется при ковалентном обратимом присоединении фосфата. Такое фосфорилирование осуществляют протеинкиназы с помощью АТР.
БЕЛОК + АТР ФОСФОРИЛИРОВАННЫЙ БЕЛОК + ADP
Обратный процесс — дефосфорилирование — осуществляют фосфатазы.
ФОСФОРИЛИРОВАННЫЙ БЕЛОК БЕЛОК + ФОСФАТ
Примеры таких ферментов:
1) фосфорилаза а, которая фосфоролитически отщепляет глюкозо-1-фосфат от гликогена;
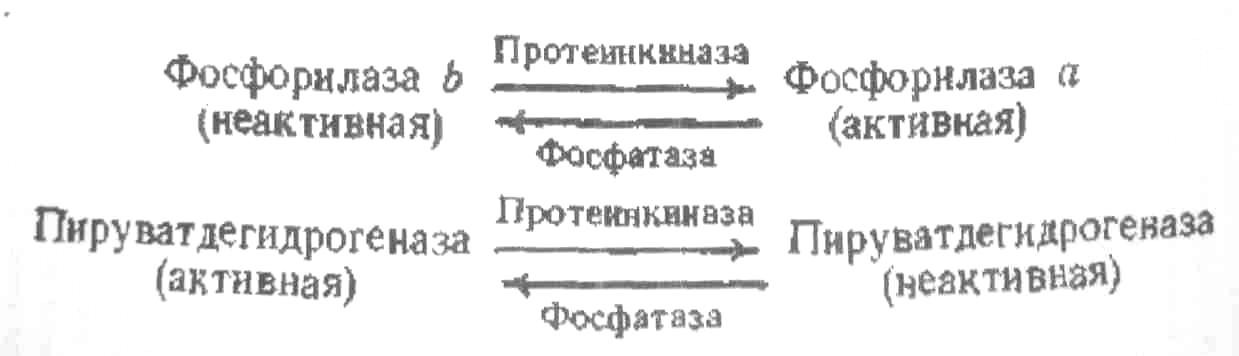
Как видно, рассматриваемые здесь ферменты существуют в двух формах, активной и неактивной, и эти формы способны переходить одна в другую. При регуляции такого типа активность одного фермента (конвертируемого) изменяется под действием другого (конвертирующего). Благодаря тому, что одна молекула второго из них может модифицировать много молекул первого, достигается эффект усиления. Иногда конвертирующий фермент сам в свою очередь может изменяться, и тогда возникает регуляторный каскад: протеинкиназа 1 активирует протеинкиназу 2, протеинкиназа 2 активирует протеинкиназу 3 и т. д.
Стоящий в начале каскада конвертирующий фермент (в нашем примере протеинкиназа 1) подвержен регуляции иного типа, в большинстве случаев аллостерической.
На конвертирующие ферменты могут влиять также продукты или субстраты конвертируемого фермента. Например, пируват тормозит активность той протеинкиназы, которая инактивирует (см. выше) комплекс пируватдегидрогеназы. Таким способом пируват, накопившийся в повышенной концентрации, ускоряет свое собственное превращение. Ацетил-СоА, наоборот, стимулирует ту же самую протеинкиназу. Если для цикла лимонной кислоты ацетил-СоА имеется уже в достаточном количестве и в то же время поступает из других источнике (например, в результате расщепления жиров), то превращение пирувата в ацетил-СоА тормозится и пируват направляется по другим путям.
Наряду с фосфорилированием известны и другие обратимые химические модификации:
аденилирование (присоединение AМФ);
AДФ-рибозилирование (присоединение аденозиндифосфорибозы);
ацилирование (присоединение остатка жирной кислоты);
карбамилирование (присоединение карбамильного остатка — CONH2);
переход SH SS (дегидрирование двух остатков -SH в белке с образованием дисульфидного мостика -S-S-).
Следует подчеркнуть, что существование регуляции активности ферментов путем их ковалентной модификации не противоречит тому общему положению, что регуляция осуществляется аллостерическими белками. В самом деле, ферменты, катализирующие ковалентную модификацию других ферментов, сами аллостерически регулируются. В этом смысле ковалентную модификацию можно рассматривать как одно из проявлений аллостерической регуляции.
СПЕЦИФИЧЕСКИЕ МЕХАНИЗМЫ РЕГУЛЯЦИИ АКТИВНОСТИ ФЕРМЕНТОВ У МИКРООРГАНИЗМОВ. РЕГУЛЯЦИЯ ПУТЕЙ БИОСИНТЕЗА И ПРОМЕЖУТОЧНОГО ОБМЕНА. РОЛЬ ЭНЕРГЕТИЧЕСКОГО ЗАРЯДА В РЕГУЛЯЦИИ КЛЕТОЧНОГО МЕТАБОЛИЗМА. РЕГУЛЯТОРНЫЕ ЭФФЕКТЫ ПАСТЕРА И КРЭБТРИ. РЕГУЛЯЦИЯ МЕТАБОЛИЧЕСКОЙ АКТИВНОСТИ ЗА СЧЁТ КОМПАРТМЕНТАЛИЗАЦИИ ФЕРМЕНТОВ И ИХ ВЗАИМОДЕЙСТВИЯ С КЛЕТОЧНЫМИ МЕМБРАНАМИ
Источник
КОВАЛЕНТНАЯ МОДИФИКАЦИЯ ФЕРМЕНТОВ И ЕЕ ТИПЫ



Ковалентная модификация ферментов – тип регуляции ферментативной активности под действием других ферментов, осуществляющийся за счет присоединения к белковой молекуле небольших химических групп, что вызывает конформационные изменения в молекуле белка, приводящие к изменению определенной геометрии каталитического центра. Является быстрым механизмом регуляции активности ферментов внешними сигналами. Ковалентная модификация является основным механизмом при рецептор-зависимом ответе клеток на внешние воздействия, тогда как аллостерические эффекторы изменяют активность ферментов в ответ на изменение внутриклеточных условий.
Фосфорилирование – наиболее распространенный тип ковалентной модификации, является АТФ-зависимым процессом и осуществляется с помощью ферментов протеинкиназ. В большинстве случаев фосфорилированная форма фермента более активна, чем нефосфорилированная. Фосфорилирование модифицирует белки добавлением отрицательно заряженных остатков фосфорной кислоты к гидроксильным группам остатков серина, треонина и, реже, тирозина.
Рис. 4.3.1. Фосфорилирование/дефосфорилирование.
Возвращение фермента в исходное состояние осуществляется ферментами протеинфосфатазами, которые отщепляют неорганический фосфат от молекулы белка.
В некоторых случаях фосфорилирующие и дефосфорилирующие белки сами являются модифицируемыми ферментами. Активность протеинкиназ и протеинфосфатаз находится под гормональным контролем и регулируется нервной системой.
К ковалентной модификации ферментов помимо фосфорилирования относятся также аденилирование, уридилирование, ацетилирование, АДФ-рибозилирование.
Ковалентную модификацию аденилированием и уридилированием можно рассмотреть на примере регуляции активности фермента глутаминсинтетазы. Глутаминсинтетаза выполняет одну из ключевых функций в обмене азота у бактерий E. Coli. При выращивании Е. coli на среде, в которой источником азота служит не NH4 + , а другие соединения, в клетках наблюдается высокий уровень глутаминсинтетазной активности. Добавление в ростовую среду солей NH4 + вызывает быстрое (в течение минуты) десятикратное снижение активности фермента, которое нельзя объяснить подавлением его синтеза. Попытки объяснить данное явление привели к открытию фермента, катализирующего инактивацию глутаминсинтетазы in vitro в присутствии АТФ, Mg 2+ и глутамина. Далее было установлено, что разные формы фермента содержат различные количества ковалентно связанной АМФ. Далее было установлено, что инактивирующий белок является аденилилтрансферазой, катализирующей ковалентное присоединение АМФ к определенной тирозильной группе в каждой из 12 субъединиц глутаминсинтетазы. Однако полное превращение происходит только в экстремальных условиях, например когда клетки, выращенные в условиях недостатка NH4 + , попадают в среду, богатую этим соединением. Обычно глутаминсинтетаза находится в промежуточных состояниях аденилирования, в которых аденилированными являются лишь некоторые из 12 субъединиц.
Активность отдельной субъединицы в составе олигомера зависит от состояния соседних субъединиц (аденилированы они или не аденилированы), вероятно, из-за аллостерического влияния, которое передается через межсубъединичные контакты.
При переносе Е. coli из среды, богатой NH4 + , в бедную этим соединением среду происходит быстрая реактивация глутаминсинтетазы, что указывает на обратимость процесса аденилирования. Было установлено, что активность аденилилтрансферазой регулируется с помощью уридилирования и деуридилирования. Уридилирование происходит в результате катализируемого специфичной уридилилтрансферазой ковалентного присоединения УМФ к одному или двум тирозильмым остаткам каждой субъединицы аденилилтрансферазы. Деуридилирование катализируется уридилил-отщепляющим ферментом. Уридилирующий и деуридилирующий ферменты образованы одним полипептидом, который, подобно аденилилтрансферазе, проявляет бифункциональные свойства.
Примером ковалентной модификации белков с помощью ацетилирования является модификация гистонов. Ацетилирование гистонов играет важную роль в модуляции структуры хроматина при активации транскрипции, увеличивая доступность хроматина для транскрипционного аппарата. Гистоны целенаправленно модифицируются на тех промоторах, которые требуется активировать. Ацетилированию и деацетилированию подвергаются определенные остатки лизина, что осуществляется с помощью ферментов ацетилтрансфераз и деацетилаз. Предполагается, что ацетилированные гистоны менее прочно связаны с ДНК и поэтому ацетилирование может облегчать доступ и связывание факторов транскрипции с их элементами узнавания на ДНК. Ацетилирование остатков лизина в N-концевых «хвостиках» гистонов H2A, H2B, H3 и H4 нейтрализует их положительный заряд и соответственно блокирует ассоциацию с витками нуклеосомной ДНК. Это, в свою очередь, декомпактизует структуру как самой нуклеосомы, так и хроматина в целом и освобождает внешнюю поверхность витков ДНК для взаимодействий с регуляторными факторами.

Еще одним способом химической модификации ферментов с помощью присоединения небольших химических групп является АДФ-рибозилирование. АДФ-рибоза может вызывать неэнзиматическое АДФ-рибозилирование ряда белков. К ним относятсябелки регулирующие репарацию ДНК, белки-регуляторы трансляции и агрегации тромбоцитов. Моно-АДФ-рибозилирование – посттрансляционный процесс модификации белков, ответственный за токсический эффект некоторых бактериальных токсинов. Действие коклюшного или холерного токсинов вызывает моно-АДФ-рибозилирование белков плазматической мембраны и может изменять работу сигнальных систем или активность мембранного транспорта в результате нарушения функционирования G-белков. Схематически действие холерного токсина можно описать следующим образом (Рис. 4.3.2). В норме ГТФ, связанный с Gsα быстро гидролизуется (синяя стрелочка), так, что активация аденилатциклазы и увеличение цАМФ происходит столь долго, сколько гормон связан с рецептором. В присутствии холерного токсина Gsα необратимо модифицируется АДФ- рибозилированием, так, что она может связывать ГТФ, но не может его гидролизовать (красные стрелочки). В результате постоянной активации происходит нерегулируемый рост уровня цАМФ.
Рис. 4.3.2. Механизм действия холерного токсина
При нормальных условиях АДФ-рибозилированию могут подвергаться актин, десмин, интегрин-α-7.
Рис. 4.3.3. АДФ-рибоза
Аденилатциклаза
Аденилатциклаза (АТФ -пирофосфатлиаза циклизирующая) фермент, класса лиаз, катализирует гидролиз АТФ с образованием цАМФ и пирофосфата.
Рис. 4.3.4. структура цАМФ
Аденилатциклаза обнаружена практически во всех тканях животных, а также у бактерий. В клетках животных он локализован в плазматических мембранах, у бактерий – в мембранах и цитоплазме. Наиболее существенная роль цАМФ состоит в активации цАМФ – зависимых протеинкиназ (протеинкиназы А).
Рис. 4.3.5. Первичная структура аденилатциклазы
Рис. 4.3.6. Расположение аденилатциклазы в мембране
Фосфолипаза С
Фосфолипаза С является ключевым ферментом фосфоинозитидной мессенджерной системы. Многочисленные внеклеточные сигнальные молекулы (гормоны, нейромедиаторы, факторы роста, иммуноглобулины, антигены и др.), при взаимодействии со своими рецепторами вызывают активацию фосфолипазы С (ФЛC). При взаимодействии лиганда с рецептором активурующий ФЛC сигнал может передаваться специальным G-белком (Gq). Активированная ФЛC катализирует расщепление мембранного фосфолипида фосфатидилинозитол-4,5-дифосфата (ФИФ2) на инозитолтрифосфат (ИФ3) и диацилглицерол (ДАГ). Диацилглицерол связывается и стимулирует протеинкиназу С (ПKC), ИФ3 взаимодействует с активируемым им Са 2+ каналом (ИФ3 рецептором), в результате чего происходит выход ионов кальция из эндоплазматического ретикулума, которые участвуют в активации Са 2+ — кальмодулин-зависимых протеинкиназ, протеинкиназы С и многочисленных кальций-чувствительных белков. Таким образом, в отличие от других ферментов, катализирующих образование вторичных мессенджеров, ФЛС использует компоненты самой мембраны.
Рис. 4.3.7. Действие фосфолипазы С на фосфатидилинозитол-4,5-дифосфат
Протеинкиназы, типы
Протеинкиназами называют ферменты, катализирующие перенос фосфата от АТФ к специфическому аминокислотному остатку (серину, треонину, тирозину и т.д.). Протеинкиназы эукариот представляют собой суперсемейство гомологичных белков. Важнейшими представителями этого семейства являются серин-треониновые протеинкиназы и тирозиновые протеинкиназы.
Источник
Ковалентная модификация белков как способ регуляции их биологической активности
• Под аллостерической регуляцией понимают способность молекулы связываться с белком-мишенью нековалентной связью и изменять его конформацию
• Регуляция активности белка часто осуществляется за счет модификации его химической структуры
В системе передачи сигналов используется почти любой механизм регуляции активности внутриклеточных белков, однако в большинстве случаев реализуется механизм аллостерической или ковалентной регуляции. Реакция индивидуальных белков на сигналы, вызывающие их аллостерические и ковалентные модификации, носит типичный характер.
Под аллостерической регуляцией понимают способность молекулы связываться с белком-мишенью нековалентной связью и изменять его конформацию.
Поскольку активность белка отражает его конформацию, связывание любой молекулы, влияющей на конформацию, приводит к изменению активности белка-мишени. Любая молекула может проявлять аллостерический эффект: протоны и ионы Са2+, небольшие органические молекулы или другие белки. Аллостерическая регуляция может оказывать на активность белка стимулирующий или ингибирующий эффект.
Активность белка часто регулируется за счет ковалентной модификацией его химической струтуры. Изменение химической структуры белка меняет его конформацию, и, следовательно, активность. Большинство ковалентных модификаций, носящих регуляторный характер, являются обратимыми.
Наиболее распространенной, классической регуляторной ковалентной модификацией является фосфорилирование, при котором фосфатная группа переносится от АТФ обычно на гидроксильную группу серина (Ser), треонина (Thr) или тирозина (Tyr). Ферменты, фосфорилирующие белки, называются протеинкиназы. Им противостоят фосфопротеинфосфатазы, которые катализируют реакцию гидролиза фосфатных групп. При этом образуется свободный фосфат и восстанавливается гидроксильная группа аминокислоты.
Известны также другие формы ковалентной модификации белков, которые будут рассмотрены в отдельных статьях на сайте (рекомендуем пользоваться формой поиска на главной странице сайта).
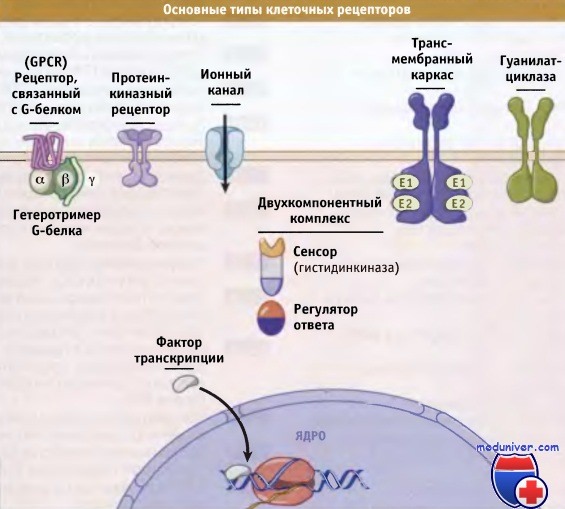
которые характеризуются общими механизмами действия и общностью структуры.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник