Конденсационные методы получения дисперсных систем
Методы конденсации по сравнению с методами диспергирования дают возможность получать коллоидные системы более высокой дисперсности. Кроме того, они обычно не связаны с применением специальных машин.
Конденсационные методы получения дисперсных систем основаны на создании условий, при которых будущая дисперсионная среда пересыщается веществом будущей дисперсной фазы. В зависимости от способов создания этих условий конденсационный метод подразделяют на физический и химический.
К физической конденсации относятся:
а) Конденсация паров при пропускании их через холодную жидкость, в результате чего образуются лиозоли. Так, при пропускании паров кипящей ртути, серы, селена в холодную воду образуются их коллоидные растворы.
б) Замена растворителя. Метод основан на том, что вещество, из которого хотят получить золь, растворяют в подходящем растворителе, затем добавляют вторую жидкость, являющуюся плохим растворителем для вещества, но хорошо смешивающуюся с исходным растворителем. Растворенное первоначально вещество выделяется из раствора в высокодисперсном состоянии. Например, таким путем можно получить гидрозоли серы, фосфора, канифоли, парафина и многих других органических веществ, вливая их спиртовый раствор в воду.
Химическая конденсация отличается от всех рассмотренных выше методов тем, что диспергируемое вещество берут не в готовом виде, а получают непосредственно в растворе химической реакцией, в результате которой образуется нерастворимое в данной среде нужное соединение. Задача сводится к тому, чтобы получить выпадающий осадок в мелкодисперсном состоянии. При сливании растворов необходимо добиться таких условий, чтобы возникло много центров кристаллизации, тогда образующиеся кристаллики будут очень маленького размера. Оптимальные условия получения золей (концентрация растворов, порядок сливания, скорость сливания, соотношение компонентов, температура) обычно находят опытным путем.
В методах химической конденсации используются любые реакции, ведущие к образованию новой фазы: реакция двойного обмена, разложения, окисления-восстановления и т.д. Можно использовать электрохимические реакции, например, восстановление металлов электролизом.
Ниже приведены некоторые примеры синтеза коллоидных систем с использованием различных реакций. Стабилизатором коллоидного раствора служит обычно один из участников реакции или побочный продукт, из которых на границе раздела частица – среда образуются адсорбционные слои ионного или молекулярного типа, препятствующие слипанию частиц и выпадению их в осадок.
При взаимодействии газообразных NH3 и HCl образуется аэрозоль (дым) твердого хлорида аммония (реакция соединения):
Реакцией тиосульфата натрия с серной кислотой можно получить гидрозоль серы (реакция окисления-восстановления):
Многие золи можно синтезировать с помощью реакций обмена:
Полученные золи загрязнены примесями низкомолекулярных веществ.
Очистка дисперсных систем
Для очистки дисперсных систем от растворенных низкомолекулярных веществ Грэм предложил воспользоваться способностью мелкопористых пленок (мембран) задерживать частицы дисперсной фазы и свободно пропускать ионы и молекулы. Этот способ назван диализом.
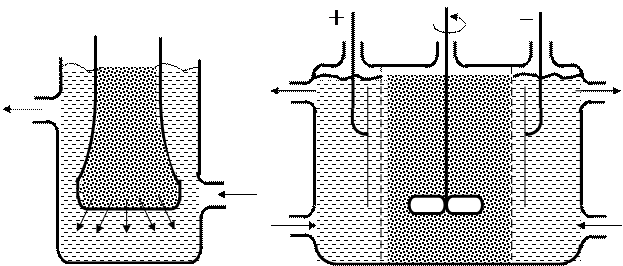
Очищаемую дисперсную систему помещают в сосуд, изготовленный из мелкопористого материала, или имеющий мелкопористое дно (рис. 9.33 а). Сосуд омывается проточной водой (дистиллированной). Согласно законам диффузии, ионы и молекулы растворенного вещества, содержащиеся в дисперсной системе в виде примесей, проникают через поры мембраны в дистиллированную воду, а частицы дисперсной фазы задерживаются и остаются в дисперсной системе.
Рис. 9.33. Схемы диализатора (а) и электродиализатора (б)
Скорость диализа очень мала, но ее можно значительно увеличить (в 10-20 раз), воспользовавшись действием электрического поля на ионы растворенной примеси. Такой метод очистки дисперсных систем от примесей электролитов называют электродиализом.

Электродиализатор (рис.9.33. б) — это сосуд, разделенный мембранами на три отсека, из которых средний заполняют очищаемой дисперсной системой, а в крайних размещены электроды; через эти же отсеки циркулирует жидкость, однородная с веществом дисперсионной среды очищаемой системы. При наложении на электроды достаточной разности потенциалов ( несколько сот вольт) дисперсная система относительно быстро очищается от электролита.
В настоящее время диализ используют во многих производствах. Особенно эффективен он в медицине. Например, на принципе электролиза основано действие аппарата «искусственная почка», позволяющего очищать кровь больного от вредных продуктов жизнедеятельности организма.
Ультрафильтрация – метод очистки золей путем продавливания дисперсионной среды с низкомолекулярными примесями через ультрафильтры. Ультрафильтры – это мембраны с таким размером пор, через которые проходят примеси и растворитель, но не проходят частицы золя (или высокомолекулярных соединений).
В мешочек, изготовленный из ультрафильтра, наливают очищаемый золь и под давлением продавливают его через мембрану. Дисперсионную среду обновляют, добавляя к золю чистый растворитель. В мешочке остается чистый золь.
Таким образом, для получения дисперсных систем используют как методы измельчения крупных частиц (диспергирование), так и методы, основанные на объединении молекулярных частиц до размеров коллоидных (конденсация). Диспергационные методы позволяют получать грубодисперсные системы с крупными размерами частиц. Конденсационные методы позволяют получать высокодисперсные золи. Очистку дисперсных систем от низкомолекулярных примесей осуществляют с помощью мелкопористых фильтров – мембран.
Источник
Конденсационные методы



Дисперсные системы
Дисперсными называют системы, в которых одно вещество (дисперсная фаза) равномерно распределено в другом веществе (дисперсионная среда).
Классификация дисперсных систем
По размеру частиц дисперсной фазы(d)дисперсные системы делятся на грубодисперсные, коллоидные и истинные растворы.
| Грубодисперсные (ГД) | Коллоидные растворы | Истинные растворы |
| d > 10 -7 м | d=10 -7 — 10 -9 м | d -9 м |
| Взвесь глины, мела в воде, эмульсия жира в молоке | Вирусы, гемоглобин крови, нервные клетки, протоплазма | Растворы солей, кислот, оснований, глюкозы |
Классификация коллоидных растворов
1. По агрегатному состоянию фаз
| Агрегатное состояние дисперсионной среды и тип системы | Агрегатное состояние дисперсной фазы условное обозначение | Название системы | Пример |
| Жидкость Лиозоли | Твердое Т/Ж Жидкость Ж/Ж Газ Г/Ж | Золи, суспензии Эмульсии Пены | Золи металлов Молоко, смазки Мыльная пена |
| Газ Аэрозоли | Твердое Т/Г Жидкость Ж/Г Газ Г/Г | Аэрозоль Аэрозоль – | Дым, пыль Туман, облака – |
| Твердое Солидозоли | Твердое Т/Т Жидкость Ж/Т Газ Г/Т | – Твердые эмульсии Твердые пены | Сплавы Почва, жемчуг Пемза, уголь активированный |
2. По характеру взаимодействия фазы и средысистемы бывают лиофобными и лиофильными, если дисперсионная среда – вода, то соответственно – гидрофобными и гидрофильными.
В лиофобных системах частицы фазы слабо взаимодействуют или не взаимодействуют со средой. Эти системы необратимы и термодинамически неустойчивы. Примеры: гидрозоли серебра, золота, хлорида серебра AgCl.
В лиофильных системах взаимодействие частиц фазы со средой достаточно сильное, т.е. частицы фазы сильно сольватированы (гидратированы). Такие системы являются термодинамически устойчивыми и обратимыми (восстанавливаются при добавлении растворителя после его испарения). Примеры: растворы белков, полисахаридов, нуклеиновых кислот в воде.
2.2. Методы получения
коллоидных растворов
Коллоидные растворы (золи) можно получить:
1) из грубодисперсных систем путем диспергирования (измельчения)частиц дисперсной фазы – это диспергационныеметоды;
2) из истинных растворов путем конденсации (укрупнения)частиц – конденсационныеметоды.
Методы диспергирования
1. Механическое дробление в шаровых и коллоидных мельницах.
2. Измельчение под действием ультразвука.
3. Электрическое диспергирование.
Перечисленные методы используются для получения золей металлов, полимеров (крахмала, каучука, нитроцеллюлозы), при производстве лекарственных препаратов, краски, цемента и т.д.
4. Пептизация – перевод свежеполученного осадка в золь под действием пептизатора-стабилизатора.
Пример: расщепление сложных белков на более простые под действием пепсина, получение гидрозоля из осадка Fe(OH)3 под действием пептизатора FeCl3.
Конденсационные методы
1.Физическая конденсация заключается в замене растворителя (дисперсионной среды).
Пример: раствор NaCl в воде – истинный раствор, в бензоле – коллоидный раствор.
См. опыт 1, стр. 45. Получение золя канифоли.
2. Химическая конденсация – получение золей в химической реакции (гидролиза, окислительно-восстановительной, обменной) при следующих условиях:
1) образование труднорастворимого вещества;
2) наличие стабилизатора (избыток одного из реагентов, ПАВ);
3) малые концентрации растворов (для получения d частиц 10 -7 -10 -9 м).
2.3. Методы очистки
коллоидных растворов
От грубодисперсных частиц очищают путем фильтрации. Коллоидные растворы проходят через фильтр, крупные частицы задерживаются.
От низкомолекулярныхпримесей коллоиды очищают методами диализа, электродиализа, ультрафильтрации, компенсационного диализа.
Диализ основан на свойстве полупроницаемых мембран задерживать коллоидные частицы и пропускать молекулы или ионы низкомолекулярных веществ в растворитель, циркулирующий в диализаторе.
Электродиализ – это ускоренный диализ под действием электрического тока (продолжительность диализа – недели, месяцы, электродиализа – минуты, часы).

Ультрафильтрация – это диализ под давлением или при разрежении. Этот метод широко используют для очистки воды, белков, нуклеиновых кислот, витаминов, для определения размеров вирусов.
Компенсационный диализ или вивидиализ – это очистка от части низкомолекулярных примесей. В диализаторе растворитель заменяется раствором низкомолекулярного вещества, которое необходимо оставить в коллоидном растворе.
Вивидиализ применяется для количественного определения веществ в биологических жидкостях. Например, содержание сахара в крови определяется диализом сыворотки крови по сравнению с физиологическим раствором, к которому добавляют различные количества сахара. Концентрация сахара во внешнем растворе не изменяется лишь в том случае, когда она равна концентрации свободного сахара в крови.
По принципу компенсационного диализа работает аппарат «искусственная почка» (АИП), применяемый при острых отравлениях, обширных ожогах, токсикозах для очистки крови (гемодиализа) от шлаков: мочевины, мочевой кислоты, билирубина и т.д. Внешним диализирующим раствором является физиологический раствор (0,85% NaCl).
2.4. Молекулярно-кинетические
свойства коллоидных растворов
Броуновское движение – хаотическое тепловое движение коллоидных частиц вследствие ударов о них молекул растворителя.
Интенсивность броуновского движения оценивается средним квадратичным проекции смещения частицы 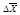

где КБ – константа Больцмана (1,38×10 -23 Дж/К), t – время (с), Т – температура (К), r – радиус частицы (м), h – вязкость среды (Н×с/м 2 ).
Благодаря броуновскому движению коллоидные частицы находятся во взвешенном состоянии, коллоидный раствор обладает кинетической устойчивостью.
Диффузия – самопроизвольный процесс выравнивания концентрации частиц во всем объеме раствора. Cкорость диффузии увеличивается с повышением температуры и уменьшением размера частиц и вязкости среды:

где D – коэффициент диффузии (м 2 /с), КБ – константа Больцмана (1,38×10 -23 Дж/К), Т – температура, r – радиус частицы (м), h – вязкость среды (Н×с/м 2 ).
Осмотическое давление коллоидных растворов подчиняется закону Вант-Гоффа:
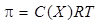


где n – число частиц в единице объема, NA – число Авогадро (6,02 ×10 23 молекул).
Из-за большого размера и малой концентрации коллоидных частиц осмотическое давление коллоидных растворов значительно меньше осмотического давления истинных растворов.
Седиментационное равновесие – это протекание противоположных процессов: диффузии и седиментации. Седиментация – оседание частиц под действием силы тяжести. По закону Стокса на частицу действуют сила тяжести и сила трения:
При оседании с постоянной скоростью Fтрения = Fтяжести. Из уравнения Стокса cледует, что скорость седиментации (u) прямо пропорциональна размеру частиц, разности плотностей дисперсной фазы и дисперсионной среды и обратно пропорциональна вязкости раствора.

где U – скорость седиментации (м/с), r – радиус сферической частицы дисперсной фазы (м), r и r0 –плотность дисперсной фазы и среды соответственно (кг/м 3 ), g – ускорение силы тяжести (9,8 м/с 2 ), h – вязкость (Н ×с/м 2 ).
Определение скорости седиментации лежит в основе седиментационного анализа, который используется:
1) для определения скорости оседания эритроцитов СОЭ (в норме у женщин – 3-12 мм/ч, у мужчин – 2-6 мм/ч);
2) для разделения на фракции центрифугированием компонентов клетки, крови, костного мозга;
3) для выделения белков, ДНК, вирусов.
2.5. Оптические свойства
коллоидных растворов
Оптические свойства коллоидных растворов существенно отличаются от свойств истинных растворов.
Размеры коллоидной частицы соизмеримы с длиной волны падающего света 2r » l. Частица становится вторичным источником света, в коллоидах наблюдается дифракционное рассеяние света. Визуально наблюдается опалесценция – различная окраска золей в проходящем свете (напротив источника света) и в рассеянном свете (сбоку). Это явление было обнаружено Фарадеем и Тиндалем:
При боковом освещении коллоидного раствора хорошо виден светящийся конус Тиндаля.
Интенсивность светорассеяния количественно выражается уравнением Рэлея

где I, I0 – интенсивность рассеянного и падающего света (Вт/м 2 ), КР – константа Рэлея, n – число частиц в 1 м 3 , V –объем частицы (м 3 ), l – длина волны падающего света (м).
Из уравнения Рэлея следует, что I рассеянного света обратно пропорциональна l 4 (I
1/l 4 ), следовательно, сильнее всего рассеиваются волны синей и фиолетовой части спектра (окраска золя в рассеянном свете). Незначительное рассеивание красного и желтого цветов объясняет окраску коллоидного раствора в проходящем свете.
Явление светорассеяния лежит в основе работы ультрамикроскопа, применяемого для определения размеров частиц плазмы, сыворотки крови, лимфы, вакцин и для контроля чистоты инъекционных растворов.
Строение мицеллы
Мицелла – это сложная коллоидная частица. Основой мицеллы является электронейтральный агрегат – совокупность атомов или молекул труднорастворимого вещества.
Коллоидная частица образуется только при избытке одного из реагентов, т.е. в присутствии стабилизатора. На поверхности агрегата избирательно адсорбируются потенциалопределяющие ионы (ПОИ) по правилу Панета – Фаянса (в данном случае – ионы I — ), в результате чего агрегат приобретает заряд. Агрегат и ПОИ образуют ядро мицеллы.
С заряженной поверхностью ядра устойчиво связано некоторое количество ионов противоположного знака – противоионов (в данном примере – ионы К + ). ПОИ и часть противоионов формируют адсорбционный слой. Агрегат вместе с адсорбционным слоем называют гранулой.
Знак заряда гранулы определяется знаком потенциалопределяющих ионов (ПОИ). Заряд гранулы компенсируют остальные противоионы, образующие подвижный диффузный слой. Диффузный слой насыщен молекулами растворителя.
Источник