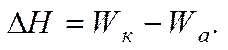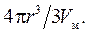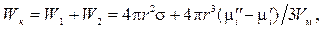Конденсационные методы получения дисперсных систем
Методы конденсации по сравнению с методами диспергирования дают возможность получать коллоидные системы более высокой дисперсности. Кроме того, они обычно не связаны с применением специальных машин.
Конденсационные методы получения дисперсных систем основаны на создании условий, при которых будущая дисперсионная среда пересыщается веществом будущей дисперсной фазы. В зависимости от способов создания этих условий конденсационный метод подразделяют на физический и химический.
К физической конденсации относятся:
а) Конденсация паров при пропускании их через холодную жидкость, в результате чего образуются лиозоли. Так, при пропускании паров кипящей ртути, серы, селена в холодную воду образуются их коллоидные растворы.
б) Замена растворителя. Метод основан на том, что вещество, из которого хотят получить золь, растворяют в подходящем растворителе, затем добавляют вторую жидкость, являющуюся плохим растворителем для вещества, но хорошо смешивающуюся с исходным растворителем. Растворенное первоначально вещество выделяется из раствора в высокодисперсном состоянии. Например, таким путем можно получить гидрозоли серы, фосфора, канифоли, парафина и многих других органических веществ, вливая их спиртовый раствор в воду.
Химическая конденсация отличается от всех рассмотренных выше методов тем, что диспергируемое вещество берут не в готовом виде, а получают непосредственно в растворе химической реакцией, в результате которой образуется нерастворимое в данной среде нужное соединение. Задача сводится к тому, чтобы получить выпадающий осадок в мелкодисперсном состоянии. При сливании растворов необходимо добиться таких условий, чтобы возникло много центров кристаллизации, тогда образующиеся кристаллики будут очень маленького размера. Оптимальные условия получения золей (концентрация растворов, порядок сливания, скорость сливания, соотношение компонентов, температура) обычно находят опытным путем.
В методах химической конденсации используются любые реакции, ведущие к образованию новой фазы: реакция двойного обмена, разложения, окисления-восстановления и т.д. Можно использовать электрохимические реакции, например, восстановление металлов электролизом.
Ниже приведены некоторые примеры синтеза коллоидных систем с использованием различных реакций. Стабилизатором коллоидного раствора служит обычно один из участников реакции или побочный продукт, из которых на границе раздела частица – среда образуются адсорбционные слои ионного или молекулярного типа, препятствующие слипанию частиц и выпадению их в осадок.
При взаимодействии газообразных NH3 и HCl образуется аэрозоль (дым) твердого хлорида аммония (реакция соединения):
Реакцией тиосульфата натрия с серной кислотой можно получить гидрозоль серы (реакция окисления-восстановления):
Многие золи можно синтезировать с помощью реакций обмена:
Полученные золи загрязнены примесями низкомолекулярных веществ.
Очистка дисперсных систем
Для очистки дисперсных систем от растворенных низкомолекулярных веществ Грэм предложил воспользоваться способностью мелкопористых пленок (мембран) задерживать частицы дисперсной фазы и свободно пропускать ионы и молекулы. Этот способ назван диализом.
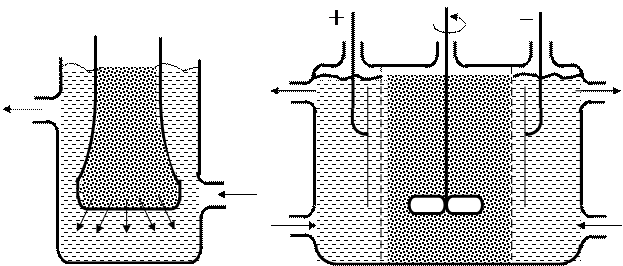
Очищаемую дисперсную систему помещают в сосуд, изготовленный из мелкопористого материала, или имеющий мелкопористое дно (рис. 9.33 а). Сосуд омывается проточной водой (дистиллированной). Согласно законам диффузии, ионы и молекулы растворенного вещества, содержащиеся в дисперсной системе в виде примесей, проникают через поры мембраны в дистиллированную воду, а частицы дисперсной фазы задерживаются и остаются в дисперсной системе.
Рис. 9.33. Схемы диализатора (а) и электродиализатора (б)
Скорость диализа очень мала, но ее можно значительно увеличить (в 10-20 раз), воспользовавшись действием электрического поля на ионы растворенной примеси. Такой метод очистки дисперсных систем от примесей электролитов называют электродиализом.

Электродиализатор (рис.9.33. б) — это сосуд, разделенный мембранами на три отсека, из которых средний заполняют очищаемой дисперсной системой, а в крайних размещены электроды; через эти же отсеки циркулирует жидкость, однородная с веществом дисперсионной среды очищаемой системы. При наложении на электроды достаточной разности потенциалов ( несколько сот вольт) дисперсная система относительно быстро очищается от электролита.
В настоящее время диализ используют во многих производствах. Особенно эффективен он в медицине. Например, на принципе электролиза основано действие аппарата «искусственная почка», позволяющего очищать кровь больного от вредных продуктов жизнедеятельности организма.
Ультрафильтрация – метод очистки золей путем продавливания дисперсионной среды с низкомолекулярными примесями через ультрафильтры. Ультрафильтры – это мембраны с таким размером пор, через которые проходят примеси и растворитель, но не проходят частицы золя (или высокомолекулярных соединений).
В мешочек, изготовленный из ультрафильтра, наливают очищаемый золь и под давлением продавливают его через мембрану. Дисперсионную среду обновляют, добавляя к золю чистый растворитель. В мешочке остается чистый золь.
Таким образом, для получения дисперсных систем используют как методы измельчения крупных частиц (диспергирование), так и методы, основанные на объединении молекулярных частиц до размеров коллоидных (конденсация). Диспергационные методы позволяют получать грубодисперсные системы с крупными размерами частиц. Конденсационные методы позволяют получать высокодисперсные золи. Очистку дисперсных систем от низкомолекулярных примесей осуществляют с помощью мелкопористых фильтров – мембран.
Источник
Методы получения ДИСПЕРСНЫХ СИСТЕМ



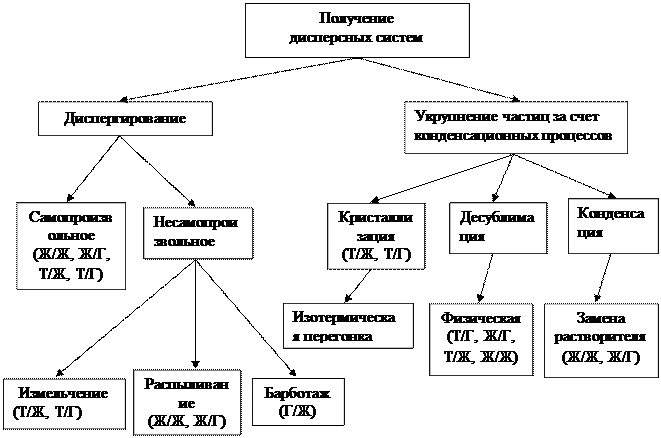
Методы получения коллоидных растворов также можно разделить на две группы: методы конденсации и диспергирования (в отдельную группу выделяется метод пептизации, который будет рассмотрен позднее). Еще одним необходимым для получения золей условием, помимо доведения размеров частиц до коллоидных, является наличие в системе стабилизаторов – веществ, препятствующих процессу самопроизвольного укрупнения коллоидных частиц.
Рис. Классификация способов получения дисперсных систем (в скобках указан вид систем)
Дисперсионные методы
Дисперсионные методы основаны на раздроблении твердых тел до частиц коллоидного размера и образовании таким образом коллоидных растворов. Процесс диспергирования осуществляется различными методами: механическим размалыванием вещества в т.н. коллоидных мельницах, электродуговым распылением металлов, дроблением вещества при помощи ультразвука.
Диспергирование может быть самопроизвольное и несамопроизвольное. Самопроизвольное диспергирование характерно для лиофильных систем и связано с ростом беспорядка системы (когда из одного большого куска образуется много мелких частиц). При диспергировании при постоянной температуре рост энтропии должен превышать изменение энтальпии.
В отношении лиофобных систем самопроизвольное диспергирование исключено, поэтому диспергирование возможно лишь путем затраты определенной работы или эквивалентного количества теплоты, которое измеряется, в частности, энтальпией.
Изменение энтальпии в изобарно-изотермическом процессе определяется соотношением между работой когезии Wки работой адгезии Wа. Энергия (работа) когезии Wкхарактеризует связь внутри тела, а энергия (работа) адгезии Wа — связь его с окружающей средой.
Энергию образования новой поверхности можно выразить через энтальпию, которая имеет вид:
Уравнение показывает изменение энтальпии в результате диспергирования. Для лиофильных систем, способных к самопроизвольному диспергированию, когда ΔS > 0, из условия следует, что ΔH 0) соответствуют увеличению энергии Гиббса:
Процесс диспергирования в этом случае является типично несамопроизвольным и осуществляется за счет внешней энергии.
Диспергирование характеризуется степенью диспергирования. Она определяется отношением размеров исходного продукта и частиц дисперсной фазы полученной системы. Степень диспергирования можно выразить следующим образом:
где dн; dк; Bн; Bк; Vн; Vк — соответственно диаметр, площадь пoвepxнocти, объем частиц до и после диспергирования.
Таким образом, степень диспергирования может быть выражена в единицах размера (α1), площади поверхности (α2) или объема (α3) частиц дисперсной фазы, т.е. может быть линейной, поверхностной или объемной.
Работа W, необходимая для диспергирования твердого тела или жидкости, затрачивается на деформирование тела Wди на образование новой поверхности раздела фаз Wа, которая измеряется работой адгезии. Деформирование является необходимой предпосылкой разрушения тела. Согласно П.А. Ребиндеру работа диспергирования определяется по формуле
где σ* — величина, пропорциональная или равная поверхностному натяжению на границе раздела между дисперсной фазой и дисперсионной средой; ΔB — увеличение поверхности раздела фаз в результате диспергирования; V — объем исходного тела до диспергирования; к — коэффициент, эквивалентный работе деформирования единицы объема тела.
Методы конденсации
К конденсационным методам получения дисперсных систем относятся конденсация, десублимация и кристаллизация. Они основаны на образовании новой фазы в условиях пересыщенного состояния вещества в газовой или жидкой среде. При этом система из гомогенной переходит в гетерогенную. Конденсация и десублимация характерны для газовой, а кристаллизация — для жидкой среды.

Необходимым условием конденсации и кристаллизации является пересыщение и неравномерное распределение вещества в дисперсионной среде (флуктуация концентрации), а также образование центров конденсации или зародышей.
Степень пересыщения β для раствора и пара можно выразить следующим образом:
где р, с — давление пересыщенного пара и концентрация вещества в пересыщенном растворе; рs— равновесное давление насыщенного пара над плоской поверхностью; сs— равновесная концентрация, соответствующая образованию новой фазы.
Для осуществления кристаллизации охлаждают раствор или газовую смесь.
В основе конденсационных методов получение дисперсных систем лежат процессы кристаллизации, десублимации и конденсации, которые вызваны уменьшением энергии Гиббса (ΔG 2 σ,
где 4πr 2 — поверхность сферических частиц радиусом r.
Химический потенциал изменяется следующим образом:
где μi / и μi // — химические потенциалы гомо и гетерогенных систем (при переходе от мелких капель к крупным).
Изменение химического потенциала характеризует перенос определенного числа молей вещества из одной фазы в другую; это число n молей равно объему частицы 4πr 3 /3, деленному на мольный объем Vм:
Работа образования новой поверхности в процессе конденсации Wк равна:
где W1и W2 — соответственно работа, затрачиваемая на образование поверхности частиц, и работа на перенос вещества из гомогенной среды в гетерогенную.
Образование дисперсных систем может происходить в результате физической и химической конденсации, а также при замене растворителя.
Физическая конденсация осуществляется при понижении температуры газовой среды, содержащей пары различных веществ. При выполнении необходимых условий образуются частицы или капли дисперсной фазы. Подобный процесс имеет место не только в объеме газа, но и на охлажденной твердой поверхности, которую помещают в более теплую газовую среду.
Конденсация определяется разностью химических потенциалов (μi // – μi / )
Источник
Методы получения дисперсных систем
Цель работы: ознакомиться с различными методами получения дисперсных систем.
Краткое теоретическое введение.
Способы получения дисперсных систем можно разделить на две группы: методы диспергирования и методы конденсации.
Методы диспергирования основаны на дроблении крупных кусков вещества до требуемой степени дисперсности. Эти методы чаще применяются для получения суспензий и эмульсий Системы с размерами частиц 10 -6 – 10 -7 см получают методами конденсации. Методы конденсации представляют собой объединение молекул или ионов до размеров коллоидных частиц, следствием чего является возникновение границы раздела фаз.
Для получения дисперсных систем любым из этих методов необходимо выполнение следующих условий:
а) нерастворимость или ограниченная растворимость дисперсной фазы в дисперсионной среде;
б) наличие в системе стабилизатора, который должен обеспечить устойчивость взвешенных частиц и приостановить их рост.
Затрачивая работу против молекулярных сил сцепления, можно различными способами достичь нужной степени дисперсности.
1. Механическое диспергирование.
Способ заключается в энергичном и продолжительном растирании, размалывании или распыливании вещества дисперсной фазы и смешивании его с жидкостью, которая служит дисперсионной средой. Крупные частицы дробят, пользуясь ступками, коллоидными мельницами, краскотёрками. Способом механического диспергирования получают фармацевтические препараты, смазочные материалы, пищевые продукты.
2. Диспергирование ультразвуком.
В основе метода лежит использование ультразвуковых колебаний (более 20000 колебаний в секунду). Диспергирование при помощи ультразвука эффективно лишь для веществ, имеющих небольшую прочность: сера, графит, краски, крахмал, каучук, желатин. Очень легко получаются этим методом эмульсии, например, эмульсии какао, высококачественные кремы и др.
В основе конденсационных методов лежат процессы образования частиц дисперсной фазы из веществ, находящихся в молекулярном или ионном состоянии. Процессы эти могут носить как физический, так и химический характер.
1. Метод замены растворителя.
Сущность метода заключается в том, что растворитель, в котором вещество растворяется, образуя истинный раствор, заменяется растворителем, в котором это вещество нерастворимо. Например, если спиртовой раствор серы, фосфора или канифоли влить в воду, то раствор становится насыщенным, происходит конденсация, и образуются частицы дисперсной фазы. Это происходит потому, что указанные вещества плохо растворяются в водно-спиртовой смеси.
2. Конденсация при охлаждении пара.
Наиболее наглядный пример конденсации из паров – образование тумана или дыма. Другим примером возникновения коллоидных частиц в результате конденсации пара можно назвать камеру Вильсона, используемую в ядерной физике.
Получение дисперсных систем методами химической конденсации сводится к образованию молекул нерастворимых веществ в результате химической реакции с последующим укрупнением их до размеров коллоидных частиц. Химические конденсационные методы классифицируются в зависимости от типа химической реакции, лежащей в основе получения золя. К числу реакций, в результате которых при соответствующих условиях могут образовываться вещества в коллоидном состоянии, относятся реакции окисления, восстановления, обмена, гидролиза.
Пример окислительной реакции – окисление сероводорода в водной среде:
Примером такой реакции является образование золя сульфида мышьяка (III):
3. Реакции гидролиза.
Гидролиз чаще всего используется для получения золей гидроксидов металлов:
Пептизацией называется процесс перехода в коллоидный раствор осадков, образовавшихся при коагуляции. Вызвать пептизацию можно промыванием коагулята растворителем, а также воздействием пептизаторов (электролитов, неэлектролитов, поверхностно-активных веществ, высокомолекулярных соединений). Пептизировать можно только свежеполученные осадки, в которых не прошли явления кристаллизации и частицы не потеряли своей индивидуальности.
Экспериментальная часть.
I. Методы физической конденсации.
Опыт 1. Получение золя серы методом замены растворителя.
В пробирку наливают 10 мл дистиллированной воды, добавляют 5 капель раствора серы в этаноле и энергично перемешивают содержимое пробирки. Образуется прозрачный опалесцирующий золь. Сера растворима в спирте, но нерастворима в воде. При замене спирта водой молекулы растворённого вещества соединяются в агрегаты коллоидных размеров.
Для наблюдения эффекта Фарадея-Тиндаля пробирку с коллоидным раствором помещают на пути луча света проекционного фонаря. Рассматривают пробирку под углом 90 0 к направлению падающего луча.
Источник