- Химическая кинетика
- Описание
- Оглавление
- 1. Скорость химической реакции
- 1.1. Кинетическое уравнение химической реакции. Порядок реакции
- 1.2. Реакции нулевого порядка
- 1.3. Реакции первого порядка
- 1.4. Реакции второго порядка
- 1.5. Методы определения порядка реакции
- 3.2 Кинетическая классификация химических реакций
- 3.2.1 Молекулярность реакции
- 3.2.2 Порядок реакции
Химическая кинетика
| Сайт: | MOODLE — Виртуальная среда обучения КНИТУ (КХТИ) |
| Курс: | Физическая химия |
| Книга: | Химическая кинетика |
| Напечатано:: | Гость |
| Дата: | Четверг, 18 Ноябрь 2021, 05:34 |
Описание
Законы химической термодинамики позволяют определить направление и предел протекания возможного при данных условиях химического процесса, а также его энергетический эффект. Однако термодинамика не может ответить на вопросы о том, как осуществляется данный процесс и с какой скоростью. Эти вопросы – механизм и скорость химической реакции – и являются предметом химической кинетики.
Оглавление
1. Скорость химической реакции
Дадим определение основному понятию химической кинетики – скорости химической реакции:
Скорость химической реакции есть число элементарных актов химической реакции, происходящих в единицу времени в единице объема (для гомогенных реакций) или на единице поверхности (для гетерогенных реакций).
Скорость химической реакции есть изменение концентрации реагирующих веществ в единицу времени.
Первое определение является наиболее строгим; из него следует, что скорость химической реакции можно также выражать как изменение во времени любого параметра состояния системы, зависящего от числа частиц какого-либо реагирующего вещества, отнесенное к единице объема или поверхности – электропроводности, оптической плотности, диэлектрической проницаемости и т.д. и т.п. Однако наиболее часто в химии рассматривается зависимость концентрации реагентов от времени. В случае односторонних (необратимых) химических реакций (здесь и далее рассматриваются только односторонние реакции) очевидно, что концентрации исходных веществ во времени постоянно уменьшаются (ΔСисх 0). Скорость реакции считается положительной, поэтому математически определение средней скорости реакции в интервале времени Δt записывается следующим образом:
В различных интервалах времени средняя скорость химической реакции имеет разные значения; истинная (мгновенная) скорость реакции определяется как производная от концентрации по времени:
Графическое изображение зависимости концентрации реагентов от времени есть кинетическая кривая (рисунок 2.1).
Рис. 2.1 Кинетические кривые для исходных веществ (А) и продуктов реакции (В).
Истинную скорость реакции можно определить графически, проведя касательную к кинетической кривой (рис. 2.2); истинная скорость реакции в данный момент времени равна по абсолютной величине тангенсу угла наклона касательной:
Рис. 2.2 Графическое определение Vист.
Необходимо отметить, что в том случае, если стехиометрические коэффициенты в уравнении химической реакции неодинаковы, величина скорости реакции будет зависеть от того, изменение концентрации какого реагента определялось. Очевидно, что в реакции
концентрации водорода, кислорода и воды изменяются в различной степени:
Скорость химической реакции зависит от множества факторов: природы реагирующих веществ, их концентрации, температуры, природы растворителя и т.д.
Одной из задач, стоящих перед химической кинетикой, является определение состава реакционной смеси (т.е. концентраций всех реагентов) в любой момент времени, для чего необходимо знать зависимость скорости реакции от концентраций. В общем случае, чем больше концентрации реагирующих веществ, тем больше скорость химической реакции. В основе химической кинетики лежит т. н. основной постулат химической кинетики:
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в некоторых степенях.
Т. е. для реакции
аА + bВ + dD + . → еЕ + .
Коэффициент пропорциональности k есть константа скорости химической реакции. Константа скорости численно равна скорости реакции при концентрациях всех реагирующих веществ, равных 1 моль/л.
Зависимость скорости реакции от концентраций реагирующих веществ определяется экспериментально и называется кинетическим уравнением химической реакции. Очевидно, что для того, чтобы записать кинетическое уравнение, необходимо экспериментально определить величину константы скорости и показателей степени при концентрациях реагирующих веществ. Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции (в уравнении (II.4) соответственно x, y и z) есть частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции (x + y + z) представляет собой общий порядок реакции. Следует подчеркнуть, что порядок реакции определяется только из экспериментальных данных и не связан со стехиометрическими коэффициентами при реагентах в уравнении реакции. Стехиометрическое уравнение реакции представляет собой уравнение материального баланса и никоим образом не может определять характера протекания этой реакции во времени.
В химической кинетике принято классифицировать реакции по величине общего порядка реакции. Рассмотрим зависимость концентрации реагирующих веществ от времени для необратимых (односторонних) реакций нулевого, первого и второго порядков.
1.1. Кинетическое уравнение химической реакции. Порядок реакции
Одной из задач, стоящих перед химической кинетикой, является определение состава реакционной смеси (т.е. концентраций всех реагентов) в любой момент времени, для чего необходимо знать зависимость скорости реакции от концентраций. В общем случае, чем больше концентрации реагирующих веществ, тем больше скорость химической реакции. В основе химической кинетики лежит т. н. основной постулат химической кинетики:
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в некоторых степенях.
Т. е. для реакции
аА + bВ + dD + . → еЕ + .
Коэффициент пропорциональности k есть константа скорости химической реакции. Константа скорости численно равна скорости реакции при концентрациях всех реагирующих веществ, равных 1 моль/л.
Зависимость скорости реакции от концентраций реагирующих веществ определяется экспериментально и называется кинетическим уравнением химической реакции. Очевидно, что для того, чтобы записать кинетическое уравнение, необходимо экспериментально определить величину константы скорости и показателей степени при концентрациях реагирующих веществ. Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции (в уравнении (II.4) соответственно x, y и z) есть частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции (x + y + z) представляет собой общий порядок реакции. Следует подчеркнуть, что порядок реакции определяется только из экспериментальных данных и не связан со стехиометрическими коэффициентами при реагентах в уравнении реакции. Стехиометрическое уравнение реакции представляет собой уравнение материального баланса и никоим образом не может определять характера протекания этой реакции во времени.
В химической кинетике принято классифицировать реакции по величине общего порядка реакции. Рассмотрим зависимость концентрации реагирующих веществ от времени для необратимых (односторонних) реакций нулевого, первого и второго порядков.
1.2. Реакции нулевого порядка
Для реакций нулевого порядка кинетическое уравнение имеет следующий вид:
Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ; это характерно для многих гетерогенных (идущих на поверхности раздела фаз) реакций в том случае, когда скорость диффузии реагентов к поверхности меньше скорости их химического превращения.
1.3. Реакции первого порядка
Рассмотрим зависимость от времени концентрации исходного вещества А для случая реакции первого порядка А → В. Реакции первого порядка характеризуются кинетическим уравнением вида (II.6). Подставим в него выражение (II.2):
После интегрирования выражения (II.7) получаем:
Константу интегрирования g определим из начальных условий: в момент времени t = 0 концентрация С равна начальной концентрации Со. Отсюда следует, что g = ln Со. Получаем:
Рис. 2.3 Зависимость логарифма концентрации от времени для реакций первого порядка.
Т.о., логарифм концентрации для реакции первого порядка линейно зависит от времени (рис. 2.3) и константа скорости численно равна тангенсу угла наклона прямой к оси времени.
Из уравнения (II.9) легко получить выражение для константы скорости односторонней реакции первого порядка:
Еще одной кинетической характеристикой реакции является период полупревращения t1/2 – время, за которое концентрация исходного вещества уменьшается вдвое по сравнению с исходной. Выразим t1/2 для реакции первого порядка, учитывая, что С = ½Со:
Как видно из полученного выражения, период полупревращения реакции первого порядка не зависит от начальной концентрации исходного вещества.
1.4. Реакции второго порядка
Для реакций второго порядка кинетическое уравнение имеет следующий вид:
Рассмотрим простейший случай, когда кинетическое уравнение имеет вид (II.14) или, что то же самое, в уравнении вида (II.15) концентрации исходных веществ одинаковы; уравнение (II.14) в этом случае можно переписать следующим образом:
После разделения переменных и интегрирования получаем:
Постоянную интегрирования g, как и в предыдущем случае, определим из начальных условий. Получим:
Таким образом, для реакций второго порядка, имеющих кинетическое уравнение вида (II.14), характерна линейная зависимость обратной концентрации от времени (рис. 2.4) и константа скорости равна тангенсу угла наклона прямой к оси времени:
Рис. 2.4 Зависимость обратной концентрации от времени для реакций второго порядка.
Если начальные концентрации реагирующих веществ Cо,А и Cо,В различны, то константу скорости реакции находят интегрированием уравнения (II.21), в котором CА и CВ – концентрации реагирующих веществ в момент времени t от начала реакции:
В этом случае для константы скорости получаем выражение
Порядок химической реакции есть формально-кинетическое понятие, физический смысл которого для элементарных (одностадийных) реакций заключается в следующем: порядок реакции равен числу одновременно изменяющихся концентраций. В случае элементарных реакций порядок реакции может быть равен сумме коэффициентов в стехиометрическом уравнении реакции; однако в общем случае порядок реакции определяется только из экспериментальных данных и зависит от условий проведения реакции. Рассмотрим в качестве примера элементарную реакцию гидролиза этилового эфира уксусной кислоты (этилацетата), кинетика которой изучается в лабораторном практикуме по физической химии:
Если проводить эту реакцию при близких концентрациях этилацетата и воды, то общий порядок реакции равен двум и кинетическое уравнение имеет следующий вид:
При проведении этой же реакции в условиях большого избытка одного из реагентов (воды или этилацетата) концентрация вещества, находящегося в избытке, практически не изменяется и может быть включена в константу скорости; кинетическое уравнение для двух возможных случаев принимает следующий вид:
2) Избыток этилацетата:
В этих случаях мы имеем дело с так назывемой реакцией псевдопервого порядка. Проведение реакции при большом избытке одного из исходных веществ используется для определения частных порядков реакции.
1.5. Методы определения порядка реакции
Проведение реакции в условиях, когда концентрация одного из реагентов много меньше концентрации другого (других) и скорость реакции зависит от концентрации только этого реагента, используется для определения частных порядков реакции – это т.н. метод избыточных концентраций или метод изолирования Оствальда. Порядок реакции по данному веществу определяется одним из перечисленных ниже методов.
Графический метод заключается в построении графика зависимости концентрации реагента от времени в различных координатах. Для различных частных порядков эти зависимости имеют следующий вид:
Зависимость концентрации от времени
Если построить графики этих зависимостей на основании опытных данных, то лишь одна из них будет являться прямой линией. Если, например, график, построенный по опытным данным, оказался прямолинейным к координатах lnC = f(t), то частный порядок реакции по данному веществу равен единице.
Метод подбора кинетического уравнения заключается в подстановке экспериментальных данных изучения зависимости концентрации вещества от времени в кинетические уравнения различных порядков. Подставляя в приведённые в таблице уравнения значения концентрации реагента в разные моменты времени, вычисляют значения константы скорости. Частный порядок реакции по данному веществу равен порядку того кинетического уравнения, для которого величина константы скорости остаётся постоянной во времени.
Выражение для константы скорости
Метод определения времени полупревращения заключается в определении t1/2 для нескольких начальных концентраций. Как видно из приведённых в таблице уравнений, для реакции первого порядка время полупревращения не зависит от Co, для реакции второго порядка – обратно пропорционально Co, и для реакции третьего порядка – обратно пропорционально квадрату начальной концентрации.
Источник
3.2 Кинетическая классификация химических реакций
В кинетике химические реакции разделяются по признаку молекулярности и по признаку порядка реакции.
3.2.1 Молекулярность реакции
Наименьшее число частиц в элементарном акте химического превращения определяет молекулярность реакции.
Если реакция aA + bB 
К мономолекулярным реакциям относятся некоторые реакции разложения молекул, реакции внутримолекулярных перегруппировок, реакции радиоактивного распада.
К бимолекулярным реакциям относятся такие, в которых взаимодействие происходит при столкновении двух молекул различного или одинакового вида:
К тримолекулярным относятся реакции, в которых необходимо столкновение трех молекул:
Если же реакция происходит через несколько элементарных актов, то каждый акт имеет свою молекулярность. Например, в реакции
Происходят следующие стадии:
3. Н + Br2(г) 
По виду стехиометрического уравнения (а) нельзя судить о молекулярности реакции, надо знать механизм течения реакции, а значит классифицировать по молекулярности можно лишь реакции, протекающие в одну стадию. Поэтому для характеристики кинетики экспериментально изучаемых реакций вводится более формальный признак – порядок реакции.
3.2.2 Порядок реакции
Порядок реакции по данному веществу – число, равное степени, в которой концентрация этого вещества входит в кинетическое уравнение реакции:

где m – частный порядок по веществу А; n — частный порядок по веществу В.
Сумма показателей степеней, в которых концентрации всех исходных веществ входят в кинетическое уравнение, определяет порядок реакции.
Если реакция проходит в одну стадию, то молекулярность совпадает с ее порядком. Обычно же порядок не совпадает с молекулярностью. Это происходит потому, что реакции, как правило, не протекают путем непосредственного взаимодействия одновременно всех исходных частиц с прямым переходом их в продукты реакции. Это прежде всего относится к тем реакциям, в которых принимает участие более трех частиц.
Однако, даже реакции, в которых участвуют две или одна молекулы, часто идут не по бимолекулярному или мономолекулярному механизму, а более сложным путем. В простейшем случае, когда одна из стадий протекает очень медленно по сравнению с остальными, скорость (и порядок) реакции определяется этой наиболее медленной реакцией, которая называется лимитирующей. Если же скорости реакций отдельных стадий сравнимы, а эти стадии являются к тому же сложными, то картина еще более усложняется. В общем случае коэффициенты в стехиометрическом уравнении аА + вВ 
будут различны, а порядок реакции равен сумме показателей в кинетическом уравнении: m + n.
Реакции могут быть первого, второго, третьего, дробного и нулевого порядков. Так, рассмотренная нами выше реакция
является реакцией полуторного порядка, так как стадия (1) – реакция первого порядка, стадии (2) и (3) – второго порядка, причем стадия (3) является сложной (обратимой). В целом реакция имеет полуторный порядок.
Реакциями нулевого порядка называют реакции, в которых скорость процесса сохраняется постоянной во времени. Это встречается в некоторых гетерогенных системах. Так, если в реакции омыления сложного эфира водой в разбавленном водном растворе
применять эфир, малорастворимый в воде, и взять его в избытке, чтобы в системе присутствовал эфирный слой, то расход эфира будет постоянно восполняться из эфирного слоя. Таким образом, концентрация его в водном растворе будет постоянной. Но так как реакция идет в разбавленном водном растворе, то есть в присутствии избытка воды, то концентрация воды изменяется весьма незначительно, ее можно считать тоже постоянной, следовательно, постоянной будет скорость процесса. И реакция в целом имеет нулевой порядок. Если же только один из компонентов, например, вода, в избытке, то расход ее в реакции практически не отражается на ее концентрации (порядок по воде равен нулю) и скорость реакции зависит лишь от изменения концентрации эфира. Порядок реакции в этом случае равен порядку по эфиру.
Реакции первого порядка
Пусть реакция является кинетически необратимой реакцией первого порядка.
Составим дифференциальное уравнение которым описывается изменение концентрации исходного вещества А:

Поскольку А – единственное исходное вещество впредь будем опускать индекс А.
Решаем дифференциальное уравнение :

Уравнение (3.2) является уравнением прямой в координатах (lnC; t), рисунок 3.2.
Рисунок 3.2 – Зависимость lnC от времени для реакций первого порядка
Константа скорости может быть найдена как тангенс угла наклона прямой.
Определенное интегрирование дает:
то есть константа не зависит от способа выражения концентрации. Размерность константы [t -1 ]. Если известна константа скорости k, то можно определить текущую концентрацию:

Отсюда 
Существенное значение имеет время, за которое концентрация исходного вещества упадет в два раза, так называемое время полураспада (t1/2) или полупериод реакции.

Таким образом, из уравнения (3.4) видно, что полупериод реакции первого порядка не зависит от начальной концентрации.
Скорость, разумеется, будет зависеть от концентрации (рисунок 3.3).
Рисунок 3.3 – Кинетическая кривая реакции первого порядка
Как видно из рисунка 3.3 время, за которое начальная концентрация упадет вдвое, сохраняется постоянным для данной реакции, а скорость понижается (кривые становятся более пологими с уменьшением начальной концентрации).
Реакции второго порядка
Кинетическое уравнение для реакции второго порядка имеет вид:
Приведем выводы (аналогичные реакции первого порядка), для простоты, полагая, что концентрации веществ А и В одинаковы: 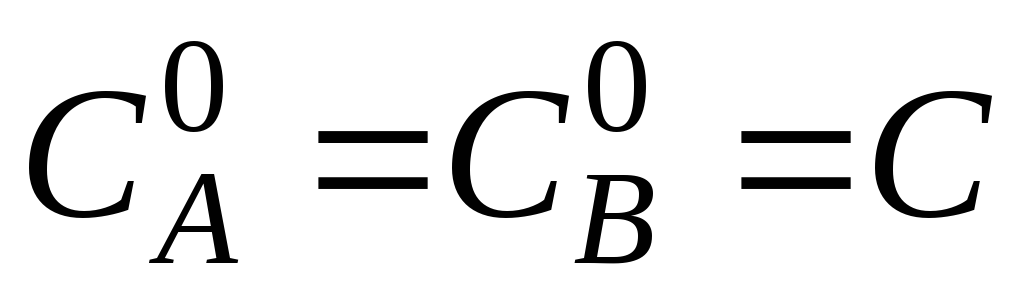
Полученное уравнение – линейная зависимость 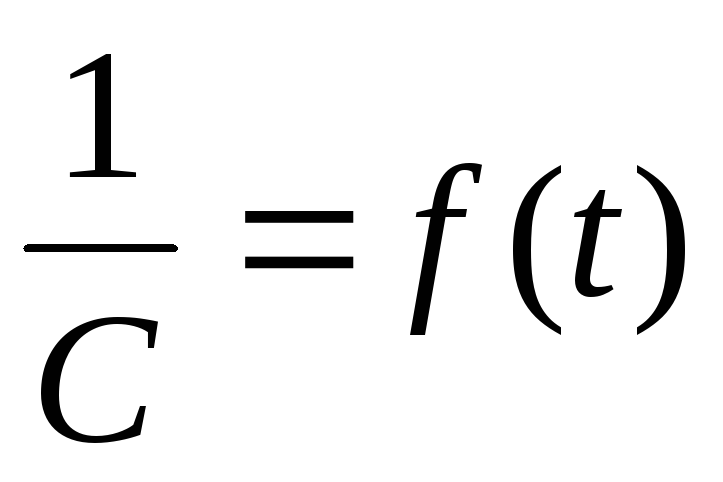
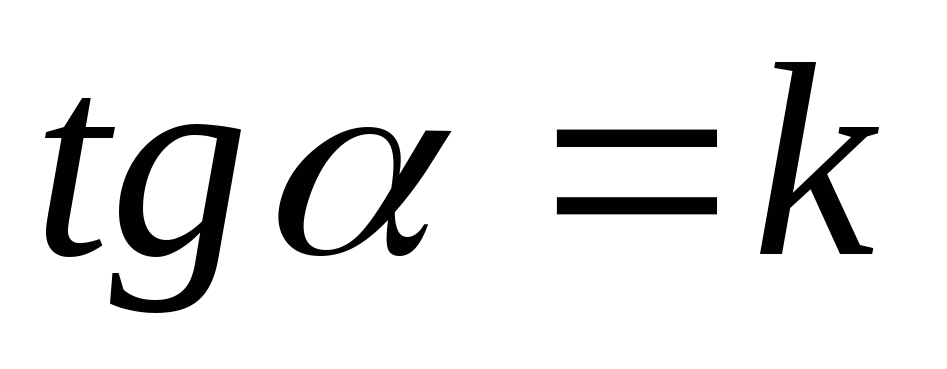
Рисунок 3.4 – Зависимость 
Из уравнения (3.5) выводится значение константы скорости реакции второго порядка:

Время полупериода вычисляется так:
Отсюда видно, что время полураспада зависит от начальной концентрации. Во сколько раз уменьшается концентрация, во столько раз увеличивается полупериод реакции.
Рисунок 3.5 – Кинетическая кривая реакции второго порядка
Если же исходные концентрации веществ А и В различны, то константа скорости определяется уравнением:

где 
Тут вы можете оставить комментарий к выбранному абзацу или сообщить об ошибке.
Источник















