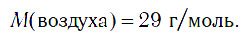Урок 15. Воздух как смесь газов
В уроке 15 «Воздух как смесь газов» из курса «Химия для чайников» мы выясним из чего состоит воздух; узнаем о получении, собирании и хранении газов, а также об их герметичности.
Вы уже знаете, что вещества могут находиться в различных агрегатных состояниях: газообразном, жидком и твердом.
В окружающей нас природе многие вещества при обычных условиях находятся в газообразном состоянии. Прежде всего, это компоненты воздушной оболочки Земли — атмосферы. Очень много газов растворено в водах Мирового океана. Во время извержения вулканов в атмосферу также выбрасывается большое количество вулканических газов. В недрах нашей планеты хранятся огромные запасы природного газа.
Атмосфере принадлежит важнейшая роль в жизни человека, животных и растений. Ее исследованиям были посвящены труды многих ученых прошлого. С давних времен был известен лишь один вид газа — воздух. При этом он изучался в основном физиками и интереса у химиков не вызывал. Лишь во второй половине XVIII в. было установлено, что воздух представляет собой смесь газов.
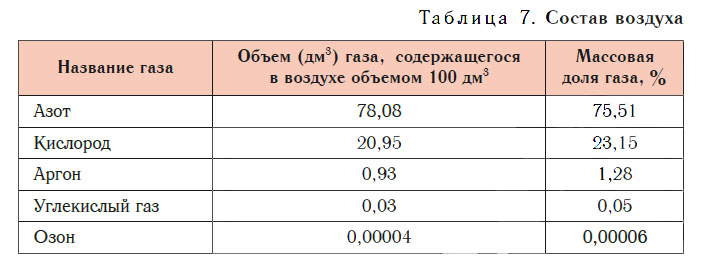
Состав воздуха
Основные компоненты воздуха — азот и кислород. При нормальных условиях в воздухе объемом 100 дм 3 содержится азот объемом около 78 дм 3 и кислород объемом около 21 дм 3 , а на долю всех остальных газов приходится около 1 дм 3 . В заметных количествах в воздухе присутствуют аргон, углекислый газ, озон и другие газы (табл. 7).
Для решения некоторых задач и проведения расчетов в физике, химии, технике очень удобно рассматривать воздух не как смесь газов, а как одно газообразное вещество. Экспериментальным путем можно установить, что при нормальных условиях масса воздуха объемом 22,4 дм 3 равна 29 г. Поскольку такой объем при н. у. занимает любой газ химическим количеством 1 моль, то молярную массу воздуха можно условно считать равной 29 г/моль:
Все газы, молярная масса которых меньше 29 г/моль, принято называть газами легче воздуха (например, водород H2, аммиак NH3, угарный газ CO, метан CH4), а газы, у которых она больше 29 г/моль — газами тяжелее воздуха (например, кислород O2, озон O3, углекислый газ CO2).
Получение, собирание и хранение газов
Газы имеют важное значение в жизни и деятельности человека. Поэтому необходимо уметь их получать, собирать и хранить.
В химической лаборатории небольшие объемы газов можно получать различными способами. Например, газы выделяются при нагревании некоторых твердых веществ (рис. 66).
Газообразные вещества могут образовываться при действии некоторых жидких веществ на твердые. Так, при действии уксуса на мрамор или мел выделяется углекислый газ (рис. 67).
В промышленности используют значительно большие, чем в химических лабораториях, количества различных газов. Большие объемы кислорода и азота получают из воздуха. Позднее вы узнаете, как это делается.
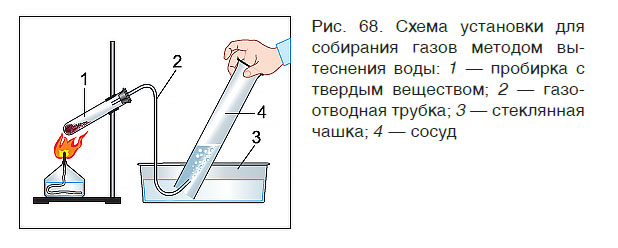
В лабораторных условиях собрать газ в сосуд можно двумя способами: вытеснением воды (рис. 68) и вытеснением воздуха. Первый способ применяют для собирания только нерастворимых в воде газов (кислород, азот, водород). Вто-
рой — для собирания как растворимых (аммиак, углекислый газ), так и нерастворимых в воде газов.
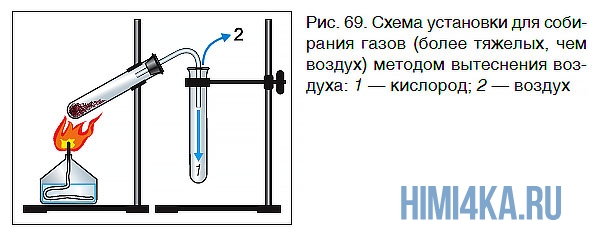
Для собирания газов, которые легче воздуха, сосуд для сбора газа следует закрепить дном вверх, а для газов, которые тяжелее воздуха, — дном вниз (рис. 69)
Для хранения газов следует использовать сосуды, не сообщающиеся с окружающей средой. Такие сосуды называют герметичными (т. е. не имеющими отверстий для выхода газа из сосуда наружу). В быту примером герметичного сосуда является бутылка с плотной пробкой, завязанный воздушный шарик или накачанная камера от велосипедного колеса, в химической лаборатории — пробирка, плотно закрытая пробкой, газометр.
Из курса физики вы знаете, что при нагревании газы расширяются. Это свойство можно использовать для проверки прибора для получения газов на герметичность (рис. 70). Для этого после сборки прибора следует погрузить конец газоотводной трубки в воду, а пробирку на несколько секунд зажать в ладони. Нагреваясь от тепла руки, воздух в пробирке расширяется и выходит из газоотводной трубки в виде пузырьков. Если пузырьки не наблюдаются, то это свидетельствует о том, что прибор собран негерметично и для газа имеется другой выход, кроме газоотводной трубки.
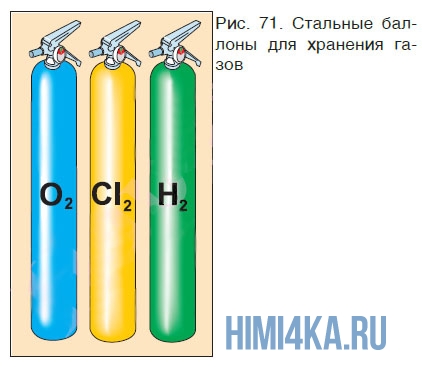
В промышленности для хранения газов чаще всего используют более прочные сосуды — баллоны (рис. 71), в которых сжатые газы находятся под большим давлением; для предупреждения разрушения баллона сжатым газом его стенки делают из толстой стали. Узнать, какой газ содержится в баллоне, можно по окраске баллона, цвету надписи на нем и цвету полосы. Например, баллон с кислородом должен быть окрашен в голубой цвет и иметь черную надпись «Кислород», баллон с азотом должен быть окрашен в черный цвет, иметь желтую надпись «Азот» и коричневую полосу, баллон с очень чистым аргоном должен быть окрашен в серый цвет, иметь зеленую надпись «Аргон» и зеленую полосу.
Краткие выводы урока:
- Вещества могут находиться в газообразном, жидком или твердом агрегатном состоянии.
- Воздух представляет собой смесь газов. Основными компонентами воздуха являются азот и кислород.
- При нормальных условиях в воздухе объемом 100 дм 3 содержится азот объемом около 78 дм 3 и кислород объемом около 21 дм 3 .
- Воздух можно условно рассматривать как газ, молярная масса которого равна 29 г/моль.
Надеюсь урок 15 «Воздух как смесь газов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Источник
Конспект урока: «Воздух как смесь газов. Методы собирания газов»(7 класс)
Тема урока: «Воздух как смесь газов. Методы собирания газов»
Цели и задачи урока: Образовательные : Создать условия для знакомства учащихся с составом воздуха. Обучения учащихся с различными методами собирания газов. .Дать представление о лабораторных приборах для получения газов. Создать условия для знакомства с видами загрязнения атмосферы и мерами по ее охране, убедиться во взаимном влиянии веществ атмосферного воздуха и живых организмов друг на друга.
Развивающие: Создать условия для развития навыков проведения химического эксперимента, соблюдения правила техники безопасности; умения решать расчетные задачи с использованием понятий: молярный объем газа, молярная масса воздуха.
Воспитательные: Создать условия для воспитания мотивации учёбы, положительного отношения к знаниям, продолжения экологического воспитания и бережливого отношения к окружающей среде.
Оборудование: Марганцовка, пробирки, штатив, мрамор, соляная кислота, спиртовка, спички, пробирка с газоотводной трубкой, пакеты, шарик, чёрный ящик.
Тип урока: урок усвоения новых знаний.
I . Организационный момент. Учитель приветствует учащихся, проверяет готовность к уроку, настраивает на продуктивную деятельность.
II . Изучение нового материала.
Сегодня на уроке речь пойдет о том, что находится внутри черного ящика (на столе черный ящик). Подсказка: это знакомо абсолютно всем, это часть природы. Дети задают наводящие вопросы.
Приглашается один ученик для открытия ящика.
Что же там? Пустота?
Древнегреческий ученый, философ Аристотель более двух тысяч лет назад говорил своим ученикам: “Природа не терпит пустоты”. Кажется пустым, а на самом деле полностью заполнено вездесущим … (воздухом). Учитель: (загадывает загадку)
Через нас проходит в грудь
И обратный держит путь.
Он невидимый, но все же
Без него мы жить не можем.
Что же мы сегодня будем изучать? (Ответы учащихся)
Учащиеся формулируют тему урока (запись в тетради и на доске), в течение одной минуты отвечают в тетрадях на вопрос: “что вы знаете о воздухе?”. После того, как записали все, что знают о воздухе, обсуждают с соседом по парте. Далее делятся своими знаниями с учителем. Идет обсуждение. Что хотели бы еще узнать о воздухе? Учащиеся формулируют цель урока.
На доске план изучения темы:
Состав воздуха и физические свойства воздуха.
Методы собирание и хранение газов.
Применение и охрана воздуха.
Значение воздуха для живых организмов очень велико. Вот, что говорится в древнеегипетской притче :
«Речь, Зрение, Слух, Мысль, Дыхание состязались друг с другом, говоря: «Я- песнь, я-песнь». Они сказали: «Хорошо, оставим это тело, и пусть будет песней тот из нас, кто, выйдя из тела, заставит его упасть».
Речь вышла из тела, но тело продолжало существовать, лишенное речи, поглощая пищу и питье.
Зрение вышло из тела, но тело продолжало существовать, не видя, поглощая воду и питье.
Слух вышел и тела, но тело продолжало существовать, не слыша, поглощая воду и питье.
Мысль вышла из тела, но тело продолжало существовать, не мысля, поглощая воду и питье.
Дыхание вышло из тела. Тело упало. Оно разложилось. И о теле сказали: «тело стало телом»
Учитель обращается к учащимся: Как вы думаете, в чем смысл этой притчи?
Действительно, без пищи можно прожить более двух месяцев. Без воды — пару суток. А без воздуха – менее 10 минут. Эта притча говорит о том, что еще наши предки хорошо понимали, что без воздуха нет жизни. И всем известная поговорка: «Это нужно как воздух» отражает важное значение воздуха для человека и всего живого на Земле. Воздух содержится буквально во всем, что нас окружает: в воде, твердых веществах, организмах. Живые организмы вдыхают и выдыхают воздух. Какими же свойствами обладает воздух? (Учащиеся берут полиэтиленовые пакетики и надувают их).
Вопросы к учащимся:
— Что находится в пакетике?
— Какими свойствами обладает воздух? (без цвета, вкуса, запаха)
Воздух нужен всем: людям, животным, растениям. Чем же объясняется такое важное значение воздуха? Оно объясняется его составом. Сегодня о воздухе известно гораздо больше, чем двести лет назад знали ученые. Они считали воздух простым веществом. Шведский химик Кар Вильгельм Шееле, проводя опыты с воздухом в 1770 году, обнаружил газ, без которого не горит ни одно вещество.
Такое же открытие сделала Джосеф Пристли. Исследователи назвали его огненным газом. Позднее французский химик А. Лавуазье назвал этот газ кислородом. В 1774 году французский ученый А. Лавуазье провел 12–дневный опыт и установил, что лишь 1/5 часть воздуха занимает простое вещество — кислород. Значит воздух – это не одно вещество, а смесь. Думают и отвечают: воздух — гомогенная или гетерогенная смесь. Остальные составные части воздуха были определены позже в конце XIX века.
Составляем кластер , используя информацию текста учебника (стр.95-96). Проговариваем, из каких газов состоит воздух: постоянные части воздуха: кислород –21%, азот –78%, инертные газы (в основном аргон) –0,94%; переменные составляющие воздуха: углекислый газ — 0,03%, прочие примеси (водяной пар, пыль, оксиды серы и азота и другие газообразные вещества). Молярная масса воздуха 29 г/ моль. Все газы можно поделить на 2 группы в зависимости от их молярной массы: газы легче и тяжелее воздуха: запись в тетради.
Делаем вывод: воздух – однородная (гомогенная) смесь газов.
Методы собирания газов
В лабораторных условиях собрать газ можно двумя методами: вытеснением воды и вытеснением воздуха.
Первый из них применяется для собирания только нерастворимых в воде газов (кислород, азот, водород).
Второй – для собирания как растворимых (аммиак, углекислый газ), так и нерастворимых в воде газов.
Для собирания газов, которые легче воздуха, сосуд для сбора газа следует закрепить дном вверх, а для газов, которые тяжелее воздуха, – дном вниз.
Для хранения газов следует использовать сосуды, не сообщающиеся с окружающей средой. Такие сосуды называют герметичными (т. е. не имеющие отверстий для выхода газа из сосуда наружу). В быту примером герметичного сосуда является завязанный воздушный шарик или накачанная камера от велосипедного колеса, в химической лаборатории – пробирка, плотно закрытая резиновой пробкой.
Делаем опыт (Л.оп. 4) На столах находятся пробирки, прочно закрытые пробкой со стеклянной трубкой. Берем в ладошку пробирку и опускаем в стакан с водой трубку. Наблюдают за происходящим. Выслушиваем ответы учеников.
Тепло руки перешло воздуху, он расширился, перестал умещаться в пробирке и начал выходить по трубочке в воду, образуя пузырьки. Так проверяют прибор на герметичность, прежде чем использовать его для получения в нем газов.
Делается запись в опорный конспект: “ При нагревании воздух расширяется, при охлаждении – сжимается”.
Делаются записи в тетради.
Основные компоненты воздуха кислород и азот. Какое значение имеет кислород в природе? (благодаря кислороду появилась жизнь на Земле).
Да, значение кислорода очень велико. Именно кислород, попадая в организм человека, делает жизнетворной кровь, питающую клетки и ткани. Один человек за сутки выпивает из воздушного океана 11 тыс. литров воздуха, в котором содержится кислород. Благодаря кислороду существует жизнь на Земле, им дышат все живые организмы. Запасы кислорода восполняются благодаря растениям, которые выделяют этот газ. Особенно много кислорода выделяют леса.
Сейчас мы получим этот газ с помощью опыта и посмотрим, какими свойствами он обладает.
Опыт№1.В лабораторный штатив помещается пробирка с перманганатом калия. Нагревается на огне спиртовки. Кислород выделяется через отверстие пробирки по газоотводной трубке и собирается в химическом стакане. Тлеющая лучинка, помещенная в стакан с кислородом, вспыхивает.
Какой газ мы получили? (Ответ учащихся)
Какие свойства этого газа мы обнаружили? (Ответы учащихся)
Итак, кислород- газ, который:
-бесцветный, без вкуса и запаха, неядовит.
— кислород тяжелее воздуха.
— малорастворим в воде.
— химический знак его- О 2
-необходим для дыхания, горения
— применяется в медицине для облегчения
— кислородные маски необходимы при полетах в космос, при работе под водой.
Сейчас мы обнаружим газ, который тоже входит в состав воздуха.
Опыт№2. В пробирку помещаются кусочки мела, добавляется соляная кислота. Пробирка закрепляется в лапке штатива. Тлеющая лучинка, помещенная в атмосферу углекислого газа, гаснет.
-Какой газ мы получили?
— Какое свойство этого газа вы отметили бы? (не поддерживает горение, бесцветный, без вкуса и запаха, в больших количествах ядовит).
Значение углекислого газа в природе тоже очень велико. Из него растения создают крахмал — необходимое для них питательное вещество. (Показать)
Также его применяют для газирования напитков (показать — открыть бутылку с минеральной водой)Свойство углекислого газа, не поддерживать горение, применяется в огнетушителях.
Еще одной составной частью воздуха является азот. Он занимает самую большую часть воздуха. Воздушный азот растения и животные усваивать не умеют. Но существуют бактерии, которые могут поглощать его в земле. Вот какие клубеньки образуют бактерии на корнях гороха, фасоли. В них в виде соединений содержится азот.
На землю азот попадает вместе с каплями дождя и пылью. Бактерии, соединяя азот с другими элементами, образуют минеральные азотистые соединения. Главным образом, соли, растворенные в воде, всасывающиеся растениями.
Состав трех основных газов в атмосфере неизменен, но и в результате природных явлений в воздухе можно обнаружить достаточное количество пыли, сажи. Главным источником пыли в нижних слоях атмосферы являются безводные пустыни и степи при суховеях, сопровождающихся ветрами.
Предприятия выбрасывают в атмосферу частицы пыли, которая соединяется с вредными веществами образует смог, становится трудно дышать. Смог можно наблюдать в больших городах.
Одна крупная электростанция выбрасывает ежедневно 1200 тонн золы, 600 тонн сернистого газа. Поэтому нужно принимать меры, что бы обеспечить чистоту воздуха и сохранить его газовый состав.
Нужно помнить, что в помещениях, где скапливается много народа, изменяется состав воздуха. Уменьшается количество кислорода, увеличивается количество углекислого газа. Появляется головокружение, слабость, головная боль. Становится трудно дышать. Что же нужно делать, что бы поддерживать нормальный состав воздуха в классе? (Ответы учащихся)
Учитель подводит итог сказанному:
Необходимо проветривать класс.
На перемене нужно выходить из класса.
Проводить влажную уборку, что бы уменьшить количество пыли
В классе желательно иметь комнатные растения.
III .Закрепление: фронтальный опрос
Перечислите газы, входящие в состав воздуха.
Назовите основные физические свойства воздуха.
Какие вы знаете классификации газов?
Перечислите методы собирания газов.
Приведите примеры газов легче и газов тяжелее воздуха.
Найдите объём кислорода в воздухе объёмом 120 дм 3.
Источник