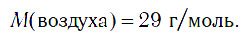Собирание газов
Получение газов термическим разложением твердых веществ
Газообразные вещества образуются также при прокаливании твердых со-
единений. Для получения газов таким способом разлагаемое вещество помещают в реторту или пробирку из тугоплавкого стекла и нагревают. При прокаливании веществ необходимо следить за наличием свободного выхода выделяющегося газа.
Способы собирания газов определяются их свойствами: растворимостью и
взаимодействием с водой, с воздухом, ядовитостью газа. Различают два основных способа собирания газов: вытеснением воздуха и вытеснением воды.
Вытеснением воздуха собирают газы, которые не взаимодействуют с воздухом. По относительной плотности газа по воздуху делают заключение, как расположить сосуд для собирания газов (рис. 30, а, б) На рис. 30, показано собирание газа с плотностью по воздуху более единицы, например, оксид азота (IV), плотность которого по воздуху равна 1,58. На рис. 30, б показано собирание газа с плотностью по воздуху менее единицы, например водорода, аммиака и др.
Вытеснением воды собирают газы, которые не взаимодействуют с водой и
плохо в ней растворяются (рис. 30, в). Цилиндр или банку заполняют водой и закрывают стеклянной пластинкой так, чтобы в цилиндре не оставалось пузырьков воздуха. Пластинку придерживают рукой, цилиндр переворачивают и опускают в стеклянную ванну с водой. Под водой пластинку удаляют, в открытое отверстие
цилиндра подводят газоотводную трубку. Газ постепенно вытесняет воду из цилиндра и заполняет его, после чего отверстие цилиндра под водой закрывают стеклянной пластинкой и цилиндр, заполненный газом, вынимают. Если газ тяжелее воздуха, то цилиндр ставят дном на стол, а если легче, то дном вверх на пластинку. Газы над водой можно собирать в пробирки, которые, так же как и цилиндр, заполняют водой, закрывают пальцем и опрокидывают в стакан или в стеклянную ванну с водой. Для собирания газа чаще всего применяют цилиндры с притертыми к ним стеклянными пластинками для закрывания.
Ядовитые газы собирают обычно вытеснением воды, так как при этом легко
отметить, когда газ целиком заполнит сосуд. Если необходимо собрать газ вытеснением воздуха, то поступают следующим образом (рис. 29, г). В колбу (банку, цилиндр) вставляют пробку с двумя газоотводными трубками. Через одну, которая доходит почти до дна, впускают газ, конец другой опускают в стакан с раствором, поглощающим газ. Например, для поглощения оксида серы (IV) в стакан наливают раствор щелочи, для поглощения хлороводорода – воду. После заполнения колбы (банки) газом вынимают из нее пробку с газоотводными трубками и сосуд быстро закрывают пробкой или стеклянной пластиной, а пробку с газоотводными трубками помещают в газопоглощающий раствор.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Урок 15. Воздух как смесь газов
В уроке 15 «Воздух как смесь газов» из курса «Химия для чайников» мы выясним из чего состоит воздух; узнаем о получении, собирании и хранении газов, а также об их герметичности.
Вы уже знаете, что вещества могут находиться в различных агрегатных состояниях: газообразном, жидком и твердом.
В окружающей нас природе многие вещества при обычных условиях находятся в газообразном состоянии. Прежде всего, это компоненты воздушной оболочки Земли — атмосферы. Очень много газов растворено в водах Мирового океана. Во время извержения вулканов в атмосферу также выбрасывается большое количество вулканических газов. В недрах нашей планеты хранятся огромные запасы природного газа.
Атмосфере принадлежит важнейшая роль в жизни человека, животных и растений. Ее исследованиям были посвящены труды многих ученых прошлого. С давних времен был известен лишь один вид газа — воздух. При этом он изучался в основном физиками и интереса у химиков не вызывал. Лишь во второй половине XVIII в. было установлено, что воздух представляет собой смесь газов.
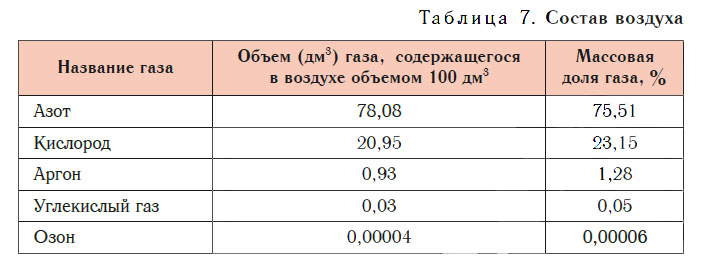
Состав воздуха
Основные компоненты воздуха — азот и кислород. При нормальных условиях в воздухе объемом 100 дм 3 содержится азот объемом около 78 дм 3 и кислород объемом около 21 дм 3 , а на долю всех остальных газов приходится около 1 дм 3 . В заметных количествах в воздухе присутствуют аргон, углекислый газ, озон и другие газы (табл. 7).
Для решения некоторых задач и проведения расчетов в физике, химии, технике очень удобно рассматривать воздух не как смесь газов, а как одно газообразное вещество. Экспериментальным путем можно установить, что при нормальных условиях масса воздуха объемом 22,4 дм 3 равна 29 г. Поскольку такой объем при н. у. занимает любой газ химическим количеством 1 моль, то молярную массу воздуха можно условно считать равной 29 г/моль:
Все газы, молярная масса которых меньше 29 г/моль, принято называть газами легче воздуха (например, водород H2, аммиак NH3, угарный газ CO, метан CH4), а газы, у которых она больше 29 г/моль — газами тяжелее воздуха (например, кислород O2, озон O3, углекислый газ CO2).
Получение, собирание и хранение газов
Газы имеют важное значение в жизни и деятельности человека. Поэтому необходимо уметь их получать, собирать и хранить.
В химической лаборатории небольшие объемы газов можно получать различными способами. Например, газы выделяются при нагревании некоторых твердых веществ (рис. 66).
Газообразные вещества могут образовываться при действии некоторых жидких веществ на твердые. Так, при действии уксуса на мрамор или мел выделяется углекислый газ (рис. 67).
В промышленности используют значительно большие, чем в химических лабораториях, количества различных газов. Большие объемы кислорода и азота получают из воздуха. Позднее вы узнаете, как это делается.
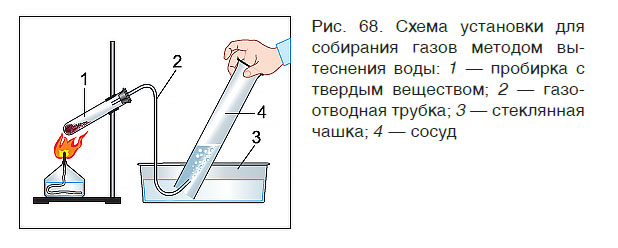
В лабораторных условиях собрать газ в сосуд можно двумя способами: вытеснением воды (рис. 68) и вытеснением воздуха. Первый способ применяют для собирания только нерастворимых в воде газов (кислород, азот, водород). Вто-
рой — для собирания как растворимых (аммиак, углекислый газ), так и нерастворимых в воде газов.
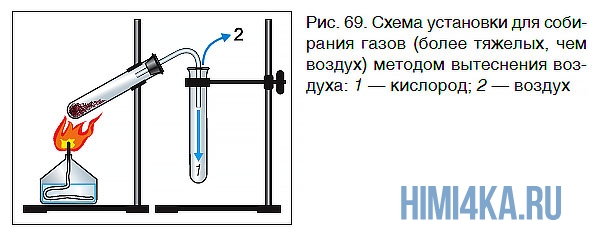
Для собирания газов, которые легче воздуха, сосуд для сбора газа следует закрепить дном вверх, а для газов, которые тяжелее воздуха, — дном вниз (рис. 69)
Для хранения газов следует использовать сосуды, не сообщающиеся с окружающей средой. Такие сосуды называют герметичными (т. е. не имеющими отверстий для выхода газа из сосуда наружу). В быту примером герметичного сосуда является бутылка с плотной пробкой, завязанный воздушный шарик или накачанная камера от велосипедного колеса, в химической лаборатории — пробирка, плотно закрытая пробкой, газометр.
Из курса физики вы знаете, что при нагревании газы расширяются. Это свойство можно использовать для проверки прибора для получения газов на герметичность (рис. 70). Для этого после сборки прибора следует погрузить конец газоотводной трубки в воду, а пробирку на несколько секунд зажать в ладони. Нагреваясь от тепла руки, воздух в пробирке расширяется и выходит из газоотводной трубки в виде пузырьков. Если пузырьки не наблюдаются, то это свидетельствует о том, что прибор собран негерметично и для газа имеется другой выход, кроме газоотводной трубки.
В промышленности для хранения газов чаще всего используют более прочные сосуды — баллоны (рис. 71), в которых сжатые газы находятся под большим давлением; для предупреждения разрушения баллона сжатым газом его стенки делают из толстой стали. Узнать, какой газ содержится в баллоне, можно по окраске баллона, цвету надписи на нем и цвету полосы. Например, баллон с кислородом должен быть окрашен в голубой цвет и иметь черную надпись «Кислород», баллон с азотом должен быть окрашен в черный цвет, иметь желтую надпись «Азот» и коричневую полосу, баллон с очень чистым аргоном должен быть окрашен в серый цвет, иметь зеленую надпись «Аргон» и зеленую полосу.
Краткие выводы урока:
- Вещества могут находиться в газообразном, жидком или твердом агрегатном состоянии.
- Воздух представляет собой смесь газов. Основными компонентами воздуха являются азот и кислород.
- При нормальных условиях в воздухе объемом 100 дм 3 содержится азот объемом около 78 дм 3 и кислород объемом около 21 дм 3 .
- Воздух можно условно рассматривать как газ, молярная масса которого равна 29 г/моль.
Надеюсь урок 15 «Воздух как смесь газов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Источник
Какие способы собирания газа вам известны?
Основные способы:
1. Вытеснением воздуха
2. Вытеснением воды
3. В перевёрнутую пробирку.
Способы собирания газов видоизменяются в зависимости от условий, в которых приходится работать.
Часто употребляют трубки, оттянутые с одной стороны и запаянные с другой, когда газовая среда легко доступна. Выкачав из такой трубки воздух ртутным насосом, оттянутую шейку запаивают паяльной трубкой; введя потом шейку в атмосферу газа, который хотят собирать, запаянный кончик отламывают и, когда трубка наполнится газом, его вновь запаивают. Подобного рода прием употреблялся, напр. , С. -К. -Девиллем для собирания газов, выделяющихся из кратеров потухших вулканов. Чтобы избежать употребления паяльной трубки, делают трубки для собирания газа с краном или даже двумя на одном и другом конце, и тогда, чтобы наполнить трубку исследуемым газом, достаточно, открыв краны, прососать через нее газ некот. время (для полного удаления воздуха) . Так собирают газы, выделяемые нефтью, бродящими жидкостями и т. п.
Из жидкостей растворенные в них газы извлекаются кипячением или при помощи ртутного насоса. Наполнив колбу исследуемою жидкостью доверху, закупоривают ее плотно пробкой, в которую проходит отводная трубка, также наполняемая до краев выдавливаемой жидкостью. Конец трубки подводят под цилиндр с ртутью, опрокинутый над ртутной же ванной, и затем колбу нагревают до кипения, причем растворенный газ выделяется и собирается в цилиндре.
Источник
Способы сбора газа для испытания
Методы собирания получаемых газов определяются свойствами получаемых газов. Если нужно небольшое количество газа, то можно собирать в пробирке. Если газ нужно сохранить в течение некоторого времени, пробирку закрывают хорошо подобранной пробкой. Для работы с газообразными веществами нужно иметь несколько комплектов различно изогнутых трубок диаметром 2, 3 и 4 мм. Удобно иметь также короткие, различно изогнутые трубки, которые можно присоединить к прибору каучуковыми трубками. Концы всех трубок должны быть оплавлены.
Собирание газа путем вытеснения воздуха.Колбочку или пробирку, в которой получают газ, укрепляют в штативе. Конец газоотводной трубки опускают в пробирку — газоприемник почти до дна. Если плотность газа приблизительно равна плотности воздуха или больше ее, газ собирают в открытую пробирку, поставленную вертикально отверстием вверх (См. рисунок по теме “Кислород”). Если же газ легче воздуха, пробирку газоприемник держат (или укрепляют в штативе) отверстием вниз.
Собирание газа над водой. Для собирания газа над водой необходима ванна. В качестве такой ванны можно использовать маленький кристаллизатор, фарфоровую чашку или другой подобный сосуд. Пробирку – газоприемник наполняют водой и, закрыв отверстие пальцем, опускают в ванну с водой дном вверх.
Под водой пробирку осторожно открывают и ставят так, чтобы вода из нее не выливалась. Когда весь воздух из реакционного сосуда будет вытеснен выделяющимся газом, конец газоотводной трубки погружают в воду и подводят под отверстие пробирки газоприемника (см. рис. по теме “Кислород”). Наполнив пробирку газом, закрывают ее под водой пальцем или пробкой и вынимают из ванны.
Если газ получают при нагревании, конец газоотводной трубки сразу же после наполнения газоприемника вынимают из ванны, так как при охлаждении прибора в него может быть втянута вода.
Если требуется отметить только цвет и запах выделяющегося газа или наблюдать его горение, то собирать газ в отдельный сосуд нет необходимости. Цвет газа видно через стекло пробирки, запах определяют, направляя легким взмахом руки струю газа к себе (см. рис.1).
В случае надобности газ очищают и осушают в промывных склянках с водой или растворами соответствующих поглотителей и в поглотительных склянках, наполненных каким-либо осушителем. Склянки эти размещают между аппаратом для получения газа и газоприемником.
Дата добавления: 2014-12-26 ; просмотров: 2666 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Источник
Краткие теоретические сведения



Практическая работа №2
«Получение и распознавание газов»
Краткие теоретические сведения
Строение газообразных веществ отличается от строения веществ в твердом и жидком состояниях. Газы не имеют собственной формы и расширяются до тех пор, пока не заполнят весь сосуд принимая его форму, по этой же причине газы не имеют собственного объема. Объем газа определяется объемам сосуда. Газ оказывает на стенки сосуда одинаковое во всех направлениях давления. Газы легко сжимаются. Благодаря большому расстоянию между молекулами газы смешиваются друг с другом в любом отношении. Основные газы получаемые и используемые в лабораториях это водород, кислород, углекислый газ.
Лабораторные способы получения этих газов:
Водород получают в аппарате Киппа, при взаимодействии соляной кислоты и металлического цинка (в гранулах) — при комнатной температуре:
Zn + 2HCl = ZnCl2 + H2
Оксид углерода (IV) = углекислый газ можно получить, действуя соляной или разбавленной серной кислотой на мрамор (основное вещество — карбонат кальция) или другой карбонат (при комнатной температуре). Сильная кислота (серная или соляная) будет вытеснять слабую угольную кислоту из её солей; угольная кислота нестойкая, поэтому практически сразу разлагается на углекислый газ и воду:
СаСО3 + 2HCl = CaCl2 + CO2 + H2O
Можно получить углекислый газ, сжигая лучину, бумагу или кусочек угля.
Кислород можно получить разложением при нагревании бертолетовой соли или лучше перманганата калия:
2KClO3 = 2KCl + 3O2 (есть опасность взрыва)
2KMnO4 = K2MnO4 + MnO2 + O2
Собирание газов
В устройстве аппарата Киппа предусмотрена газоотводная трубка с краником; для получения углекислого газа и кислорода реактивы помещают в пробирку и закрывают её пробкой с газоотводной трубкой. Пробирку с перманганатом калия закрепляют в штативе и нагревают пламенем спиртовки.
Водород легче воздуха, поэтому его собирают над воздухом, в перевёрнутую пробирку. Кислород и углекислый газ тяжелее воздуха, поэтому их можно собирать вытеснением воздуха, опустив газоотводную трубку на дно пробирки. Кислород малорастворим в воде, поэтому его можно также собирать над водой, в перевёрнутую пробирку (этот способ лучше, т.к. разница молярных масс кислорода (32 г/моль) и воздуха (29 г/моль) невелика).
Чтобы распознать эти газы, нужно знать их свойства.
Так, кислород поддерживает горение — опущенная в пробирку с кислородом тлеющая лучинка начинает ярко гореть; углекислый газ не поддерживает горение — горящая лучинка, опущенная в пробирку с углекислым газом, гаснет.
Углекислый газ, кроме того, мутит известковую воду: при его взаимодействии с гидроксидом кальция («известковой водой») образуется нерастворимый в воде осадок карбоната кальция:
Са(ОН)2 + СО2 = СаСО3 + Н2О
Чистый водород сгорает с легким звуком «пах», водород с примесью воздуха взрывоопасен «гремучий газ» и в небольшом количестве сгорает с резким лающим звуком.
Водород (Н2) – самый легкий, бесцветный, не имеет запаха.
Кислород (О2) без запаха и цвета,тяжелее воздуха, мало растворим в воде.
Аммиак (NН3) имеет резкий характерный запах, без цвета, хорошо растворим в воде, легче воздуха.
Это оформить в тетради!
Практическая работа №2
Получение и распознавание газов
Цель: изучить процессы и химизм получения газов на примере водорода, кислорода и углекислого газа.
Оборудование:цинк в гранулах, раствор соляной кислоты, мел, раствор пероксида водорода, оксид марганца (II); пробирки, спиртовка, лучинка
Последовательность выполнения работы:
Внимание: Записи о наблюдаемых явлениях по всем опытам внесите в таблицу по форме:
| Что делали | Что наблюдали | Уравнения реакций |
| В пробирку поместить две гранулы цинка. 2. Прилить 2 мл раствора соляной кислоты. Что наблюдаете? Запишите уравнение реакции с точки зрения окислительно-восстановительного процесса. 3. Накрыть пробирку-реактор пробиркой большего диаметра. 4. Через 4 минуты поднимите большую пробирку и, не переворачивая, поднесите её к пламени спиртовки. Что наблюдаете? Запишите уравнение реакции. Что можете сказать о «чистоте» собранного водорода? | ||
| 1. В пробирку прилить 5 мл раствора пероксида водорода. 2. Подготовьте тлеющую лучину. 3. Добавьте в пробирку несколько крупинок оксида марганца (IV). Что наблюдаете? Запишите уравнение реакции с точки зрения окислительно-восстановительного процесса. 4. Внесите тлеющую лучину в пробирку с раствором пероксида водорода. | ||
| 1. В пробирку поместить кусочек мела. 2. Прилить к мрамору 4 мл раствора уксусной кислоты. Что наблюдаете? Запишите уравнение химической реакции в молекулярной и ионной форме. 3. Зажгите лучину. 4. Внесите горящую лучину в пробирку-реактор. |
Контрольные вопросы:
1. Почему водород собирают в перевернутую пробирку?
2. Если через раствор известковой воды посредством стеклянной трубки продувать выдыхаемый воздух, то через некоторое время известковая вода помутнеет. Почему?
3. Какое свойство углекислого газа лежит в основе его применения в углекислотном огнетушителе.
Список литературы
Габриелян О.С., Остроумов И.Г. Химия для профессий и специальностей технического профиля. М. Издательский центр «Академия». 2017
Тема 2. Практическая работа №3
Решение экспериментальных задач по теме «Металлы и неметаллы»
Это для ознакомления, не писать!
Краткие теоретические сведения
Распознавание веществ производится с помощью качественных реакций.
Качественные реакции – это химические реакции, с помощью которых можно определить то, чем одно вещество отличается от другого по элементарному составу, иначе говоря, эти реакции позволяют определить отдельные ионы или молекулы, из которых состоит исследуемое вещество или смесь веществ. В качественном анализе применяют реакции, сопровождающиеся каким-либо эффектом, который можно легко обнаружить органами чувств:
· Изменение окраски раствора;
· Выпадение или растворение осадка;
· Выделение газов (иногда обладающих характерным запахом)
В таблице приведены некоторые из качественных реакций.
| Катион | Воздействие или реактив | Наблюдаемая реакция |
| Na + | Пламя | Желтое окрашивание |
| К + | Пламя | Фиолетовое окрашивание |
| Са 2+ | Пламя | Кирпично-красное окрашивание |
| Аg + | хлорид | Выпадение белого осадка |
| Fe 2+ | гексациано-феррат (III) калия (красная кровяная соль) | Выпадение синего осадка |
| Fe 3+ | роданид | Красное окрашивание |
| Анион | Воздействие или реактив | Наблюдаемая реакция |
| S04 2- | соль бария | Выпадение белого осадка |
| СО3 2- | кислота | вскипание или пузырьки газа |
| Cl — | ионы Аg+ | Выпадение белого осадка, не растворимого в HN03 |
Для выполнения опытов отбирается проба (небольшое количество вещества помещается в чистую пробирку) и исследуется реактивом.
Источник