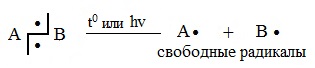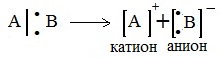- Какие способы разрыва ковалентной связи вам известны приведите примеры
- Какие способы разрыва ковалентной связи вам известны приведите примеры
- Какие способы разрыва ковалентной связи вам известны приведите примеры
- Таблица Менделеева
- Универсальная таблица растворимости
- Коллекция таблиц к урокам по химии
- Электронная природа химических связей в органических соединениях. Способы разрыва ковалентной связи
Какие способы разрыва ковалентной связи вам известны приведите примеры
1. Какова сущность процесса образования ковалентных связей с учетом характера движения электронов в атомах? Свой ответ поясните конкретными примерами.
Ковалентные связи образуются за счет общих пар электронов. В образовании ковалентной связи могут участвовать и s-электроны, и р-электроны, но только находящиеся на внешней электронной оболочке. Примеры:
1) молекула водорода Н2.
атом водорода имеет один электрон на 1 s-орбитали. Каждый атом водорода предоставляет по одному электрону для образования ковалентной связи.
2) молекула аммиака NH3.
атом водорода имеет один электрон на 1s-орбитали. Строение электронной оболочки атома азота 1s22s22р3.
2. В молекуле C2H5OH наиболее полярная связь образуется между атомами :
1) C и O
2) C и H
3) O и H
4) C и C
3. К какому виду по способу перекрывания орбиталей относятся связи в соединениях: H2, I2 ; HCl ; H2O
H₂ — s-s — перекрывание
J₂ — p-p — перекрывание
HCl —s-p — перекрывание
H₂O — p-s-p (sp²) — перекрывание
4. Какие реакции называют свободнорадикальными? приведите пример и запишите механизм этой реакции
Радикальный разрыв ковалентной связи.
А^В —► А + В
Происходит симметричный разрыв ковалентной связи, образуются частицы, имеющие по одному неспаренному электрону, неустойчивые и способные быстро вступить в химические превращения.
Радикалы, взаимодействуя друг с другом, превращаются в устойчивые продукты путем димеризации:
СН3 + СН3 ► Н3С—СН3; Н + Н ► Н2; СН3+Н—» СН4;
Реакции, протекающие при участии свободных радикалов, называют свободнорадикальными.
5. Какие способы разрыва ковалентной связи вам известны? Приведите примеры.
Радикальные (гомолитические) (см. выше) и ионные реакции. Ионные реакции в свою очередь делятся по характеру реагента, действующего на молекулу, на электрофильные и нуклеофильные.
Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим.
В результате образуются разноименно заряженные ионы — катион и анион. Гомолитический разрыв более характерен для неполярных и слабополярных связей, а гетеролитический — для полярных.
Источник
Какие способы разрыва ковалентной связи вам известны приведите примеры
По способу разрыва ковалентных связей органические реакции подразделяются на радикальные и ионные реакции. Ионные реакции в свою очередь делятся по характеру реагента, действующего на молекулу, на электрофильные и нуклеофильные.
1. Свободнорадикальный (гомолитический) разрыв связей
Разрыв связи, при котором каждый атом получает по одному электрону из общей пары, называется гомолитическим:
Такому разрыву подвергаются неполярные и малополярные ковалентные связи под действием света или высокой температуры. Образующиеся частицы содержат неспаренные электроны и называются свободными радикалами. Эти частицы обладают большой энергией и очень активны.
2. Ионный (гетеролитический) разрыв связей
Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим:
В результате образуются разноименно заряженные ионы – катион и анион. Если заряд иона сосредоточен на атоме углерода, то катион называют карбокатионом, а анион — карбанионом.
Устойчивы более разветвлённые катионы.
Такому разрыву подвергаются полярные ковалентные связи.
Образующиеся органические ионные частицы отличаются от неорганических тем, что они возникают в момент реакции.
Источник
Какие способы разрыва ковалентной связи вам известны приведите примеры
ХИМИЯ – это область чудес, в ней скрыто счастье человечества,
величайшие завоевания разума будут сделаны
именно в этой области.(М. ГОРЬКИЙ)
Таблица
Менделеева
Универсальная таблица растворимости
Коллекция таблиц к урокам по химии
Электронная природа химических связей в органических соединениях. Способы разрыва ковалентной связи
Данный урок поможет вам получить представление о теме «Ковалентная связь в органических соединениях». Вы вспомните природу химических связей. Узнаете о том, за счет чего образуется ковалентная связь, что является основой этой связи. На этом уроке также рассматривается принцип построения формул Льюиса, рассказывается о характеристиках ковалентной связи (полярности, длине и прочности), объясняется теория А. Бутлерова
I. Электронная природа химических связей в органических соединениях
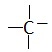
1. Все органические вещества содержат углерод. В молекулах органических веществ углерод переходит в возбуждённое состояние:
2. Органическим соединениям свойственны ковалентные связи. Ковалентная связь в молекулах характеризуется: энергией, длиной, насыщаемостью и пространственной направленностью.
а) Из курса химии 8 класса вы знаете, что ковалентная связь образуется за счёт перекрывания электронных облаков, при этом выделяется энергия, чем больше перекрывание, тем больше выделяется энергии и тем прочнее связь.
Типы перекрываний электронных облаков в порядке возрастания их прочности и энергии выделяемой при образовании:
σ(s – s)
б) Длина связи определяется расстоянием между центрами ядер связывающихся атомов и измеряется в нанометрах (1 нм = 10 -9 м). С повышением кратности связи (одинарная, двойная, тройная) длина становится меньше, а энергия выше:
в) Под насыщаемостью связи понимают способность образовывать строго определённое количество ковалентных связей.
г) Направленность ковалентной связи определяется взаимным расположением электронных облаков, участвующих в образовании химической связи. Ковалентная связь образуется в направлении максимального перекрывания электронных орбиталей взаимодействующих атомов.
Вы уже знаете, что атом углерода содержит на внешнем уровне четыре валентных электрона:
1 электрон на s – орбитали сферической формы
3 электрона на трёх p – орбиталях, орбитали имеют форму гантели и расположены под углом 90˚.
Таким образом можно предположить, что в молекуле метана CH4 атом углерода не может образовать 4 одинаковых связи с четырьмя атомами водорода (1 атом водорода имеет 1 электрон на s – орбитали сферической формы). Однако экспериментально доказано, что в молекуле метана все связи С – Н равноценны и направлены к вершинам правильного тетраэдра под углом 109˚28`.
В 1931 г. американский учёный Л. Полинг доказал, что в молекуле метана в момент образования молекулы электронные облака смешиваются и образуют гибридные электронные облака, происходит процесс гибридизации.
II. Гибридизация атомных орбиталей
Гибридизация – процесс смешения разных, но близких по энергии, орбиталей данного атома, с возникновением того же числа новых гибридных орбиталей, одинаковых по форме и энергии.
В зависимости от числа вступивших в гибридизацию орбиталей атом углерода может находиться в одном их трёх состояний гибридизации: sp 3 , sp 2 , sp.
1) sp 3 – гибридизация
Происходит смешение одной s и трёх p орбиталей. Образуются четыре одинаковые гибридные орбитали, расположенные относительно друг друга под тетраэдрическим углом 109˚28`. Образуются 4 ковалентные σ – связи.
Рис. Строение молекулы метана СН4 (тетраэдрическое)
2) sp 2 – гибридизация:
Происходит смешение одной s и двух p орбиталей. Образуются три одинаковые гибридные орбитали, они расположены относительно друг друга под углом 120˚, лежат в одной плоскости и стремятся к вершинам треугольника. Образуются 3 ковалентные σ – связи.
Оставшаяся одна негибридизованная орбиталь расположена перпендикулярно плоскости образования σ – связей и участвует в образовании П — связи.
Рис. Строение молекулы этилена С2Н4 (плоское тригональное)
3) sp – гибридизация
Происходит смешение одной s и одной p орбитали. Образуются две одинаковые гибридные орбитали, они расположены относительно друг друга под углом 180˚, лежат на одной линии. Образуются 2 ковалентные σ – связи.
Оставшиеся две негибридизованные орбитали расположены во взаимно перпендикулярных плоскостях и образуют две П — связи.
Рис. Строение молекулы ацетилена С2Н2 (линейное)
Направленность гибридных орбиталей в пространстве, а следовательно, и геометрическое строение молекул зависят от типа гибридизации. На форму молекулы в пространстве влияет направленность только σ – связей.
III. Степень окисления атома углерода
Для атома углерода в органических соединениях характерны степени окисления от -4 до +4.
Укажите степени окисления всех элементов в CH3CH2OH
Решение. Нахождение степеней окисления в органических соединениях имеет свою специфику. В частности, необходимо отдельно находить степени окисления для каждого атома углерода. Рассуждать можно следующим образом. Рассмотрим, например, атом углерода в составе метильной группы (СН3 –) . Данный атом С соединен с 3 атомами водорода и соседним атомом углерода. По связи С-Н происходит смещение электронной плотности в сторону атома углерода (т. к. электроотрицательность углерода превосходит ЭО водорода). Если бы это смещение было полным, атом углерода приобрел бы заряд -3.
Атом С в составе группы -СН2ОН связан с двумя атомами водорода (смещение электронной плотности в сторону С), одним атомом кислорода (смещение электронной плотности в сторону О) и одним атомом углерода (можно считать, что смещения эл. плотности в этом случае не происходит). Степень окисления углерода равна -2 +1 +0 = -1.
Ответ: С -3 H +1 3C -1 H +1 2O -2 H +1 .
IV. Простая и кратная ковалентные связи
Способность атома углерода иметь разные степени окисления и лёгкость гибридизации позволяет атому углерода образовывать одинарные, и кратные (двойные и тройные связи) не только с другими атомами углерода, но и с атомами других элементов-органогенов:
СН3 – СН3 (1 σ – сигма связь С-С)
CH2=CH2 (1 σ – сигма связь С-С и 1 П – пи связь С-С)
CH ≡ CH (1 σ – сигма связь С-С и 2 П – пи связи С-С)
V. Способы разрыва связей в молекулах органических веществ и механизмы органических реакций
Разрыв ковалентной связи может происходить двумя способами.
1. Разрыв связи, при котором каждый атом получает по одному электрону из общей пары, называется гомолитическим:
В результате гомолитического разрыва образуются сходные по электронному строению частицы, каждая из которых имеет неспаренный электрон. Такие частицы называются свободными радикалами.
Радикал – свободный атом или частица с неспаренными электронами, неустойчив и способный быстро вступать в химическую реакцию.
Гомолитический разрыв сопровождает процессы, осуществляемые при высоких температурах; на свету; при радиоактивном облучении в отсутствие растворителя (в газовой фазе) или неполярных растворителях. Гомолитическому разрыву подвергаются малополярные или неполярные связи C—C, C—H, Cl—Cl и др.
2. Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим:
А + — электрофильная частица,
:В — — нуклеофильная частица
В результате образуются разноименно заряженные ионы — катион и анион. Если заряд иона сосредоточен на атоме углерода, то катион называют карбокатионом, а анион — карбанионом.
Устойчивы более разветвлённые катионы!
Ионный тип разрыва связи характерен для П- связей и полярных σ – связей; при наличии полярного растворителя или катализатора.
Источник