Основные методы определения молекулярной массы
Осмометрический метод. Метод основан на измерении осмотического давления разбавленных растворов полимеров.
Молекулярную массу определяют по величине измеренного давления, пользуясь уравнением Вант-Гоффа в вириальной форме:

где p— осмотическое давление, атм;
С — массовая концентрация полимера, г/мл;
Т — абсолютная температура;
R— газовая постоянная;
Коэффициент A2 характеризует взаимодействие между полимером и растворителем.
При бесконечном разбавлении уравнение принимает вид;

Предельное значение p/С при С 
Молекулярная масса, определяемый осмометрическим методом, является среднечисловым.
Метод светорассеяния.Измерение рассеяния света растворами полимеров — один из важнейших методов определения среднемассовой молекулярной массы 

Для определения молекулярной массы необходимо измерить величину 



При 
Таким образом, для определения молекулярной маассы полимера необходимо измерить под углом 90° приведенные интенсивности рассеяния раствора 

Построив график зависимости КС/ 
Вискозиметрический метод. Вискозиметрический метод — наиболее простой и доступный метод определения молекулярной массы полимеров в широкой области значений молекулярных масс. Этот метод является косвенным и требует определения констант в уравнении, выражающем зависимость вязкости от молекулярных масс.
Для определения вязкости раствора полимера измеряют время истечения t0 и t (в сек),равных объемов растворителя и раствора через капилляр вискозиметра при заданной постоянной температуре. Концентрацию раствора (С)обычно выражают в граммах на 100 мл растворителя; для измерения вязкости используют растворы с С
Контрольные вопросы
1.1.Что такое полидисперсность? Назовите монодисперсные и полидисперсные полимеры.
2.Какие методы усреднения молекулярных масс полимеров знаете?
3.3.Для чего необходимо знать молекулярно-массовые распределение полимеров (ММР)?
4.Принцип построения интегрального и дифференциального кривых ММР.
5.Какие методы фракционирования знаете?
6.В чем суть вискозиметрического метода определения молекулярной массы полимеров?
7.Для чего применяется гель-проникающая хроматография?
8.Принцип определения молекулярной массы полимеров методом светорассеяния.
9.Какими методами определяют среднечисловую молекулярную массу. Опишите осмометрический метод.
Источник
Методы определения молекулярной массы
Наиболее распространёнными методами определения молекулярной массы являются термодинамические. Основаны они на том, что для разбавленных растворов разность значений некоторых характеристик раствора и чистого растворителя пропорциональны количеству растворённого вещества. К таким характеристикам относятся температуры затвердевания (замерзания) и кипения, величина осмотического давления, вязкость и др.
Методы криоскопии и эбулиоскопии основаны на измерении разности величин температур затвердевания или кипения раствора и чистого растворителя. Эти методы сравнительно несложны и позволяют с достаточной достоверностью измерять молекулярные массы, если их величины не превышают 10 3 . Использовать их для более высокомолекулярных веществ не позволяют возможности современных приборов измерения температуры, так как искомая разность температур при анализе продукта с молекулярной массой 15000 составляет около 10 -6 0 С.
Осмометрические методы измерений основаны на пропорциональности осмотического давления (Р) числу находящихся в определённом объёме раствора (V) грамм-молекул растворённого вещества (n). Эта пропорциональность количественно выражается уравнением Вант-Гоффа:
PV = nRT или 
Определение осмотического давления несложно в исполнении, но требует большой подготовительной работы и специального оборудования.
Вискозиметрические методы определения молекулярной массы в отличие от двух вышеупомянутых являются не абсолютными, а косвенными. Однако простота проведения исследований и используемых приборов, а также достаточная корректность результатов способствуют их широкому распространению. Для определения молекулярных масс полимерных соединений такие методы являются основными. В основе вискозиметрических методов лежит измерение вязкости разбавленных растворов.
Вязкость (внутреннее течение) жидкостей обусловлено взаимодействием молекул жидкого тела и проявляется при его течении. Течение жидкости в капилляре диаметром х характеризуется градиентом скорости dv/dx вследствие того, что молекулярный слой, непосредственно примыкающий к стенкам капилляра остаётся неподвижным, а слой, находящийся в центре капилляра, движется с максимальной скоростью. Ламинарное течение описывается законом И.Ньютона, согласно которому напряжение сдвига, вызывающее течение жидкости, пропорционально градиенту скорости течения параллельных слоёв τ = η · dv/dx. Коэффициент пропорциональности η в этом уравнении называется коэффициентом вязкости, динамической вязкостью или вязкостью. Размерность вязкости – ньютон-секунда на квадратный метр (н·сек/м 2 ) или паскаль-секунда (Па·с).
Измерение вязкости подвижных жидкостей проводится чаще всего в капиллярных вискозиметрах. В основе измерений лежит выведенное из закона Ньютона уравнение Пуазейля: Q = πr 4 ΔPt/(8ηl), где: Q — количество жидкости, протекающей через капилляр за время t;
r, l – радиус и длина капилляра соответственно;
ΔP – разность давлений на концах капилляра.
Если жидкость течёт под действием собственного веса и измерения проводятся на одном вискозиметре, то ΔP = Δh·ρg (Δh – высота столба жидкости в приборе, ρ – плотность жидкости, g – ускорение свободного падения), величины r,l и Q являются постоянными, и решение уравнение Пуазейля относительно η, примет вид: η = К ρt, где К = πr 4 Δhg/8Ql. Величина К называется постоянной капилляра, содержится в паспорте на капилляр и может быть определена измерением продолжительности протекания через капилляр жидкости с известными плотностью и вязкостью.
Вязкость раствора полимера η всегда больше вязкости растворителя ηо, в котором он растворён. Отношение η/ηо= ηотн называется относительной вязкостью. Так как плотности разбавленных растворов мало отличаются от плотности чистых растворителей, то для них возможно определение относительной вязкости как отношения продолжительностей истечения раствора и чистого растворителя через один и тот же капилляр ηотн = t / tо. Величина относительной вязкости зависит не только от количества растворённого вещества, но и от того объёма, который оно занимает в растворе или, другими словами, от формы растворённых частиц.
При вискозиметрических измерениях используется ещё ряд показателей, связанных с продолжительностью истечения жидкости из капилляра. Важнейшие из них приведены в таблице 1.
Таблица 1. Терминология и обозначения в вискозиметрии растворов полимеров.
| Название термина | Название термина, предложенное JUPAC | Обозначение | Определение |
| Относительная вязкость | Отношение вязкостей | ηотн | t/t0 |
| Удельная вязкость | — | ηуд | ηотн — 1 |
| Приведенная вязкость | Число вязкости | ηпр | ηуд /с |
| Логарифмическая приведенная вязкость | Логарифмическое число вязкости | ηлог | ln ηотн/с |
| Характеристическая вязкость | Предельное число вязкости | [η] | (ηуд/с)с = 0 = = [lg ηотн/с]c = 0 |
Последний показатель – характеристическая вязкость или предельное число вязкости – ключевой показатель при вискозиметрическом определении молекулярной массы. Его величина определяется объёмом молекулы растворённого вещества, находящейся в предельно разбавленном растворе, когда её взаимодействие с другими молекулами этого вещества отсутствует. Этот объём зависит, в свою очередь, от молекулярной массы и строения полимера, а также от характера взаимодействия полимера с растворителем. Отсюда следует, что величина характеристической вязкости может быть определена только для конкретных пар полимер — растворитель.
Находится величина характеристической вязкости измерением относительного прироста 
где: t0 – время истечения растворителя;
t — время истечения раствора;
с – концентрация раствора в г/мл или чаще в г/100 мл.
В основе методов вискозиметрических определений молекулярной массы лежит отмеченная впервые Штаудингером пропорциональность между величиной вязкости раствора производных целлюлозы и молекулярной массой растворённого вещества. Представляя макромолекулы полимеров в растворе в форме идеально жёстких стержней, длина которых пропорциональна молекулярной массе, Штаудингер предложил выразить взаимосвязь молекулярной массы М и вязкости уравнением
Кm – константа, характерная для данного полимераналогичного ряда;
с – концентрация раствора полимера;
ηуд – удельная вязкость раствора — отношение разности вязкости раствора и растворителя
к вязкости растворителя: 

Допущение Штаудингера о вытянутой форме макромолекул в растворе справедливо в какой-то мере только для полимеров с жёсткими цепями (поливинилхлорид, целлюлоза). Гибкие же макромолекулы в растворе свёрнуты в клубки, а внутреннее трение (вязкость) существенно зависит от формы этих клубков. Поэтому использование уравнение Штаудингера в приведенном виде не может использоваться для определения молекулярной массы любого полимера. Более универсально так называемое обобщённое уравнение Штаудингера или уравнение Х.Марка, Х.Куна, Р.Хаувинка, называемое также уравнением Марка-Хаувинка или формулой Марка-Хаувинка:
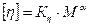
где: Кη и α – эмпирические постоянные для конкретной системы «полимер – растворитель» при определённой температуре. Определяются они независимой калибровкой для каждой пары полимер — растворитель.
Уравнение Марка-Куна-Хаувинка справедливо для большого числа полимерных веществ и является основным уравнением вискозиметрии разбавленных растворов полимеров.
В этом уравнении величина « α » характеризует форму макромолекул в растворе. Для плотных сферических клубков α = 0, для более рыхлых клубков, что наиболее характерно для большинства систем полимер – растворитель, 0,5 3 . Концентрации растворов подбираются таким образом, чтобы получаемые значения относительной вязкости изменялись в пределах 1,1 – 1,5. По полученным результатам вычисляется отношение ηуд/с (или ln ηотн/с) и строится графическая зависимость ηуд/с (или ln ηотн/с) от с 

Приведенные эмпирические соотношения между вязкостью и молекулярной массой справедливы только для линейных полимеров.
Следует отметить, что получаемые при вискозиметрических исследованиях значения молекулярных масс не всегда точны. Связано это с тем, что вязкость разбавленного раствора определяется линейными размерами макромолекулы, а размер и молекулярная масса – не одно и то же. При одинаковой молекулярной массе молекула может быть линейной и разветвлённой и если коэффициенты «а» и «К» были определены для полимера с одной степенью разветвления, а использованы для нахождения молекулярной массы другого более или менее разветвлённого полимера, то найденные значения могут быть не точными.
Химические методы определения молекулярных масс основаны на определении концентрации концевых функциональных групп.
Многие полимерные соединения содержат на концах макромолекул атомные группировки или отдельные атомы (концевые группы), которые могут быть определены химическими или физическими способами. Таковы, например, карбоксильные, гидроксильные, амидные или аминные группы, атомы галоидов и др. Полимеры, полученные методами полимеризации, могут содержать на концах цепи олефиновую связь, атомные группировки, являющиеся остатками инициаторов или регуляторов роста, атомы металлов. При известном числе таких функциональных групп в макромолекуле и знании их общего числа в растворе нетрудно вычислить число макромолекул, а, следовательно, и массовую долю групп в массе образца.

Е – химический эквивалент концевой группы;
n – число концевых групп в каждой макромолекуле.
Однако, по мере возрастания молекулярной массы полимера доля концевых групп в массе образца уменьшается и может в конце концов стать столь малой, что её экспериментальное определение с достаточной точностью станет затруднительным. Поэтому химический метод считается непригодным для полимеров с молекулярной массой свыше 30 – 50 тыс.
 |
Определение молекулярной массы полимеров химическими методами осложняется приближённостью представлений о числе функциональных групп в одной макромолекуле. Обычно число концевых групп предполагается исходя из механизма образования полимера. Например, при поликонденсации дикарбоновой кислоты и гликоля образующийся полиэфир может состоять из смеси трёх типов макромолекул:


Любой образец любого полимерного материала, даже если он получен тщательнейшим фракционированием, полидисперсен, т.е. содержит макромолекулы разных размеров. Молекулярно-массовое состояние такого образца может быть охарактеризовано с помощью кривой распределения по молекулярным массам. Вещество, кривая распределения для которого приведена на рис. 3, не содержит заметных количеств молекул с молекулярной массой менее М1 и более М2. Мmax – молекулярная масса молекул, содержание которых максимально. Все макромолекулы с промежуточными молекулярными массами присутствуют в массовых соотношениях wi, отложенных по оси ординат. Аналогично можно построить кривую распределения по числу молекул. Большинство методов определении молекулярных масс полимеров не даёт возможности получить кривую распределения, способную исчерпывающим образом описать молекулярно-массовое состояние. Они дают только средне-статистические значения молекулярных масс. Разные экспериментальные методы позволяют в зависимости от измеряемых параметров определить те или другие средние значения. В принципе, среднее значение молекулярной массы ( 
( 

Однако доля фракции в образце может определять по разным критериям. Например, по массе фракции, по числу молекул в каждой фракции, по каким-то физическим свойствам материала фракций и т.п. Наиболее распространены для характеристики молекулярных масс полимеров
три типа усреднений, предложенных В. Ленсингом и Е.Кремером: среднемассовый, среднечисловой и среднеседиментационный (z-средний). Соответственно молекулярная масса полимера представляется в виде среднемассового, среднечислового и среднесидементационного (z-среднего) значений. Широко используется также величина средневязкостной молекулярной массы.
Следует подчеркнуть, что типы усреднений увязаны с методами анализа материала фракций и использование каждого правомерно только при экспериментальном определении того критерия, по которому производится усреднение.
Среднемассовая молекулярная масса ( 



Здесь вклад в конечный результат каждой группы молекул с определённой молекулярной массой пропорционален массе этих молекул.
Значение среднемассовой молекулярной массы вычисляется как сумма произведений молекулярной массы на долю макромолекул, её имеющих, в общей молекулярной массе
Определение среднемассовой молекулярной массы производится методами, в которых измеряемый эффект пропорционален массе частиц (светорассеивания, седиментационного равновесия и, при некоторых ограничениях, вискозиметрия).
Среднечисловая (среднечисленная) молекулярная масса ( 
i — порядковый номер фракции;
ni = Ni/ΣNi — числовая доля фракции с молекулярной массой Mi в смеси.
Среднеседиментационная (z-средняя) молекулярная масса ( 
Вычисляется она на основе седиментационного равновесия при определении молекулярных масс с помощью ультрацентрифуги.
Средневязкостная молекулярная масса ( 


где: α — константа системы «полимер – растворитель», для которой определялась вязкость при определённой температуре.
Получаемые при различных методах опеделения и типах усреднения величины могут для одного и того же полимерного образца различаться в несколько раз.
1. Понятие молекулярной массы для полимерных макромолекул.
2. Дайте определение полидисперсности.
3. Причины полидисперсности.
4. Методы определения молекулярной массы
5. Суть среднемассового способа усреднения молекулярных масс полимеров.
6. Суть среднечислового способа усреднения молекулярных масс полимеров.
7. Суть средневязкостного способа усреднения молекулярных масс полимеров.
Источник












