- «Триумф онкологии». Какие лекарства успешно побеждают рак
- Долгий путь из лаборатории к пациенту
- Как заставить работать иммунитет
- Каждый шестой умирает от рака
- Методы лечения рака
- Хирургическое лечение
- Химиотерапия
- Лучевая терапия
- Гормональная терапия
- Иммунотерапия
- Таргетная терапия
- Генная инженерия в лечении онкологических заболеваний
«Триумф онкологии». Какие лекарства успешно побеждают рак
«Ученые обещают лечить рак одним уколом», «Открыто новое лекарство от рака», «Найдено универсальное средство от злокачественных новообразований» — подобные заголовки появляются в СМИ едва ли не каждую неделю. Однако врачи полагаются на давно опробованные методы: хирургическое удаление опухоли, химио- и лучевую терапию. Практически все онкологические заболевания неизлечимы. РИА Новости разбирается, куда пропадают сенсационные разработки и когда наука победит рак.
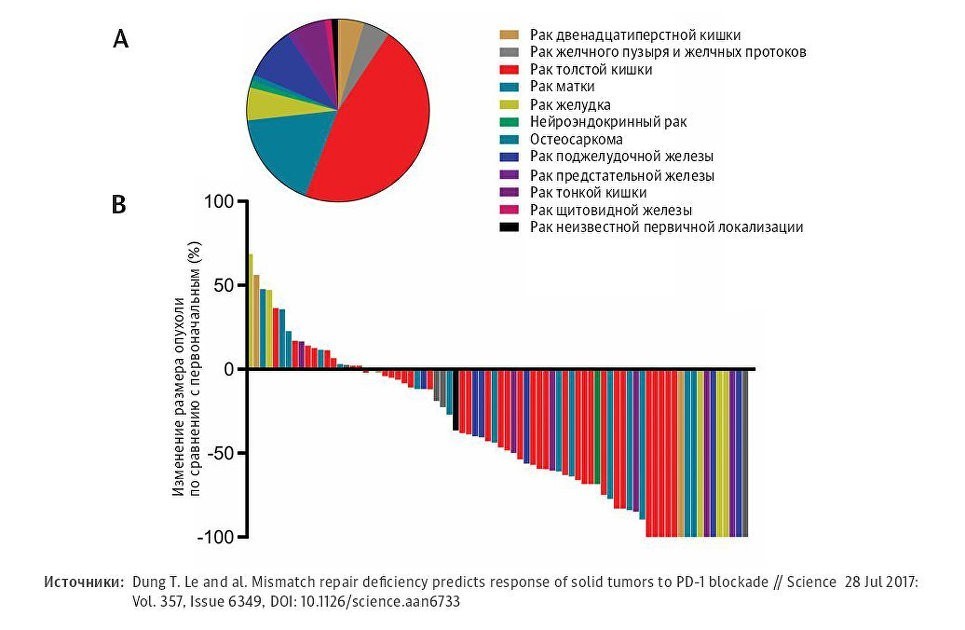
В июле прошлого года в журнале Science вышла статья, наделавшая много шума в научном мире: в результате испытаний нового противоракового препарата от онкологических заболеваний полностью вылечились два десятка человек. У всех были поражены разные органы — матка, желудок, простата, щитовидная железа.
Единственное, что объединяло пациентов, — их опухоли не отвечали на стандартное лечение из-за редких мутаций в геноме. После приема нового лекарства — моноклональных антител, помогающих иммунной системе атаковать болезнь, — 66 из 86 участников исследования почувствовали себя лучше. Их опухоли значительно уменьшились в размерах и стабилизировались, прекратив рост. Восемнадцати пациентам повезло еще больше: рак покинул их навсегда.
И хотя тестирование проходило в урезанном виде, без обязательной в таких случаях контрольной группы, принимающей плацебо, уже через год FDA, главный регулятор лекарственных средств в США, рекомендовал его для лечения сразу нескольких видов рака у детей и взрослых. По мнению специалистов, скорость, с которой была дана рекомендация, — беспрецедентная, и государство могло пойти на такие уступки только в том случае, если разработка действительно оказалась прорывной.
(А) — типы раковых опухолей, обнаруженные у участников исследования; (В) — ответ раковых опухолей на терапию пембролизумабом (результат после первых 20 недель лечения)
На самом деле этой истории почти 11 лет, ведь пембролизумаб (так назывался новый препарат) Грегори Карвен, Ханс ван Эненнаам и Джон Дулос создали в 2007 году. К испытаниям приступили только в 2013-м, а с 2018-го пациенты, страдающие агрессивными видами рака, не отвечающими на стандартную терапию, могли рассчитывать на лечение. Конечно, это состоятельные люди: один курс стоит около 150 тысяч долларов.
Долгий путь из лаборатории к пациенту
«Это долгий и сложный путь: от идеи до пациента. Все перспективные молекулы сначала тестируются на животных, потом проходят исследования с участием 10-20 пациентов, затем их число растет, счет идет на тысячи. На каждый следующий этап препарат переходит, только если продемонстрирует эффективность и безопасность на предыдущем. Это занимает годы, но защищает больных от неприятных последствий», — рассказывает Марина Секачева, руководитель Центра персонализированной онкологии, профессор кафедры онкологии Первого МГМУ им. И. М. Сеченова.
На каждом из этих этапов лекарство может быть выбраковано из-за нулевой эффективности или — еще хуже — негативного воздействия на организм пациентов. Например, в 2017 году во время клинических испытаний препарата CAR-T один из участников исследования умер. Несмотря на доказанную несколькими месяцами ранее эффективность терапии при лечении множественной миеломы и лейкемии, эксперимент был немедленно прекращен.
Похожая история произошла и с инновационным методом лечения рака ROCKET. В ходе клинических испытаний второй фазы проверяли эффективность и безопасность биопрепарата JCAR015, предназначенного для лечения рецидивирующего или устойчивого к терапии В-клеточного острого лимфобластного лейкоза. В июле 2016 года тестирование приостановили на два месяца из-за смерти трех пациентов. Спустя год от исследований лекарства и вовсе отказались, так как еще двое участников исследования скончались по одной и той же причине — отек головного мозга.
Как заставить работать иммунитет
Технология CAR предусматривает введение пациенту его собственных генно-модифицированных Т-лимфоцитов. Таким способом к лечению подключают иммунитет больного. Иммунные клетки распознают опухоль и атакуют ее. Несмотря на первые отрицательные результаты, исследования в этом направлении одобрены в некоторых странах.
«Последние пять лет в онкологии — это триумф иммуноонкологических препаратов, которые делают опухоль доступной для собственной иммунной системы пациента. И мы еще в процессе активного изучения этих лекарств: подбираем оптимальное сочетание, время назначения, последовательность; смотрим, как они влияют на хирургические результаты», — уточняет Марина Секачева.
Каждый шестой умирает от рака
Несмотря на идущую уже четыре десятилетия войну с раком, эта болезнь уносит сегодня жизнь каждого шестого обитателя планеты. По данным Всемирной организации здравоохранения, чаще всего люди погибают от рака легких (один миллион 690 тысяч смертей в год), печени (788 тысяч), толстой и прямой кишок (774 тысячи), желудка (754 тысячи) и молочной железы (571 тысяча).
Как отмечают специалисты, помимо физических канцерогенов (например, ультрафиолетового излучения) и вредных химических веществ (табак, асбест) риск заболевания повышают генетические особенности. В последние годы открыли гены, у носителей которых больше вероятность возникновения рака. С другой стороны, злокачественная опухоль часто образуется у тех, кто когда-то перенес инфекции, вызываемые некоторыми вирусами, бактериями или паразитами. Четверть онкологических заболеваний в развивающихся странах вызваны гепатитом и вирусом папилломы человека.
Ежегодный экономический ущерб от рака, по некоторым оценкам, достигает триллиона долларов. На разработку препаратов из года в год тратятся миллиарды. Однако, несмотря на все усилия, говорить о том, что в ближайшем будущем рак будет побежден, не приходится.
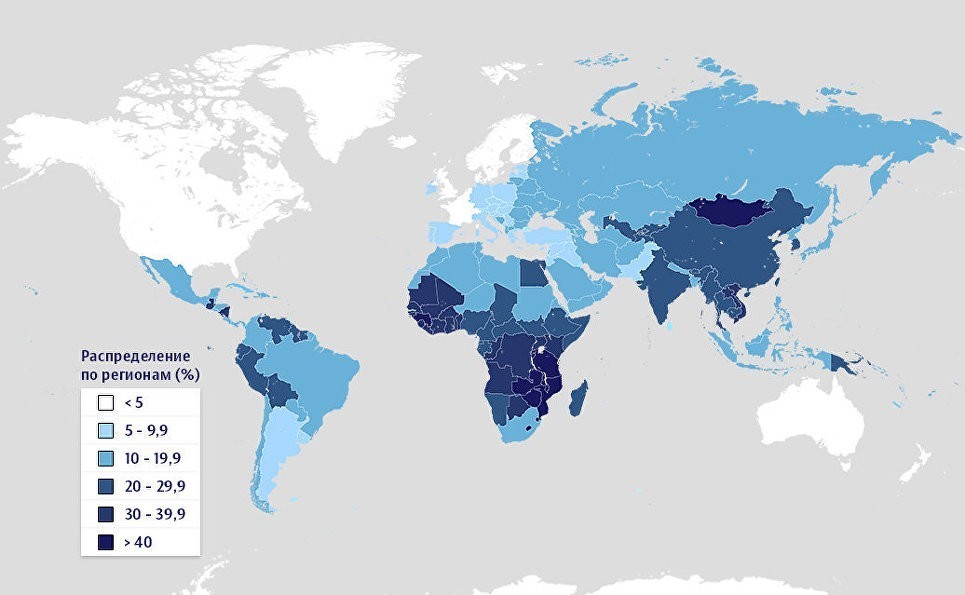
© Pathogen-Associated Malignancies Integrated Research Center, Fred Hutch
Доля онкологических больных, чья опухоль связана с перенесенными ранее инфекциями. Распределение по странам мира.
«К сожалению, человечество изобрело пока не так много лекарственных препаратов, позволяющих добиться полного излечения от того или иного недуга — главным образом, это касается инфекций. В большинстве случаев нам удается лишь перевести заболевание из смертельного или мучительного в хроническое и без выраженных симптомов. Эта тенденция прослеживается и в онкологии. В редчайших случаях лекарственная противоопухолевая терапия приводит к полному излечению, но примеров, когда удается перевести рак в длительный вялотекущий процесс, все больше. Скажем, хронический лимфолейкоз, рак молочной или предстательной железы. Мы каждый день (без преувеличения) открываем молекулярные особенности злокачественных новообразований, и это позволяет нам найти новые пути их лечения», — резюмирует онколог.
Источник
Методы лечения рака
Еще несколько лет назад диагноз «рак» зачастую звучал как приговор. Но онкология, как и любая сфера медицины, не стоит на месте. Классическая триада лечения онкологических заболеваний — хирургия, химиотерапия и лучевая терапия — сегодня дополнилась новыми методиками. Современные онкологи имеют в своем распоряжении широкий арсенал, который помогает спасать многие жизни, а в случаях, когда это невозможно — существенно продлевать жизнь пациента и избавлять от мучительных симптомов.
Врач-онколог разрабатывает программу лечения, исходя из типа, локализации, стадии опухоли, состояния здоровья больного. С пациентом работает команда специалистов, которая может включать онкологов, терапевтов, химиотерапевтов, радиологов, анестезиологов, психоонкологов, реабилитологов, хирургов-онкологов.
В данной статье будут рассмотрены основные методы лечения онкологических заболеваний, мы коротко остановимся на каждом из них и расскажем о важных моментах.
Хирургическое лечение
Во время операции хирург удаляет опухолевую ткань, пораженные близлежащие лимфатические узлы. Цели хирургического лечения могут быть разными:
- Удаление опухоли целиком.
- Удаление части опухоли (циторедуктивные операции). От рака это не излечит, но поможет повысить эффективность химиотерапии и других методов лечения.
Паллиативные операции обычно выполняют на поздних стадиях рака. Они помогают уменьшить боли, частично восстановить функции пораженного органа.
Иногда можно прибегнуть к миниинвазивному лапароскопическому вмешательству, в других случаях приходится делать большой разрез. Это зависит от размеров и локализации опухоли. При больших новообразованиях приходится удалять много тканей или даже целые части тела, например, молочную железу. В дальнейшем восстановить внешность помогают реконструктивно-пластические операции, протезы.
В случаях, когда это возможно, современные хирурги обходятся без скальпеля и прибегают к криохирургии (разрушение новообразования при помощи низкой температуры), лазерной хирургии, фотодинамической терапии (введение в опухоль специального препарата, который делает её чувствительной к свету, с последующим облучением).
Химиотерапия
Химиопрепараты уничтожают быстро делящиеся клетки. Химиотерапия может применяться как самостоятельно, так и в сочетании с другими методами, например, хирургическими вмешательствами, лучевой терапией. Химиотерапия может преследовать разные цели:
- Уменьшить опухоль перед хирургическим вмешательством или курсом лучевой терапии. В данном случае химиотерапия будет называться неоадъювантной.
- Уничтожить раковые клетки, которые остались в организме пациента после операции. Такую химиотерапию называют адъювантной.
- Повысить эффективность других методов лечения рака.
- Предотвратить рецидив после операции, лучевой терапии.
- Облегчить боль и другие симптомы, вызванные опухолью.
Химиопрепараты применяют в виде таблеток и капсул, внутривенных инъекций, также их могут вводить в организм другими способами.
Лучевая терапия
Лучевая терапия применяет ионизирующее излучение, которое, как и химиопрепараты, уничтожает быстро делящиеся клетки. Её можно использовать как для уничтожения опухоли, так и для облегчения боли и других симптомов.
Существуют две разновидности лучевой терапии:
- При внешнем облучении аппарат находится на расстоянии от пациента и посылает пучок лучей в область тела, где находится опухоль.
- При внутреннем облучении источник излучения вводят в тело пациента. Если источник излучения представляет собой твердый предмет (капсулу или ленту), такой вид лечения называется брахитерапией. В качестве источника излучения может выступать и жидкость, которую вводят внутривенно. Она распространяется по всему организму и уничтожает раковые клетки в разных органах. Такую методику используют, в частности, при раке щитовидной железы.
Лучевую терапию нередко сочетают с хирургическим лечением:
- Перед операцией она помогает уменьшить размеры опухоли.
- Во время операции хирург имеет возможность облучать опухоль непосредственно, так, чтобы лучи не проходили через кожу.
- После операции лучевая терапия помогает уничтожить оставшиеся раковые клетки.
Гормональная терапия
Рост злокачественных опухолей простаты и молочной железы сильно зависит от гормональных эффектов. Если раковые клетки имеют рецепторы к мужским или женским половым гормонам, врач назначит гормональную терапию. Препараты, которые при этом применяются, могут бороться с опухолью двумя путями:
Подавлять выработку «виновного» гормона.
«Мешать» гормонам оказывать свои эффекты, связываясь с рецепторами на поверхности раковых клеток.
Гормональную терапию очень редко назначают отдельно, чаще всего она дополняет другие виды лечения. Иногда прибегают к хирургическим вмешательствам, во время которых удаляют яичники или яички, чтобы половые гормоны в организме больше не вырабатывались.
Иммунотерапия
Раковые клетки — мастера маскировки. Они умело скрываются от иммунной системы, благодаря чему та не распознает их и не атакует. Это помогает исправить иммунотерапия. Существуют разные группы препаратов, одни из которых «помечают» раковые клетки и помогают иммунитету «увидеть» их, другие воздействуют на иммунитет, активируя его и заставляя атаковать опухоль.
Современные ученые научились редактировать гены в иммунных клетках. У пациента берут Т-лимфоциты, изменяют их гены таким образом, чтобы они могли атаковать опухоль, искусственно размножают новые клетки в пробирке и возвращают в организм.
Таргетная терапия
В последние годы ученые многое узнали о молекулярных механизмах, которые помогают раковым клеткам расти, размножаться, выживать. Новые знания помогли создать новое направление в лечении рака — таргетную терапию. У таргетного препарата всегда есть конкретная цель — специфическая молекула, которая образуется в раковых клетках и нужна для роста, выживания опухоли.
Разные таргетные препараты действуют по-разному:
- работают как препараты для иммунотерапии;
- блокируют молекулярные сигналы, которые заставляют раковые клетки бесконтрольно делиться;
- блокируют молекулярные сигналы, которые нужны для роста новых сосудов и питания опухоли;
- делают клетки опухоли чувствительными к химиопрепаратам, излучению;
- вызывают естественную гибель раковых клеток — апоптоз;
- работают как препараты для гормональной терапии.
Таргетную терапию можно применять как отдельно, так и в сочетании с другими методами лечения.
Генная инженерия в лечении онкологических заболеваний
Несмотря на то, что за последние годы онкология шагнула далеко вперед, перед ней стоит еще много проблем. Даже современные методы лечения не всегда оказываются эффективными. Ученые постоянно ищут новые пути.
Например, в октябре 2016 года китайские ученые сообщили о том, что впервые применили новую технологию редактирования генома у пациента, страдающего раком легкого с метастазами. Исследователи взяли у мужчины лейкоциты и при помощи системы CRISPR-cas9 отредактировали в них гены, которые мешают иммунной системе атаковать опухоль. «Исправленные» клетки размножили в лаборатории и вернули обратно в организм больного. Если испытание увенчается успехом, аналогичный метод применят для лечения рака мочевого пузыря, почек, предстательной железы.
Много лет назад ученые обнаружили, что в геноме бактерий есть странные повторяющиеся последовательности. Долгое время считалось, что они «лишние» и не выполняют никаких функций. Но потом обнаружилось, что эти последовательности — копии генов фагов, которые поражают бактериальные клетки, и они работают как аналог иммунитета у человека. Когда соответствующий фаг инфицирует бактерию, она распознает его с помощью системы CRISPR-Cas и активирует фермент, который «разрезает» ДНК фага, тем самым инактивируя его.
Ученые обнаружили, что в лаборатории с помощью CRISPR-Cas можно разрезать любые гены в нужном месте. Был открыт относительно простой, быстрый и недорогой метод редактирования генов. Он нашел применение во многих сферах, в том числе в онкологии. С помощью CRISPR-Cas изучают гены, ответственные за развитие злокачественных опухолей, создают новые лекарственные препараты, модифицируют иммунные клетки таким образом, чтобы они могли распознавать и атаковать раковые клетки. Несколько клинических исследований проводится прямо сейчас.
В 2016 году онкологам из США впервые удалось вылечить женщину от рака молочной железы IV стадии с помощью адаптивной T-клеточной иммунотерапии. 46-летняя Джуди Перкинс перенесла несколько курсов химиотерапии, но лечение оказалось безуспешным, опухоль продолжала прогрессировать, появились метастазы в печени.
Специалисты из Национального института рака (NCI) в Мэриленде решили применить у пациентки инновационный метод лечения, который ранее хорошо зарекомендовал себя в борьбе с меланомой. Из ее крови извлекли T-лимфоциты, «обучили» их атаковать раковые клетки и ввели обратно в организм. Предварительно было проведено секвенирование генома опухолевых клеток, чтобы выявить произошедшие в них мутации. На основе этой информации были отобраны подходящие T-клетки.
В результате у женщины наступила ремиссия. В 2018 году ученые сообщили, что в ее организме вот уже два года не обнаруживаются признаки присутствия злокачественной опухоли. До этого врачи говорили, что Джуди осталось жить не более трех лет.
Такое лечение все еще носит характер экспериментального. Оно не до конца изучено, есть много сложностей с его внедрением. Например, при использовании T-клеточной терапии невозможно создать «универсальные» T-клетки, которые помогали бы всем больным, для каждого пациента их нужно «обучать» персонально, с учетом мутаций, обнаруженных в конкретной злокачественной опухоли. Это стоит очень дорого. Но прогресс не стоит на месте. Кто знает, как изменится ситуация в будущем. Ведь уже сегодня стало реальностью то, что десятилетия назад считалось чем-то из разряда научной фантастики.
Лечащему врачу можно и нужно задавать вопросы. Когда пациент хорошо информирован, это идет на пользу лечению. Спросите онколога о том, какие виды лечения вам будут назначены, как будут проходить процедуры, на какой результат можно рассчитывать, какие возможны побочные эффекты, как их предотвратить и как с ними справиться. Врачи «Евроонко» применяют весь арсенал методик, которые на данный момент доступны в России. Мы постоянно следим за инновациями.
Источник