- Как исходя из метана, двумя различными способами получить этан? Напишите уравнения реакции, которые необходимо осуществить
- Описание и исходные данные задания, 50% решения + фотография:
- Как получить этан двумя способами
- Содержание
- Физические свойства [ править | править код ]
- Строение [ править | править код ]
- Получение [ править | править код ]
- В промышленности [ править | править код ]
- В лабораторных условиях [ править | править код ]
- Химические свойства [ править | править код ]
- Применение [ править | править код ]
- Физиологическое действие [ править | править код ]
- Интересные факты [ править | править код ]
- Другие вопросы из категории
- Читайте также
Как исходя из метана, двумя различными способами получить этан? Напишите уравнения реакции, которые необходимо осуществить






Чтобы получить решение , напишите мне в WhatsApp , оплатите, и я Вам вышлю файлы.
Кстати, если эта работа не по вашей теме или не по вашим данным , не расстраивайтесь, напишите мне в WhatsApp и закажите у меня новую работу , я смогу выполнить её в срок 1-3 дня!
Описание и исходные данные задания, 50% решения + фотография:
Как исходя из метана, двумя различными способами получить этан? Напишите уравнения реакции, которые необходимо осуществить.
Решение:
| Если вам нужно решить химию, тогда нажмите ➔ помощь по химии. |
| Похожие готовые решения: |
- Из ацетилена объемом 3,36л получили бензол объемом 2,5мл. Определите выход продукта, если плотность бензола равна 0,88г/мл
- Напишите уравнения реакций с помощью которых можно осуществить следующие превращения: H2SO4(конц), 180-200С
- При сжигании 11 г. этаналя выделилось 298,11 кДж теплоты. Составьте термохимическое уравнение этой реакции
- Напишите структурные формулы соединений по их названиям: 4-метилпентин-2 1,2-дибромбутан 2-метил-3-этилпентанол 1,3-диметилбензол
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
Источник
Как получить этан двумя способами
Эта́н (лат. ethanum ), C 2 H 6 — органическое соединение, второй член гомологического ряда алканов. Газ без цвета и запаха. В промышленности этан получают из природного газа и нефти и расходуют преимущественно для производства этилена.
Содержание
Физические свойства [ править | править код ]
Этан при н. у. — бесцветный газ, без запаха и вкуса. Молярная масса — 30,07. Температура плавления −183,23 °C, температура кипения −88,63 °C. Плотность ρгаз.=0,001342 г/см³ или 1,342 кг/м³ (н. у.), ρжидк.=0,561 г/см³ (T=-100 °C). Давление паров при 0 °C — 2,379 МПа. Растворимость в воде — 4,7 мл в 100 мл (при 20 °C), в этаноле — 46 мл в 100 мл (при 0 °C), хорошо растворяется в углеводородах. Точка вспышки у этана равна –187,8 °C, температура самовоспламенения — 595 °C. Этан образует с воздухом взрывоопасные смеси при содержании 5–15 об. % (при 20 °C). Октановое число —120,3 [2] [3] [4] .
Строение [ править | править код ]
Молекула этана имеет тетраэдрическое строение: атомы углерода являются sp 3 -гибридными. Связь C–C образована перекрыванием sp 3 -гибридных орбиталей, а связь C–H — перекрыванием sp 3 -гибридной орбитали углерода и s-орбитали водорода. Длина связи C–C равна 1,54 Å, а длина связи C–H равна 1,095 Å [5] .
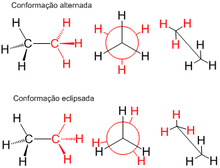
Поскольку С–С-связь в этане одинарная, вокруг неё возможно свободное вращение метильных групп. При вращении возникают различные пространственные формы молекулы этана, которые называются конформациями. Конформации принято изображать в виде перспективного изображения (такие изображения иногда называют «лесопильными козлами») либо в виде проекций Ньюмена [5] .
Число конформаций для этана бесконечно, однако принято рассматривать две крайние конформации:
- заслонённую, в которой атомы водорода максимально сближены в пространстве;
- и заторможенную, в которой атомы водорода максимально удалены [5] .
Заслонённая конформация имеет наибольшую энергию из всех конформаций, а заторможенная — наименьшую, то есть является наиболее энергетически выгодной и, следовательно, более устойчивой. Разница энергии между этими конформациями равна 2,9 ккал/моль. Считается, что это число отражает торсионное напряжение в менее выгодной заслонённой конформации. Если разделить эту энергию на три взаимодействия между парами атомов водорода, то энергия торсионного взаимодействия двух атомов водорода составит примерно 1 ккал/моль [5] .
По значению 2,9 ккал/моль из уравнения Гиббса можно вычислить константу равновесия между двумя конформациями этана. При температуре 25 °С значительно преобладает заторможенная конформация: 99 % молекул этана находятся в этой конформации и лишь 1 % — в заслонённой [5] .
Энергии крайних и промежуточных конформаций принято представлять в виде циклических графиков, где по оси абсцисс отложен торсионный угол, а по оси ординат — энергия.
Получение [ править | править код ]
В промышленности [ править | править код ]
В промышленности получают из нефтяных и природных газов, где он составляет до 10 % по объёму. В России содержание этана в нефтяных газах очень низкое. В США и Канаде (где его содержание в нефтяных и природных газах высоко) служит основным сырьём для получения этилена [6] . Также этан получают при гидрокрекинге углеводородов и ожижении углей [7] .
В лабораторных условиях [ править | править код ]
В 1848 году Кольбе и Франкленд впервые синтетически получили этан, обработав пропионитрил металлическим калием. В 1849 году они получили этот газ электролизом ацетата калия и действием цинка и воды на иодэтан [8] .
В лаборатории этан можно получить несколькими способами:
- из иодметана по реакции Вюрца;
2 C H 3 I + 2 N a → C H 3 C H 3 + 2 N a I I+2Na
ightarrow CH_ CH_ +2NaI>>>
- из ацетата натрия по реакции Кольбе;
C H 3 C O O − − e − → C H 3 C O O ⋅ → C H 3 ⋅ + C O 2 COO^ -e^
ightarrow CH_ COOcdot
ightarrow CH_ cdot +CO_ >>>
ightarrow CH_ CH_ >>>
- взаимодействием пропионата натрия с щёлочью;
C H 3 C H 2 C O O N a + N a O H → C H 3 C H 3 + N a 2 C O 3 CH_ COONa+NaOH
ightarrow CH_ CH_ +Na_ CO_ >>>
- из этилбромида гидролизом соответствующего реактива Гриньяра;
C H 3 C H 2 B r + M g → C H 3 C H 2 M g B r CH_ Br+Mg
ightarrow CH_ CH_ MgBr>>>
ightarrow CH_ CH_ +MgOHBr>>>
- гидрированием этилена (над Pd) или ацетилена (в присутствии никеля Ренея) [3] .
C H 2 C H 2 + H 2 → C H 3 C H 3 CH_ +H_
ightarrow CH_ CH_ >>>
ightarrow CH_ CH_ >>>
Химические свойства [ править | править код ]
Этан вступает в типичные реакции алканов, прежде всего реакции замещения, проходящие по свободнорадикальному механизму. Среди химических свойства этана можно выделить:
- термическое дегидрирование при 550-650 °C с образованием этилена;
- дальнейшее дегидрирование выше 800 °C, приводящее к ацетилену (в этой реакции также получаются бензол и сажа);
- хлорирование при 300-450 °C с образованием этилхлорида;
- нитрование в газовой фазе с образованием смеси нитроэтана и нитрометана (3:1) [3] .
Применение [ править | править код ]
Основное использование этана в промышленности — получение этилена методом парового крекинга. Именно из этилена далее получают важные промышленные продукты, однако в целях экономии разрабатываются методы превращения в них самого этана. Однако ни один из проектов пока не прошёл пилотную стадию. Проблемы в этой области связаны с низкой селективностью реакций. Одним из перспективных направлений является синтез винилхлорида напрямую из этана. Также применяется превращение этана в уксусную кислоту. Термическим хлорированием этана в различных условиях получают хлорэтан, 1,1-дихлорэтан и 1,1,1-трихлорэтан [7] .
Физиологическое действие [ править | править код ]
Этан обладает слабым наркотическим действием (ослаблено за счёт низкой растворимости в жидкостях организма). Класс опасности — четвёртый [9] . В концентрациях 2-5 об. % он вызывает одышку, в умеренных концентрациях — головные боли, сонливость, головокружение, повышенное слюноотделение, рвоту и потерю сознания из-за недостатка кислорода. В высоких концентрациях этан может вызвать сердечную аритмию, остановку сердца и остановку дыхания. При постоянном контакте может возникнуть дерматит. Сообщается, что при 15-19 об. % этан вызывает повышение чувствительности миокарда к катехоламинам [10] .
Интересные факты [ править | править код ]
Предположительно, на поверхности Титана (спутник Сатурна) в условиях низких температур (−180 °C) существуют целые озёра и реки из жидкой метано-этановой смеси [11] .
| Вопрос-Ответ → Раздел «Химия, биология, медицина» → Тема «Арены помогите пожалуйста осуществить превращения» |
| 1. | PolikarpovaTV |
| 2. | UrrutiaML |
| 3. | MasalkinaNN |
| 4. | HuzyagaleevNK |
| 5. | MuginevaRO |
| 6. | GorbunovSV4 |
| 7. | DrozdovNA |
| 8. | LevochkinaNV |
| 9. | KozinaEN |
| 10. | MashkovSA |
| 11. | AmosovBA |
| 12. | HrychevaAD |
| 13. | SmirnovUB |
| 14. | HaritonovVS |
| 15. | ErmilovMM |
| 16. | KatinaAV2 |
| 17. | KibasovaMB |
| 18. | KovalevaPI |
| 19. | LuhovtsevaEV |
| 20. | GitermanMYa |
| 21. | BulatkinUS |
| 22. | BudnikovaTK |
| 23. | MiroshnichenkoNN2 |
| 24. | LutsenkoEV4 |
| 25. | GilmutdinovRZ |
| 26. | TerentevDA |
| 27. | KonyuhovaEA |
| 28. | ZarifyanSE |
| 29. | MedvedevFA |
| 30. | GospodarikovAA |
| 31. | ErmakovaTG |
| 32. | Наталья |
1. Карбид кальция —» метан—> ацетилен —> бензол —> толуол —>—> бензойная кислота.
2. Метан —> ацетилен —> бензол —> бромбензол —> толуол —»—>2,4,6-тринитротолуол.
3. Этилен —> этан —> 1,2-дибромэтан —> этин —» бензол —> гек-сахлорциклогексан.
4. Гексан —> пропан —»гексан —> бензол —> хлорбензол —» толуол.
5. Этилен —> 1,2-дихлорэтан —» ацетилен —> бензол —> нитробензол —> азот.
6. Бензол —> оксид углерода (IV) —> карбонат кальция —> карбид кальция —> бензол —> циклогексан.
7. 1,6-дихлоргексан —> циклогексан —> бензол —> хлорбензол ->—> толуол —> оксид углерода (IV).
8. Пропан —> гексан —> циклогексан —> бромбензол —> метил-бензол —» 1-метил-2,4,6-тринитробензол.
1.метана
2.пропионата натрия
3.хлорэтана
4.этилового спирта
из пропионата натрия
Другие вопросы из категории
граммов 40 %-ного раствора щелочи потребуется для этой реакции? ОТВЕТ: 44,8 л, 280 г Заранее спасибо.
Читайте также
75% оксида вольфрама WO3 3)Руда массой 15кг содержит минералы: 20% — хромового ангидрида CrO3 и 25% оксида хрома ( III ) Cr2O3. Определить массу хрома, которую можно получить из этой руды P.S. Помогите решить хотя бы два задания
граммов 40% раствора щёлочи можно получить из Na , m которого вы получили в 1)
2) Какую массу соли можно получить при взаимодействии 4,32 г алюминия и 21,3 г хлора?
3) Какой объём воздуха (нормальные условия) израсходуется для сжигания 13,6 г фосфина? Объёмная доля кислорода в воздухе 21%.
применение для отбеливания и удаления пятен с белых из хлопчетобумажных и льняных тканей,мытья и дезинфекции посуды,керамической плитки, изделий из пластика и фаянса.
При нагревании препарата происходит разложение гипохлорида натрия. Одним из продуктов реакции является кислород.Скорость реакции разложения гипохлорида натрия резко возрастает при добавлении свежеосаженного гидроксида кольбата(III)Причём гидроксид кольбаната(III) можно использовать для разложения отбеливающего средства многократно.
а).Запишите уравнение реакции разложения гипохлорида натрия.
б).Какой обьём кислорода (н.у.)можно получить из 200г препарата «Белизна»,если извесно, что массовая доля гипохлорида натрия в препарате составляет 7%?
в). Какую роль выполняет гидроксид колбата (III) в данной реакции?
колчедана при выходе 90%, 3)Из природной серы с примесью, составляющей 20%, получают 448 л (н. у.) сернистого газа. Сколько природной серы расходуется при этом?
Источник