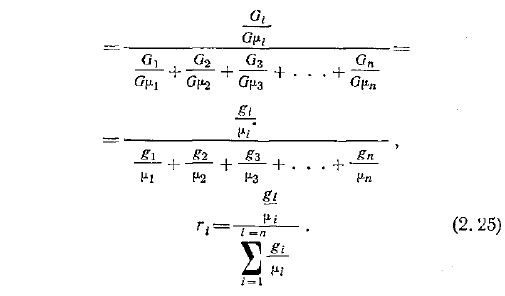Газовая постоянная смеси газов.







Газовая постоянная смеси газов.
- Газовая постоянная смешанного газа Смешанный газ следует уравнению состояния-pV = mRT и R = pV / mT. Из Формулы (3-2″) n = gtRi / R и 2G / = ZgiRi / R = 1, из которых^ Р = организации стандартов Ирана ’= ^ + g2R2 + … + гнрн. ■(3-3)) Газовая постоянная смешанного газа равна сумме массовой доли каждого газа и произведения этой
газовой постоянной. Еще одно уравнение, определяющее газовую постоянную смеси Р = 2giRi-Ф 8314.2(г,/ ^ + ГДж <он + … + г меня. по известной средней молекулярной массе смеси. Людмила Фирмаль
отдельных газов определяется тем же уравнением, но там вводится фактическая молекулярная масса каждого газа. Если указан объемный состав смеси, (3-2 ’) gi =(RiRiYi и Xg,= RZn / Rt = 1. И затем… R—V = 1 KrJR, + rJR,+; • • + rn! Дипломированная медсестра.) •(3-6))Средняя молекулярная масса газовой смеси Средняя молекулярная масса является условной величиной, которая относится
к однородному газу, в котором число молекул и общая масса равны числу молекул и массе смешанного газа. Если известна газовая постоянная смеси、 С-8314.2 / Р•. (3-7) И. Я — = 8314.2%/?+ 2 + … + gntfn). Газовая постоянная Rlt R2t …Заменив Rn величиной из уравнения Клапейрона, получим формулу средней молекулярной массы, если смесь задана массовой долей. \ х = л / (&//ИИ + gjpt + … + W-(3: 8) Если
- смесь указана в объемной доле, то из Формулы (3-6): Р = H2rJRi = 8314.2 / 2rf | если. С / ? ’8 314,2 / Форекс ’ И затем… •[Л= Srijij = rjfij +Г2[Л2+ … +Гпсп. (3-9) Средняя молекулярная масса газовой смеси равна сумме продуктов объемной доли по молекулярной массе отдельных газов, входящих в состав смеси.Парциальное давление Если известны основные параметры газа, то парциальное давление
газа можно определить по массовой доле уравнения Клапейрона. Л = п =(3-10) В. г-н р. Привет.. чтобы найти парциальное давление каждого газа при определении смеси по объемной доле. ПТВ = ПВЛ и Pi = Р ^ = РТП. (3-11) Парциальное давление каждого газа равно произведению полного давления смешанного газа на объемную долю. Формула (3-
Вы можете использовать закон Бойля-Марриотта Людмила Фирмаль
11)обычно используется при техническом расчете и испытаниях теплового оборудования. Объемная доля газа определяется специальным прибором — газоанализатором. Управление вопросами и примерами в главе 3 1.Что такое смешанный газ? 2.Дайте Далтону формулировку закона. • * 3.Что называется парциальным давлением?
4.Что называется массой, объемом и молярной долей? 5.Так называемая частичная, или. Ты убавил громкость? Какова связь между удельным объемом, плотностью, молекулярной массой и постоянной газа? 7.Почему молекулярная масса смеси называется средней молекулярной массой? * 8.Как. Пересчет массового состава в объем и пересчет объема в объем? 9., Как определяется газовая
постоянная смеси по массовой доле и объемной доле? — В J0.Как парциальное давление газа в смеси определяется массовой долей и объемной долей? 11.Как определяется средняя молекулярная масса смеси газов? Пример 3-1.Если мы предположим, что объем сухого воздуха составляет 21% 02 и 79% N2, мы получим среднюю молекулярную массу сухого воздуха. По Формуле (3-9)、 = РЛ \ іх +
r2fx3= 32-0.210 + 28.016-0.79 = 28.93 Пример 3-2 определяет газовую постоянную, плотность и парциальное давление смеси, состоящей из 20 массовых долей воздуха и 1 массовой доли легкого газа. Плотность легкого газа при температуре 273°К и давлении 101325 ″ Li2 ″ равна 0,52 кг Газовая постоянная легкого газа определяется по формуле Клапейрона. U1325 = 7и Джей!(Кг-град). J 0,52-273 В и’
Газовая постоянная воздуха составляет 287.04 Дж! Это хорошая идея. Газовая постоянная смешанного газа определяется по формуле (3-3): R = + g2R2= 287.04-20 / 21 + 714-1 / 21 = 306.3 j /(кг> град). Плотность смеси определяется уравнением Клапейрона: p = p / RT = 101325:306,30-273 = 1,21 кг / М9.Парциальное давление определяется по формуле (3-11). = 101325 — = 90100 nCl \ Ри Р. 21,306. 3 ′ Парциальное давление газа лампы = = — — — — ^- =11225 Н(м \ G2 G62 I 21 306.30





















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Источник
Способы задания состава газовой смеси
Способы задания состава газовой смеси
- Газовая постоянная, содержащаяся в формуле Клапейрона, может быть определена по формуле 2.12 только в том случае, если молекулярная масса газа равна p. молекулярная масса химически чистого газа может быть легко вычислена, если химическая формула газа равна. Сделайте это, суммируя атомные массы всех химических элементов, составляющих молекулу газа, с учетом количества элементарных атомов в молекуле газа. molecule.
Например, молекулярная масса углекислого газа CO2 Co, — s 2p-0 12 2 1 b-44 кг I кмоль. Однако в теплотехнических расчетах чаще всего приходится работать со смесями, состоящими из нескольких газов, а не с чистыми газами. Это воздух, содержащий азот, кислород, аргон, углекислый газ, водяной пар, продукты сгорания топлива или другие mixtures. In в этом случае, зная состав смеси, необходимо уметь определять молекулярные свойства смеси относительную молекулярную массу и газовую постоянную. Состав смеси может быть определен по массе, объему или молярной доле. Установите смесь в массовую долю. Массовая доля газа в смеси — это отношение массы конкретного газа к массе всей смеси.
В особых условиях (например, при измерении температуры газа в печах) для уменьшения погрешностей экранировки недостаточно. Людмила Фирмаль
Смесь газов с массой 6 масса 32, p 7н-массовая доля этих газов 2.17 Смесь com — л. Где ez, y P-массовая доля газа c — общая масса смеси, равная сумме масс центнера. О О1 О2 63. гол-2 1-1 Сумма всех массовых долей всех компонентов равна 1. 1-р 2 3 е 1-1 1 Установите смесь по объемной доле. Объемная доля газа в смеси — это отношение приведенного объема компонента к объему всей смеси. Уменьшенный объем — это объем, который занимали компоненты смеси до смешивания, и находится при том же давлении и температуре, в которых находится смесь. Сумма всех объемов, которые появляются, будет равна общему объему смеси. л 21 г- I-1 Подобный этому рН — , 2.18 Совместное использование компонентов.
- Где РТ Р2, Р3,. , ha объем И e 2, V3 уменьшенный объем компонента l3. Y — общий объем для смеси. Сумма объемных долей всех компонентов равна 1. 1 — н Г −24-2424-Х3. — — 2Г 1- г 1 Установите состав смеси с мольной фракцией. Молярная доля газа в смеси — это отношение молярного числа конкретного газа к общему молярному числу всех газов в смеси. Молярное число газа может быть определено параметрами P и T, путем деления массы газа на его молекулярную массу или объема восстановленного газа на молярный объем. М — кмоль, 2.19 Д 1 ххол. 2. Двадцать 1 гр. В Формуле 2.20 обозначение компонента I не присваивается количеству.
Это связано с тем, что это количество одинаково для всех газов, согласно закону Авогадро. Поэтому молярная доля выражается соотношением Л1 Здесь, через L4, указывается общее количество молей всех компонентов. В идеальной смеси газов объем и молярные доли будут равны друг другу. Согласно уравнению 2.21, подставим число молей, выраженное в объеме согласно уравнению 2.20. Умножение на Л. Все члены числителя и знаменателя значение дроби не изменяется ВИ, ВИ, ВИ гр 2.22 У1 2 Ч-Уд В 2 Часто состав смеси задается в 1 доле например, по массе, но нужно знать состав других долей например, по объему.
Уравнение (14-40) показывает, что для уменьшения ошибки надо, чтобы все члены уравнения, относящиеся к излучению, были малы. Людмила Фирмаль
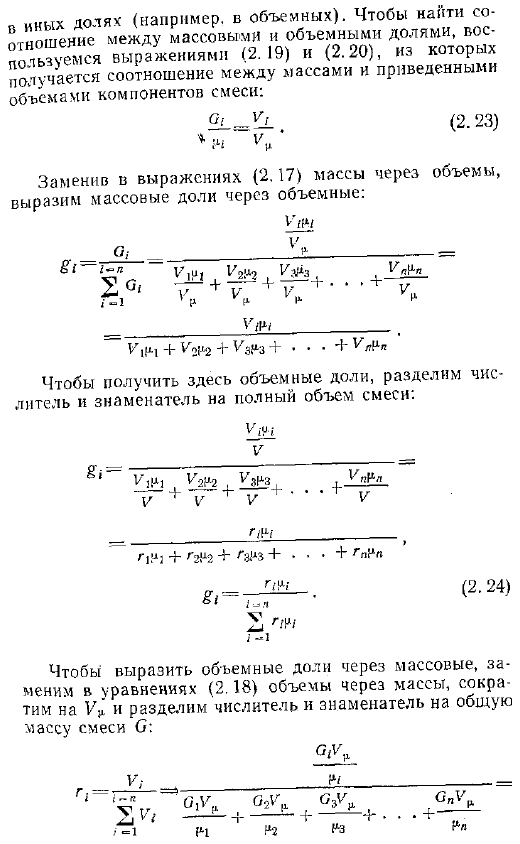
Чтобы найти соотношение массовой доли и объемной доли, по уравнениям 2.19 и 2.20 получаем соотношение между массой и уменьшающимся объемом смешиваемого компонента. Да. ч у Если заменить массу в Формуле 2.17 на объем, то по объему мы будем представлять массовую долю. ыы В П. U lnl В — В Г Лодзь. 2.23 2. , 4 г 3Н-Е Л Х Чтобы получить здесь объемную долю, разделите числитель и знаменатель на общий объем смеси. У В 1ч. 1, Ch2r 2 Ulns, D. В В В — В ЦУП Г Гг21 2 гэнз глг п 2.24 Чтобы выразить объемную долю по массе, в Формуле 2.18 уменьшите объемную долю на 1U и разделите числитель и знаменатель на общую массу смеси О о ХДС В середине 11 ода ый, ый, rSp1Y я н 0 1 Л 1ч 2. 3.





















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Источник