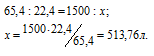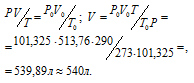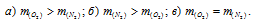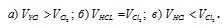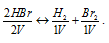- Алгоритм решения задач на определение состава газовых смесей
- Дистанционное обучение как современный формат преподавания
- Методическая работа в онлайн-образовании
- Современные педтехнологии в деятельности учителя
- Оставьте свой комментарий
- Безлимитный доступ к занятиям с онлайн-репетиторами
- Подарочные сертификаты
- Решение задач на газовые смеси | Закон Авогадро
- Задачи на тему «Агрегатные состояния вещества»
Алгоритм решения задач на определение состава газовых смесей
Определение состава газовых смесей
ЗАДАЧА: Плотность газовой смеси, состоящей из водорода и гелия, по воздуху составляет 0,1. Определите объемную долю этих газов в исходной смеси.
1.Находим среднюю молярную массу смеси газов: М (смеси) = D возд (смеси)×М(возд) = 0,1×29 = 2,9(г/моль) 2.Вычисляем объемную долю водорода в смеси. Пусть x —объемная доля водорода в смеси, φ( H 2 )= x , тогда (1- x )—объемная доля гелия в смеси, φ ( He )= 1- x по формуле М (смеси) = φ( H 2 ) ×М( H 2 ) + φ ( He ) ×М( He ) 2,9= x ×2 + (1- x ) × 4 откуда x =0,55 или x =55% φ ( He )=1-0,55=0,45 или 45%
1. Находим среднюю молярную массу смеси газов: М (смеси) = D возд (смеси)×М(возд) = 0,1×29 = 2,9(г/моль) 2. Составляем схему «правила креста» и находим объем газовой смеси:
3.Определяем объемную долю водорода и гелия в смеси:
φ (He)= =0,9/2=0,45 или 45%
Смесь азота и оксида углерода ( IV ) объемом 14л (н.у.) имеет массу 25,5г. Определите объемную, мольную и массовую доли азота в смеси.
1.Находим количество вещества газовой смеси: υ (смеси) = =14/22,4=0,625(моль ) 2.Вычисляем среднюю молярную массу смеси: М (смеси) = = 25,5:0,625= 40,8(г/моль)
3. Находим объемную долю азота в смеси: Пусть x —объемная доля азота в смеси, φ( N 2 )= x , тогда
(1- x )—объемная доля оксида углерода( IV ) в смеси, φ ( CO 2 )= 1- x по формуле М (смеси) = φ( N 2 ) × М( N 2 ) + φ ( CO 2 ) × М( CO 2 )
40,8= x ×28 + (1- x ) × 44 откуда x =0,2 или x =20% φ( N 2 )=20% φ ( CO 2 )=1-0,2=0,8 или 80%
4. Определяем мольную долю азота в смеси. По закону Авогадро объемная доля газа в смеси равна его мольной доле, поэтому φ( N 2 )= χ( N 2 )=0,2 или 20%
5. Вычисляем массовую долю азота в смеси, на основе формулы χ( N 2 )= υ( N 2 )/ υ (смеси) находим количество вещества азота
υ( N 2 ) = χ( N 2 ) × υ (смеси) =0,2×0,625=0,125 (моль), тогда m ( N 2 )= υ( N 2 ) × M ( N 2 )= 0,125×28=3,5(г) ω( N 2 )= = 3,5/25,5=0,137 или 13,7%
Все эти действия можно объединить одной формулой ω( N 2 )= = 0,2 × 0,625 × 28/25,5=0,137
или ω( N 2 )= = 0,2 × 28/40,8 = 0,137 или 13,7%
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 801 человек из 76 регионов
Курс профессиональной переподготовки
Методическая работа в онлайн-образовании
- Сейчас обучается 24 человека из 13 регионов
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
- Курс добавлен 23.09.2021
- Сейчас обучается 46 человек из 23 регионов
Ищем педагогов в команду «Инфоурок»
Номер материала: ДБ-054163
Международная дистанционная олимпиада Осень 2021
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Безлимитный доступ к занятиям с онлайн-репетиторами
Выгоднее, чем оплачивать каждое занятие отдельно
Шойгу предложил включить географию в число вступительных экзаменов в вузы
Время чтения: 1 минута
Рособрнадзор откажется от ОС Windows при проведении ЕГЭ до конца 2024 года
Время чтения: 1 минута
Минпросвещения будет стремиться к унификации школьных учебников в России
Время чтения: 1 минута
Попова предложила изменить школьную программу по биологии
Время чтения: 1 минута
В Минпросвещения предложили организовать телемосты для школьников России и Узбекистана
Время чтения: 1 минута
Минпросвещения разрабатывает образовательный минимум для подготовки педагогов
Время чтения: 2 минуты
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Источник
Решение задач на газовые смеси | Закон Авогадро
Задача 71.
При прохождении смеси равных объемов SO2 и О2 через контактный аппарат 90% молекул SO2 превращается в SO3. Определить состав (в процентах по объему) газовой смеси, выходящей из контактного аппарата.
Решение:
Уравнение реакции горения сернистого газа имеет вид:
Из уравнения реакции вытекает, что из двух молекул SO2 и одной молекулы O2 образуются две молекулы SO3. Известно, что из каждого литра SO2 превратилось в SO3 0,9л, при этом образовалось тоже 0,9л SO3. Кислорода на каждый литр прореагировало соответственно 0,45л О2 (0,9/2 = 0,45).
Таким образом, выходящая смесь газов из контактного аппарата, на каждый литр смеси состояла из 0,1л SO2 (1 – 0,9 = 0,1) и 0,55л О2 (1 – 0,45 = 0,55). Общий объём смеси, выходящей из контактного аппарата, составляет 1,55л (0,1 + 0,55 + 0,9 = 1,55).
Задача 72.
Смесь, состоящая из трех объемов Сl2 и одного объема H2, оставлена в закрытом сосуде на рассеянном свету при постоянной температуре. Через некоторое время содержание Сl2 в смеси уменьшилось на 20%. Изменилось ли давление в сосуде? Каков процентный состав смеси по объему?
Решение:
Уравнение реакции взаимодействия хлора с водородом имеет вид:
При взаимодействии одного моля хлора с одним моль водорода образуется два объёма хлороводорода, т. е. реакция идёт без изменения объёма. При нормальных условиях из трёх литров хлора в реакцию вступило 0,6л (3 . 0,2 = 0,6). Точно такое же количество водорода тоже вступило в реакцию. Таким образом, при взаимодействии 0,6л хлора и 0,6л водорода образовалось 1,2л хлороводорода (2 . 3 = 0,6). Так как реакция идёт без изменения объёма, то давление в системе тоже не изменится.
Находим процентный состав газовой смеси по формуле:
Ответ: не изменилось;

Задача 73.
При взаимодействии NН3 с Сl2 образуются хлороводород и азот. В каких объемных соотношениях взаимодействуют NH3 и С12 и каково отношение объемов получающихся газов?
Решение:
Уравнение реакции взаимодействия аммиака с хлором имеет вид:
При взаимодействии аммиака с хлором из каждых двух объёмов аммиака и трёх объёмов хлора образуются шесть объёмов хлороводорода и один объём азота. Таким образом, аммиак и хлор взаимодействуют в объёмных отношениях 2 : 3 (2VNH3 : 3VCl), а отношение объёмов получающихся газов – 1 : 6 V(N2 : V(HCl).
Ответ: V(NH3) : V(Cl2) = 2 : 3; V(HCl) : V(N2) = 6 : 1.
Задача 74. Какой объем Н2 (при 17 °С и давлении 102,4кПа) выделится при растворении 1,5кг цинка в соляной кислоте?
Решение:
Уравнение реакции имеет вид:
Зная мольную массу цинка (65,4г/моль) и мольный объём газа (22,4л), находим объём водорода, который выделится при растворении 1,5кг цинка из пропорции:
Затем приводим полученный объём к указанным условиям используя объединённое уравнение закона Бойля- Мариотта и Гей-Люссака, находим V0:
где P и V — давление и объём газа при температуре T = 290К (273 +17 = 290); P0 = 101,325 кПа; T0 = 273 К; P = 102,4 кПа; V0 -объём газа (н.у.) = 513,76 л.
Ответ: 540л.
Задача 75.
После взрыва смеси, состоящей из одного объема исследуемого газа и одного объема Н2, получился один объем водяного пара и один объем азота. Все измерения производились при одинаковых условиях. Найти формулу исследуемого газа.
Решение:
Молекулярная формула воды H2O, а азота – N2. Так как продукты реакции и исходные вещества состоят из одинаковых объёмов, то, учитывая, что образуются по одной молекуле воды и азота из одной молекулы водорода и одной молекулы исследуемого газа, можно предположить, что молекула исследуемого газа состоит из двух атомов азота и одного атома кислорода. Следовательно, формула исследуемого газа имеет вид N2O.
Ответ: N2O.
Задача 76
При одинаковых условиях взяты равные объемы N2 и O2. Каково соотношение масс обоих газов:
Решение:
Согласно закону Авогадро, в равных объёмах любых газов, взятых при одинаковых условиях (одной и той же температуре и одинаковом давлении) содержится одинаковое число молекул (6,02 . 10 23 ). Поскольку M(O2) равен 32 г/моль, а M(N2) – 28г/моль, то m(O2) > m(N2)
Ответ: а).
Задача 77.
Смешали равные объемы Н2 и С12. Как изменится объем смеси после протекания реакции: а) не изменится;
б) увеличится в два раза; в) уменьшится в два раза?
Решение:
Уравнение реакции взаимодействия хлора с водородом имеет вид:
При взаимодействии одного моля хлора с одним моль водорода образуется два объёма хлороводорода, т.е. реакция идёт без изменения объёма. Поэтому объём смеси после протекания реакции не изменится.
Ответ: а).
Задача 78.
Каково соотношение объемов, занимаемых 1 моль НСI и 1 моль Сl2 (Т и Р одинаковы):
Решение:
Согласно закону Авогадро одно и тоже число молекул любого газа занимает при одинаковых условиях (температура и давление одинаковы) один и тот же объём. Вместе с тем 1 моль любого газа содержит одинаковое число молекул. Следовательно, при одинаковых условиях 1 моль любого газа занимает один и тот же объём. Этот объём называется мольным объёмом газа и при нормальных условиях (Т = 0 °С и Р = 101,325 кПа) равен 22,4л. Поэтому соотношение объёмов одного моля HCl и одного моля Cl2 (T и Р одинаковы):
Ответ: б).
Задача 79.
При нагревании НВг полностью разлагается. При этом объём газа не изменяется. Каковы продукты реакции разложения: а) атомы Н и Вг; б) молекулы Н2 и Вг2 в) молекулы Н2 и атомы Br?
Решение:
Уравнение реакции термического разложения бромоводорода имеет вид:
Таким образом, из двух молекул НВг образуются одна молекула Н2 и одна молекула Вг2, т.е. объём системы после реакции не изменяется. Следовательно, продуктами реакции термического разложения HBr являются газообразные Н2 и Вг2.
Источник
Задачи на тему «Агрегатные состояния вещества»
1. Какой воздух легче: сухой или влажный?
Согласно закону Авогадро, в равных объемах любых газов при постоянных температуре и давлении содержится одинаковое число молекул. Состав воздуха: азот – 78%, кислород – 21%, углекислый газ – 1%, пары воды – 1%, прочие газы – 1%.
Таким образом, чтобы из сухого воздуха сделать влажный, надо часть молекул азота N2 или кислорода О2 заменить молекулами воды Н2О.
Обратимся к Периодической системе и рассчитаем молярные массы элементов:
μ (Н2О) = 1 ⋅ 2 + 16 = 18 г/моль
μ (О2) = 16 ⋅ 2 = 32 г/моль
μ (N2) = 14 ⋅ 2 = 28 г/моль
Видим, что влажный воздух содержит вместо более тяжелых молекул кислорода или азота более легкие молекулы воды, стало быть влажный воздух легче.
2. Напишите формулы четырех газов с резким запахом и двух газов, имеющих цвет.
Газы с резким запахом: аммиак NH3, оксид азота (IV) NO2 – бурый газ, сероводород Н2S, оксид серы (IV) SO2.
Газы, имеющие цвет: хлор Cl2 (желто-зеленый цвет), оксид хлора (I) Cl2O (желтовато-коричневый цвет).
3. Какое простое газообразное вещество легче первого члена гомологического ряда предельных аминов, но тяжелее первого члена гомологического ряда ацетиленовых углеводородов?
Гомологический ряд предельных аминов: СН3NH2 – метиламин (первичный амин), (СН3)2NH – диметиламин (вторичный амин), (СН3)3N – триметиламин (третичный амин) и т. д.
Гомологический ряд ацетиленовых углеводородов: С2Н2 – этин, С3Н4 – пропин, С4Н6 – бутин и т. д.
μ (СН3NH2) = 12 + 1 ⋅ 3 + 14 + 1 ⋅ 2 = 31 г/моль
μ (С2Н2) = 12 ⋅ 2 + 1 ⋅ 2 = 26 г/моль
Ответ: это азот, μ (N2) = 14 ⋅ 2 = 28 г/моль.
4. Имеется два сосуда, заполненных смесями газов: а) Н2 и Cl2; б) Н2 и О2. Как изменится давление в сосудах при пропускании через эти смеси электрической искры?
Давление не изменится, т. к. число молекул останется прежним.
Было 3 молекулы, стало 2. Значит давление уменьшится, т. к. на тот же объем приходится меньшее количество молекул.
5. В сосуде объемом 40 л находится 77 г углекислого газа под давлением 106,6 кПа. Найдите температуру газа.
Молярная масса углекислого газа:
μ (СО2) = 12 + 16 ⋅ 2 = 44 г/моль
ν = m / μ = 77 / 44 = 1.75 моль
Отсюда температура газа:
T = pV / (νR) = 106.6 кПа ⋅ 40 л / (1.75 моль ⋅ 8.314 Дж ⋅ К -1 ⋅ моль -1 ) = 293 К = 20 о С
6. Какой объем займут 20 г азота при 0 о С и давлении 202 кПа?
T = t + 273 = 0 + 273 = 273 K
Молярная масса азота газа:
μ (N2) = 14 ⋅ 2 = 28 г/моль
ν = m / μ = 20 / 28 = 0.714 моль
Отсюда объем газа:
V = νRT / p = (0.714 моль ⋅ 8.314 Дж ⋅ К -1 ⋅ моль -1 ⋅ 273 К) / 202 кПа = 8 л
7. Плотность некоторого газа по ацетилену 2.23. Чему равна плотность этого газа по водороду?
Химическая формула ацетилена – С2Н2, водорода – Н2.
μ (С2Н2) = 12 ⋅ 2 + 1 ⋅ 2 = 26 г/моль
μ (Н2) = 1 ⋅ 2 = 2 г/моль
8. Смешали равные объемы метана, оксида углерода (II) и оксида углерода (IV). Полученную смесь газов объемом 3 л пропустили через водный раствор щелочи в склянке (промывалке). Чему равен объем газа, измеренный при тех же условиях, на выходе из склянки?
Из трех газов, лишь оксид углерода (IV) (углекислый газ) будет взаимодействовать с водным раствором щелочи:
СО2 + КОН = КНСО3
Так как газы были взяты в равных объемах, то на выходе из склянки будут выделяться 1 л метана и 1 л угарного газа, т.е. объем 2 л.
9. Какой объем занимают при нормальных условиях: а) 5 г кислорода; б) 0.3 моль оксида серы (IV); в) смесь, состоящая из 0.3 моль N2 и 11 г СО2?
При нормальных условиях р = 101.3 кПа, Т = 273.15 К.
а) Молярная масса кислорода:
μ (О2) = 16 ⋅ 2 = 32 г/моль
ν = m / μ = 5 / 32 = 0.156 моль
Отсюда объем газа:
V = νRT / p = (0.156 моль ⋅ 8.314 Дж ⋅ К -1 ⋅ моль -1 ⋅ 273.15 К) / 101.3 кПа = 3.5 л
б) Уравнение Клапейрона-Менделеева:
Отсюда объем газа:
V = νRT / p = (0.3 моль ⋅ 8.314 Дж ⋅ К -1 ⋅ моль -1 ⋅ 273.15 К) / 101.3 кПа = 6.7 л
в) Молярные массы:
μ (N2) = 14 ⋅ 2 = 28 г/моль
μ (СО2) = 12 + 16 ⋅ 2 = 44 г/моль
Количество моль углекислого газа:
Общее количество моль:
ν = ν (СО2) + ν (N2) = 0.25 + 0.3 = 0.55 моль
Отсюда объем газа:
V = νRT / p = (0.55 моль ⋅ 8.314 Дж ⋅ К -1 ⋅ моль -1 ⋅ 273.15 К) / 101.3 кПа = 12.3 л
10. При дегидрировании 30 л пентана выделилось 90 л водорода. Установите молекулярную формулу образовавшегося продукта. Объемы газов измерены при 150 о С и 101 кПа.
T = t + 273 = 150 + 273 = 423 K
Отсюда количество моль:
ν (C5H12) = pV / (RT) = 101.3 кПа ⋅ 30 л / (8.314 Дж ⋅ К -1 ⋅ моль -1 ⋅ 423 К) = 0.86 моль
ν (H2) = pV / (RT) = 101.3 кПа ⋅ 90 л / (8.314 Дж ⋅ К -1 ⋅ моль -1 ⋅ 423 К) = 2.59 моль
Поскольку пентан выделил водород, то количество моль (частиц) C5H12 равно C5H12-2х, т. е. ν (C5H12-2х) = 0.86 моль.
С другой стороны, m (C5H12-2х) = 61.92 г – 5.18 г = 56.74 г
0.86 ⋅ (72 – 2x) = 56.74
Искомая молекулярная формула C5H6!
11. При каком молярном соотношении оксидов углерода получается смесь, которая в 2 раза тяжелее неона?
μ (СО2) = 12 + 16 ⋅ 2 = 44 г/моль
μ (СО) = 12 + 16 = 28 г/моль
Для смеси газов:
[44 ν (СО2) + 28ν (СО)] / [ν (СО2) + ν (СО)] = 40
44 ν (СО2) + 28 ν (СО) = 40 ν (СО2) + 40 ν (СО)
Ответ: ν (СО2) : ν (СО) = 3 : 1.
12. Вычислите среднюю молярную массу смеси, состоящей из 30% (по объему) сероводорода и 70% азота.
Для смеси газов:
Согласно закону Авогадро, в равных объемах любых газов при постоянных температуре и давлении содержится одинаковое число молекул.
μ (H2S) = 1 ⋅ 2 + 32 = 34 г/моль
μ (N2) = 14 ⋅ 2 = 28 г/моль
μ = [0.3 ⋅ 34 + 0.7 ⋅ 28] / [0.3 + 0.7] = 29.8 г/моль
13. Найдите плотность по водороду генераторного газа, имеющего следующий объемный состав: 25% СО, 70% N2, 5% CO2.
μ (СО2) = 12 + 16 ⋅ 2 = 44 г/моль
μ (СО) = 12 + 16 = 28 г/моль
μ (N2) = 14 ⋅ 2 = 28 г/моль
μ (H2) = 1 ⋅ 2 = 2 г/моль
Для смеси газов:
Согласно закону Авогадро, в равных объемах любых газов при постоянных температуре и давлении содержится одинаковое число молекул.
μ = [0.05 ⋅ 44 + 0.25 ⋅ 28 + 0.7 ⋅ 28] / [0.05 + 0.25 + 0.7] = 28.8 г/моль
Плотность по водороду:
14. При добавлении какого газа к смеси равных объемов ацетилена и бутина-2 плотность новой смеси по воздуху не изменится? Ответ подтвердите расчетами.
μ (С2Н2) = 12 ⋅ 2 + 1 ⋅ 2 = 26 г/моль
μ (С4Н6) = 12 ⋅ 4 + 1 ⋅ 6 = 54 г/моль
Средняя молярная масса:
μ = [0.5 ⋅ 26 + 0.5 ⋅ 54] / [0.5 + 0.5] = 40 г/моль
При добавлении еще одного газа с молярной массой «у» получим:
μ = [x ⋅ 26 + x ⋅ 54 + (1-2x)y] / [x + x + (1 — 2x)]
Поскольку плотность по воздуху та же, то и средние молярные массы равны:
x ⋅ 26 + x ⋅ 54 + (1-2x)y = 40
y = [40 – 80x] / (1 – 2x) = 40 г/моль
Такую молярную массу имеет аргон (Ar) или пропин (С3Н4).
15. Вычислите объем фтороводорода, который надо добавить к 3.36 л криптона, чтобы средняя молярная масса полученной газовой смеси составила 60 г/моль.
μ (НF) = 1 + 19 = 20 г/моль
μ (Kr) = 83.8 г/моль
Средняя молярная масса:
μ = mобщ / νобщ = [V (НF) ⋅ μ (НF) + V (Kr) ⋅ μ (Kr)] / [V (НF) + V (Kr)]
[х ⋅ 20 + 3.36 ⋅ 83.8] / [х + 3.36] = 60
20х + 281.57 = 60х + 201.6
16. Чему равна относительная плотность по неону: а) аргона; б) газа, плотность которого при нормальных условиях равна 1.429 г/л, в) смеси NH3 и СН4, в которой на 1 атом углерода приходится 6 атомов водорода?
а) Молярные массы аргона и неона:
Плотность по неону:
DNe = μ (Ar) / μ (Ne) = 40 / 20 = 2
б) Молярный объем газов при нормальных условиях
Значит молярная масса неизвестного газа
μ (?) = 22.4 л/моль ⋅ 1.429 г/л = 32 г/моль
Плотность по неону:
DNe = μ (?) / μ (Ne) = 32 / 20 = 1.6
в) Молярные массы:
μ (NН3) = 14 + 1 ⋅ 3 = 17 г/моль
μ (СН4) = 12 + 1 ⋅ 4 = 16 г/моль
Из условия знаем, что на каждый атом углерода приходится 6 атомов водорода, из которых 4 атома принадлежат молекуле СН4. Таким образом, соотношение количеств моль:
ν (С) : ν (Н4) : ν (Н3) : ν (N) = 1 : 4 : 2 : (2/3) = 3 : 12 : 6 : 2
Получаем отношение чисел молекул, а значит и объемов:
V (NН3) : V (СН4) = 2 : 3 = 40 : 60 (в процентах)
Средняя молярная масса:
μ = [0.4 ⋅ 17 + 0.6 ⋅ 16] / [0.4 + 0.6] = 16.4 г/моль
Плотность по неону:
DNe = μ / μ (Ne) = 16.4 / 20 = 0.82
Источник