Хлорид меди (II)
| Хлорид меди (II) | |
|---|---|
 | |
| Систематическое наименование | Хлорид меди (II) |
| Традиционные названия | Дихлорид меди, хлористая медь, двухлористая медь |
| Хим. формула | CuCl2 |
| Рац. формула | CuCl2 |
| Состояние | твёрдое |
| Молярная масса | 134,452 г/моль |
| Плотность | 3,386 г/см³ |
| Температура | |
| • плавления | 498 °C |
| • кипения | 993 °C |
| • разложения | 993 °C |
| Мол. теплоёмк. | 71,9 Дж/(моль·К) |
| Энтальпия | |
| • образования | 215 кДж/моль |
| Растворимость | |
| • в воде | 75,7 (25 °C) |
| ГОСТ | ГОСТ 4167-74 |
| Рег. номер CAS | 7447-39-4 |
| PubChem | 24014 |
| Рег. номер EINECS | 231-210-2 |
| SMILES | |
| RTECS | GL7000000 |
| ChEBI | 49553 |
| Номер ООН | 2802 |
| ChemSpider | 22447 и 148374 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хлорид меди (II) (медь хлорная) — бинарное неорганическое вещество, соединение меди с хлором, относящееся к классу галогенидов и солей (может рассматриваться как соль соляной кислоты и меди). Образует кристаллогидраты вида CuCl2·nH2O.
Содержание
Описание
Хлорид меди (II) при стандартных условиях представляет собой жёлто-бурые (по некоторым данным — тёмно-коричневые) кристаллы моноклинной сингонии, пространственная группа I 2/m, параметры ячейки a = 0,670 нм , b = 0,330 нм , c = 0,667 нм , β = 118,38° , Z = 2 .
При кристаллизации из водных растворов образует кристаллогидраты, состав которых зависит от температуры кристаллизации. При температуре ниже 117 °C образуется CuCl2·H2O, при Т a = 0,738 нм , b = 0,804 нм , c = 0,372 нм , Z = 2 .
Хорошо растворим в воде (77 г/100 мл), этаноле (53 г/100 мл), метаноле (68 г/100 мл), ацетоне. Легко восстанавливается до Cu 1+ и Сu 0 . Токсичен.
Получение
В природе дигидрат хлорида меди (II) CuCl2·2H2O встречается в виде редкого минерала эрнохальцита (кристаллы синего цвета).
В промышленности дихлорид меди получают:
- Хлорированием сульфида меди:
CuS + Cl2 → 300−400oC CuCl2 + S
- или используют хлорирующий обжиг:
CuS + 2NaCl + 2O2 → 350−360oC CuCl2 + Na2SO4
В лабораторной практике используют следующие методы:
- Взаимодействие металлической меди с хлором:
Cu + Cl2 ⟶ CuCl2
- Взаимодействие оксида меди (II) с соляной кислотой:
CuO + 2HCl ⟶ CuCl2 + H2O
- Взаимодействие гидроксида меди (II) с соляной кислотой (реакция нейтрализации):
Cu(OH)2 + 2HCl ⟶ CuCl2 + 2H2O
- Взаимодействие карбоната меди с соляной кислотой:
CuCO3 + 2HCl ⟶ CuCl2 + CO2↑ + H2O
- Растворение меди в царской водке:
3Cu + 2HNO3 + 6HCl → 30−50oC 3 CuCl2 + 2NO↑ + 4H2O
Химические свойства
- Взаимодействие с щелочами с образованием нерастворимого основания и растворимой соли:
CuCl2 + 2NaOH ⟶ Cu(OH)2↓ + 2NaCl
- Взаимодействие с металлами, стоящими в электрохимическом ряду напряжений металлов левее меди, например с цинком:
CuCl2 + Zn ⟶ ZnCl2 + Cu
- Реакции ионного обмена с другими солями (если образуется нерастворимое вещество или газ):
CuCl2 + 2AgNO3 ⟶ Cu(NO3)2 + 2AgCl↓
Применение
Применяют для омеднения металлов, как катализатор крекинга, декарбоксилирования, протраву при крашении тканей.
Источник
Получение меди
Медь или купрум, названа так в честь острова Кипр, где нашли крупное ее месторождение. Это один из первых металлов, освоенных человеком. Медный век – удивительная эпоха, в которую обиход человека был наполнен медными орудиями и предметами быта, он продолжался с IV до III тысячелетия до н. э.
Способы получения меди
Для извлечения меди из минералов и руд, в которых она находится, на сегодняшний день используют три метода:
- гидрометаллургический
- пирометаллургичекий
- электролиз.
Получение меди пирометаллургическим методом является наиболее распространенным. Сырьем для этого процесса выступает халькопирит. Чтобы получить из халькопирита чистую медь, необходимо осуществить ряд операций. Первая, из которых, заключается в обогащении медной руды, методом окислительного обжига или флотации.
В основе флотации лежит тот факт, что пустая порода и ее медесодержащие части, смачиваются по-разному. Если поместить всю массу породы в емкость с жидким составом, в котором имеются воздушные пузырьки, то часть с минеральными элементами, перемещается при помощи этих пузырьков на поверхность, и прилипает к ним. В результате на поверхности ванны наблюдается наличие концентрата или черновой меди. В этом составе присутствует от 10 до 35% чистой меди. Этот порошкообразный концентрат является сырьем для дальнейшего получения чистой меди.
Совсем по-другому протекают реакции получения меди методом окислительного обжига. Этим методом обогащают медные руды, в составе которых имеется существенное количество серы. Для реализации этой технологии необходимо нагреть руду до температуры 700–8000 градусов. Под действием таких высоких температур происходит окисление сульфидов, и объем серы в медной руде снижается почти в два раза. Следующим этапом является расплавление обогащенной руды в отражательных или шахтных печах при температуре 14500. Результатом этого расплава является образование штейна – сплава, который состоит из сульфидов меди и железа.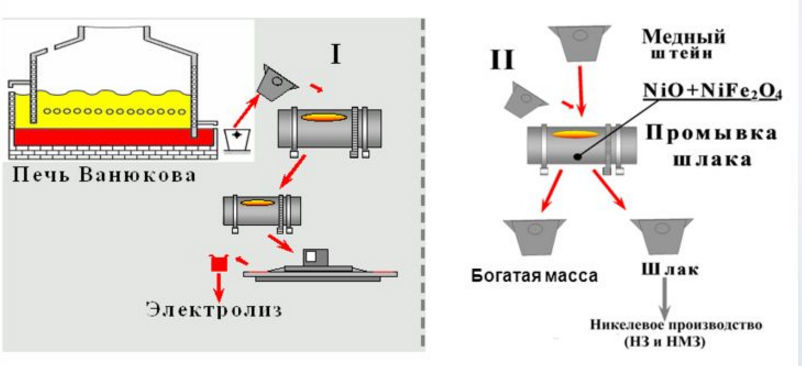
Черновая медь, полученная таким способом, имеет в своем составе около 91% меди. Для дополнительной очистки металла выполняется рафинирование меди, то есть удаление посторонних примесей. Это осуществляется благодаря технологии огневого рафинирования в присутствии подкисленного раствора медного купороса. Это рафинирование меди носит электролитический характер, и дает возможность получить металл с чистотой 99,9%.
Гидрометаллургический метод обогащения меди основан на процессе выщелачивания металла с помощью серной кислоты. Результатом такого процесса является получение раствора, из которого в дальнейшем выделяют чистую медь. Также этот метод подходит для выделения драгоценных металлов. Эту технологию применяют для обогащения руд, в которых присутствует крайне малое количество меди.
Получение меди электролизом
Электролиз меди является одним этапов химико-физических процессов, которому подвергают руду, чтобы получить медь. Примечательно, что для получения 1 тонны чистой меди, потребуется переработать как минимум 200 тонн медной руды.
Сама процедура обработки медной руды – это многоступенчатый и очень сложный процесс, который состоит из 7 стадий. Самой последней и является электролиз меди.
Руду после добычи необходимо измельчить в особых машинах. Далее происходит процесс флотации, в результате которого, как мы знаем, формируется концентрат с сохранением минералов меди. После этого происходит обжиг при высоких температурах в специальных печах. Шихту, полученную в процессе обжига, помещают в печь для плавки, где она становится штейном, который в свою очередь оправляют на конвертирование. Продукт, полученный после этих процессов, называют черновой медью, где 2-3% объема занимают примеси. В качестве примесей выступают цинк, железо, или сера. Их удаляют реакцией окисления. На этом этапе образуется «красная» медь, в которой присутствует 99,7-99,9% Cu. Последним этапом является непосредственно электролиз меди, который позволяет добиться получения максимально чистой меди.
Чтобы осуществить процесс электролиза меди понадобится специальное оборудование, а именно емкости, которые заполняют водным раствором сульфата меди с содержанием свободной серной кислоты. В результате проведения электролиза, мы получим осадок чистой меди на катодах. А все, что окажется на дне ванны, принято называть шламом. Он является сырьем для получения благородных металлов.
Получение оксида меди
Оксид меди (II) CuO представляет собой кристаллы черного цвета, которые подвергаются кристаллизации в моноклинной сингонии. Плотность соединения составляет 6,51 г/см3, а плавится он при температуре 1447°С в условиях высокого давления. В результате нагревания до 1100°С является выделение оксида меди (I):
В воде оксид меди не растворяется и не вступает в реакции с ней. Обладает слабыми амфотерными свойствами с преобладанием основных.
С водными растворами аммиака реагирует с образованием гидроксида тетраамминмеди (II):
Также легко вступает в реакции с разбавленными кислотами с выделением соли и воды:
Результатом сплавления оксида меди со щелочами является образование купратов:
Чистую медь из оксида можно получить методом восстановления водородом, угарным газом и активными металлами:
Реакция получения оксида меди методом прокаливания гидроксида меди (II) при температуре 200°С:
Также получить оксид меди можно в процессе окисления металлической меди на воздухе при температуре 400–500°С:
Получение сульфата меди
Получить сульфат меди можно тремя реакциями:
растворить CuO в H2SO4
в присутствии концентрированной серной кислоты с медью, обязательно при нагревании
методом взаимодействия Cu2O с разбавленной серной кислотой
Получение хлорида меди
В природе хлорид меди находится в составе очень редкого минерала эрнохальцита CuCl₂•2H₂O, который представляет собой кристаллы синего цвета.
Двухвалентный хлорид меди обладает важным практическим значением, и добычи его только лишь из природного минерала очень мало. Поэтому ученые придумали несколько способов искусственного получения данного соединения.
Главной реакцией промышленного синтеза CuCl₂ можно назвать реакцию хлорирования сульфида меди в условиях высокой температуры от 300 до 400 градусов °С. Выглядит реакция так
Еще одним вариантом синтеза хлорида двухвалентной меди является хлорирующий обжиг, который осуществляется при температуре более 500 С:
- CuS + 2NaCl + 2O₂ ―› CuCl₂ + Na₂SO₄
Обе реакции нуждаются в использовании специализированного оборудования и соблюдении повышенных мер безопасности, по этой причине данные реакции можно проводить только в условиях промышленного производства. В лабораторных условиях также можно получить хлорид меди следующими реакциями
- Cu + Cl₂ ―› CuCl₂
- CuO + 2HCl ―› CuCl₂ +H₂O
- Cu(OH)₂ + 2HCl ―› CuCl₂ + 2H₂O. Реакция нейтрализации
- CuCO₃ + 2HCL ―› CuCl₂ + H₂O + CO₂. В результате этой реакции более сильная кислота вытеснит кислотный остаток более слабой кислоты. Протекает реакция замещения
- 3Сu + 2HNO₃ + 6HCl ―› 3CuCl₂ + 2NO +4H₂0. Эта реакция является наиболее оригинальной. Она протекает только в присутствии смеси двух сильных кислот.
Получение глицерата меди
Качественная реакция для выявления присутствия глицерина в растворах осуществляется в присутствии сульфата меди (II) и раствора гидроксида натрия. В результате реакции образуется глицерат меди – комплексное соединение сине-василькового оттенка.
Химическую реакцию проводят следующим образом:
- к раствору сульфата меди (II) приливают раствор гидроксида натрия, в результате чего происходит окрашивание раствора в синий цвет. Таким образом, наблюдаем выпадения осадка гидроксида меди (II)
- после этого добавляем несколько мл глицерина и перемешиваем раствор. Образовавшийся осадок растворяется с образованием комплексного соединения оттенка индиго. Это и есть глицерат меди.
Получение нитрата меди
Получение нитрата меди Cu(NO3)2 довольно увлекательное занятие. А также очень полезное, поскольку он является довольно популярным красителем. Нитрат меди (II) можно получить в процессе растворения чистой меди, ее оксида или гидроксида в азотной кислоте. Уравнения выглядят следующим образом:
Получение сульфида меди
Сульфид меди(II) или моносульфид меди — CuS, является неорганическим бинарным соединением двухвалентной меди с серой. Он верного цвета, в воде не растворяется , также как и в разбавленных растворах кисло. В природе его можно встретить в виде редкого минерала ковеллина.
Получение сульфида меди осуществляется при помощи прямого взаимодействия элементов, а также в результате обменной реакции солей двухвалентной меди с водорастворимыми сульфидами.
- Na2S+CuSO4=CuS+Na2SO4
- CuCl2 + H2S —> CuS + 2HCl
- 2CuS + H2 —>Cu2S + H2S. Эта реакция протекает в условиях высокой температуры от 600 до 700 oC
Получение сухим методом дает сульфиду меди возможность проводить электрический ток. Когда отметка термометра достигает 400 °C, наблюдается заметное разложение сульфида.
Источник





