- ГК «Униконс»
- «Антисептики Септоцил»
- «Петритест»
- «АльтерСтарт»
- Стерилизация
- Стерилизация (микробиология) Индекс материала Стерилизация (микробиология) Компоненты Все страницы Стерилиза́ция — полное освобождение какого-либо предмета от всех видов микроорганизмов, включая бактерии и их споры, грибы, вирионы, а также от прионного белка, находящихся на поверхностях, оборудовании, в пищевых продуктах и лекарствах. Осуществляется термическим, химическим, радиационным, фильтрационным методами. Применение Пищевые продукты С давних времен частичная стерилизация пищи обеспечивалась за счет тщательной тепловой обработки во время приготовления. Нагревание пищи и воды позволяло снизить число случаев инфекционных заболеваний, увеличивая продолжительность жизни и трудоспособного возраста. Консервирование продуктов в герметичной упаковке стало логическим продолжением этого подхода к сохранению пищи. Медицина В медицине под стерилизацией понимается микробная деконтаминация неживых объектов. Принцип асептики предполагает исключение контакта пациента с поверхностями контаминированными условно-патогенной или даже патогенной микрофлорой. С этой целью стерилизовались скальпели, иглы и другой хирургический инструмент. Также стерилизация играет важную роль в производстве парентеральных препаратов. Нагревание медицинских инструментов было известно ещё в Древнем Риме, но было забыто в Средние века, что привело к резкому росту числа осложнений и летальности после хирургических операций. Методы стерилизации Термическая: паровая и воздушная (сухожаровая). Химическая: газовая или химическими растворами (стерилянтами) Радиационная стерилизация — применяется в промышленном варианте Метод мембранных фильтров — применяется для получения небольшого количества стерильных растворов, качество которых может резко ухудшиться при действии других методов стерилизации(бактериофаг, селективные питательные среды, антибиотики) Термические методы стерилизации Преимущества термических методов стерилизации: Надёжность Отсутствие необходимости удаления стерилянтов с предметов медицинского назначения Удобство работы персонала Стерилизация проводится в упаковках, что позволяет сохранить стерильность некоторый период времени. Паровая стерилизация Осуществляется подачей насыщенного водяного пара под давлением в паровых стерилизаторах (автоклавах). Паровая стерилизация под давлением считается наиболее эффективным методом, так как чем выше давление, тем выше температура пара, стерилизующего материал; бактерицидные свойства пара выше, чем воздуха, поэтому для стерилизации применяют пересыщенный пар. Паровой стерилизации подвергают изделия из текстиля (бельё, вату, бинты, шовный материал), из резины, стекла, некоторых полимерных материалов, питательные среды, лекарственные препараты. Режимы паровой стерилизации 132 °C — 2 атмосферы(2 кгс/см 2 ) — 20 минут — основной режим. Стерилизуют все изделия (стекло, металл, текстиль, кроме резиновых). 120 °C — 1,1 атмосфера(1,1 кгс/см 2 ) — 45 минут — щадящий режим (стекло, металл, резиновые изделия, полимерные изделия — согласно паспорту, текстиль) 110 °C — 0,5 атмосферы(0,5 кгс/см 2 ) — 180 мин — особо щадящий режим (нестойкие препараты, питательные среды) Упаковочные материалы при паровой стерилизации: Стерилизационная коробка (бикс) простая. Срок хранения 3 суток после стерилизации. Стерилизационная коробка (бикс) с фильтром. Срок хранения 20 суток после стерилизации. Крафт-пакеты со скрепками. Срок хранения — трое суток после стерилизации. Крафт-пакеты заклеивающиеся. Срок хранения — 20 суток после стерилизации. Ткань (бязь — КРОМЕ МАРЛИ). Срок хранения — трое суток после стерилизации. Комбинированные упаковки (прозрачная синтетическая плёнка + бумага) (дгм стеригард). Срок хранения от 180 суток до 720 суток. Тиндализация — способ стерилизации, предложенный Дж. Тиндалем. Заключается в дробной обработке жидкостей и пищевых продуктов в текучем паре при 100°С или при трёх — четырёхкратном нагревании их до 100—120°С с промежутками в 24 ч. За это время споры бактерий, выжившие при 100°С, прорастают, и вышедшие из них вегетативные клетки бактерий погибают при последующем нагревании. Стерилизация лекарственных препаратов, а также для так называемого горячего консервирования пищевых продуктов в специальных аппаратах с терморегуляторами. Химические методы стерилизации Используются при обработке приборов, аппаратов, сложных оптических систем, крупногабаритных изделий или изделий из титана, полимерных смол, резин. Для газовой (холодной) стерилизации используют герметичные контейнеры с парами окиси этилена, формальдегида или специализированными многокомпонентными системами. Для химической стерилизации растворами применяются основных четыре группы веществ: Кислота+окислитель (например «Первомур») Альдегид (например формалин) Детергент (например хлоргексидина биглюконат) Галоид (например Повидон-йод) Концентрации и время стерилизации зависит от используемого антисептика или дезинфектанта. Стерилизация ионизирующим излучением радиационный метод или лучевую стерилизацию γ-лучами применяют в специальных установках при промышленной стерилизации однократного применения — полимерных шприцев, систем переливания крови, чашек Петри, пипеток и других хрупких и термолабильных изделий. Ряд лет в фармтехнологии для стерилизации используется ультрафиолетовое (УФ) (длина волны 253,7 нм). Источники УФ-излучения — ртутные кварцевые лампы. Их мощное бактериостатическое действие основано на совпадении спектра испускания лампы и спектра поглощения ДНК микроорганизмов, что может является причиной их гибели при длительной обработке излучением кварцевых ламп. При недостаточно мощном действии УФ в прокариотической клетке активизируются процессы световой и темновой репарации и клетка может восстановиться. Метод применяется для стерилизации воздуха приточно-вытяжной вентиляции, оборудования в биксах, также для стерилизации дистиллированной воды. Источник Методы стерилизации, применяемые в микробиологической практике Стерилизация как совокупность физических, химических и механических способов освобождения от вегетативных и покоящихся форм микроорганизмов. Классификация фильтрующих перегородок, которые используются для стерильной фильтрации по механизму действия. Рубрика Биология и естествознание Вид реферат Язык русский Дата добавления 30.11.2014 Размер файла 16,0 K Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны. Размещено на http://www.allbest.ru Размещено на http://www.allbest.ru Под стерилизацией (sterilis — бесплодный) понимают совокупность физических, химических и механических способов освобождения от вегетативных и покоящихся форм микроорганизмов. Стерилизация должна обеспечивать уничтожение всей микрофлоры, патогенной и непатогенной, присутствующей в данном объекте. Она не должна приводить к порче материала или изменению его физического или химического состояния. Поэтому в зависимости от физических свойств стерилизуемых объектов и цели стерилизации применяют различные методы обеспложивания: горячие (влажная, дробная, сухая стерилизация) и холодные (механическая стерилизация, ионизация, стерилизация ультразвуком, ультрафиолетовыми лучами). Основное значение имеет тепловое воздействие на объект. 1. Механические методы стерилизации (стерилизующая фильтрация) Стерилизующая фильтрация. Микробные клетки и споры можно рассматривать как нерастворимые образования с очень малым (1-2 мкм) размером частиц. Подобно другим включениям, они могут быть отделены от жидкости механическим путем — фильтрованием сквозь мелкопористые фильтры. Этот метод стерилизации включен в ГФ ХI для стерилизации термолабильных растворов. По механизму действия фильтрующие перегородки, используемые для стерильной фильтрации, подразделяют на глубинные и поверхностные (мембранные) с размером пор не более 0,3 мкм. Глубинные фильтры характеризуются сложным механизмом задержания микроорганизмов (ситовым, адсорбционным, инерционным). Ввиду большой толщины таких фильтров удерживаются и частицы меньшего размера, чем размер пор фильтрующей перегородки. Глубинные фильтры бывают: керамические и фарфоровые (размер пор 3-4 мкм), стеклянные (около 2 мкм), бумажно-асбестовые (1-1,8 мкм). Недостатками керамических и фарфоровых фильтров является продолжительность стерилизации, потеря раствора в порах толстого фильтра, образование микротрещин из-за хрупкости материала и, следовательно, ненадежность стерилизации. Стеклянные фильтры малопроизводительны, бумажно-асбестовые фильтры не рекомендуются для стерилизации инъекционных растворов, поскольку они состоят из волокнистых материалов и имеется угроза отрыва волокон от фильтра. Попадая в организм с раствором, такие волокна могут вызывать различные патологические реакции. Получившие в последние годы большое распространение для стерилизующей фильтрации микропористые мембранные фильтры, лишены этих недостатков. Мембранные фильтры представляют собой тонкие (100-150 мкм) пластины из полимерных материалов, характеризующиеся ситовым механизмом задержания микроорганизмов и постоянным размером пор (около 0,3 мкм). Во избежание быстрого засорения фильтра мембраны используют в сочетании с префильтрами, имеющими более крупные поры. При стерилизации больших объемов растворов оптимальным является применение фильтров обоих типов. Использование глубинных и мембранных фильтров обеспечивает необходимую чистоту, стерильность и апирогенность растворов для инъекций. Стерилизующая фильтрация имеет преимущества по сравнению с методами термической стерилизации. Для многих растворов термолабильных веществ (апоморфина гидрохлорид, викасол, барбитал натрия и другие) он является единственно доступным методом стерилизации. Метод весьма перспективный в производстве глазных капель. 2. Химические методы стерилизации Эти методы основаны на высокой специфической (избирательной) чувствительности микроорганизмов к различным химическим веществам, что обусловливается физико-химической структурой их клеточной оболочки и протоплазмы. Механизм антимикробного действия многих таких веществ еще не достаточно изучен. Считают, что некоторые вещества вызывают коагуляцию протоплазмы клетки, другие — действуют как окислители, ряд веществ влияет на осмотические свойства клетки, многие химические факторы вызывают гибель микробиологической клетки благодаря разрушению ферментной системы. Основой любого варианта химической стерилизации является взаимодействие бактерицидного вещества с компонентами микробной клетки или споры. Химическая стерилизации подразделяется на стерилизацию растворами (веществами) и стерилизацию газами (газовая стерилизация). Стерилизация растворами или веществами. Стерилизацию растворами (веществами) серийно выпускаемой инъекционной продукции в заводских условиях не используют, так как введение в раствор постороннего биологического активного вещества нежелательно из-за возможного химического взаимодействия стерилизующего агента с действующими компонентами, а также из-за возможных побочных действий этого агента на организм человека. Еще одно принципиальное ограничение данного метода связано с тем, что практически любое бактерицидное вещество обладает определенной селективностью и его эффективность проявляется при высоких концентрациях или часто в определенных интервалах рН, недопустимых для живых организмов. Этот вид стерилизации используют для обеззараживания различной аппаратуры, трубопроводов и другого оборудования, применяемого в производстве стерильной продукции. Газовая стерилизация. Своеобразной химической стерилизацией является метод стерилизации газами. Преимуществом метода является возможность стерилизации объектов в пластмассовой упаковке, проницаемой для газов. В герметическую камеру вводят стерилизант — смесь этиленоксида и углерода диоксида в соотношении 9:1. Углекислый газ добавляют в связи со взрывоопасностью окиси этилена. При стерилизации стерилизант поступает в аппарат под давлением до 2 кгс/см2 (196133 Н/м2) при температуре 43-45°С. Продолжительность стерилизации зависит от проницаемости упаковки, толщины слоя материала и продолжается от 4 до 20 часов. Затем этиленоксид удаляют продуванием стерильным воздухом (азотом) или путем вакуумирования. При химической стерилизации газами погибают все вегетативные формы микроорганизмов и плесневые грибы. Для стерилизации донорского материала, растворов кровезаменителей или продуктов, полученных из крови, широко применяют в-пропиолактон. Главный недостаток химических методов стерилизации — необходимость освобождения простерилизованного объекта от остатков стерилизанта и продуктов возможного взаимодействия. Широкому распространению этого метода препятствуют длительность стерилизации, высокая стоимость, возможность побочного действия химического агента на обслуживающий персонал и, тем не менее, для ряда лекарственных препаратов — это единственно надежный способ стерилизации в современных условиях. Использование консервантов. Добавление консервантов условно можно отнести к методам химической стерилизации. Введение консервантов в растворы проводится в тех случаях, когда нельзя гарантировать сохранение стерильности. При этом возможно снижение температуры стерилизации или сокращение времени ее проведения. Механизмы воздействия консервантов на микроорганизмы очень различны и определяются их химическим строением. Основным результатом при этом является нарушение жизненных функций клетки, в частности, инактивация белковой части клеточных ферментов. В зависимости от степени инактивации наступает либо гибель клетки, либо замедление ее жизненных функций. 3. Физические методы стерилизации Тепловая (термическая) стерилизация. В настоящее время монопольное положение среди возможных методов стерилизации в фармацевтическом производстве занимает тепловая стерилизация. В зависимости от температурного режима тепловая стерилизация подразделяется на: · паром под давлением (автоклавирование); Стерилизация паром под давлением. Автоклавирование — это стерилизация растворов, устойчивых к нагреванию, паром под давлением 1,1 атм при температуре 119-121°С. В данных условиях погибают не только вегетативные, но и споровые микроорганизмы за счет коагуляции белка клетки. Этот традиционный способ стерилизации обладает сегодня преимуществом перед другими по трем причинам. Во-первых, он дает возможность стерилизации препаратов в конечной герметичной упаковке, что исключает опасность вторичной контаминации. Во-вторых, благодаря длительной практике использования он обеспечен достаточно надежной аппаратурой. И, в-третьих, на сегодняшний день он наиболее экономичен. При этом методе происходит комбинированное воздействие на микроорганизмы высокой температуры и влажности, при этом погибают самые стойкие споры. Коагуляция белковых веществ в этих условиях начинается при температуре 56°С. Стерилизацию паром под давлением проводят в стерилизаторах различной конструкции цилиндрической или квадратной формы. Стерилизаторы квадратной формы типа АП-7 (рис. 5.25.), АП-18 имеют двери с двух сторон: через одну происходит загрузка нестерильной продукции; через другую — выгрузка простерилизованной. Корпус автоклава нагревается глухим паром, чтобы не было его конденсации в рабочей камере. Затем в камеру для вытеснения воздуха подается острый пар. Отчет времени стерилизации начинается с момента достижения заданного давления по манометру. Стерилизаторы оснащены автоматической контрольной аппаратурой, с помощью которой на контрольной ленте записывается давление и время стерилизации. Условия стерилизации продукции указаны в промышленных регламентах или другой нормативно-технической документации. Стерилизацию растительных масел и жиров в заводских условиях осуществляют паром под давлением в герметически закрытых сосудах при температуре 119-121°С и давлении 1,0-1,1 атм. в течение 2 часов. Автоклавированию также подвергаются установки для стерилизующего фильтрования, фильтрующие перегородки и другой вспомогательный материал, используемый в технологическом процессе производства инъекционных лекарственных форм. Среди недостатков метода можно выделить невозможность стерилизации растворов, содержащих термолабильные вещества, опасность работы с паром под давлением, отсыревание многих материалов во время стерилизации и др. Стерилизация текучим паром. Растворы веществ, термически малоустойчивые, иногда стерилизуют при 100°С текучим паром (без примеси воздуха и избыточного давления). Насыщенный пар убивает только вегетативные формы микроорганизмов и при наличии в объекте споровых форм этот метод неэффективен. Тиндализация (дробная стерилизация). Для термолабильных веществ, а также для растворов в шприц-ампулах стерилизацию иногда проводят методом тиндализации. Суть метода заключается в трехкратном нагревании растворов до 40-60°С с перерывами в сутки, в течение которых объекты термостатируют при температуре 37±1°С для прорастания споровых форм в вегетативные. Стерилизация сухим жаром (воздушная стерилизация). Стерилизация сухим жаром, проводимая в аэростерилах или других аппаратах этого типа, также высокоэффективна. При этом погибают все формы микроорганизмов за счет пирогенетического разложения белковых веществ. Однако, высокая температура нагрева (160-200°С), длительное время воздействия (1-2 часа) и сухой горячий воздух оказывает повреждающее действие на стерилизуемые объекты и, следовательно, ограничивают возможности данного способа. Инъекционные растворы не подвергают стерилизации сухим жаром, так как из-за плохой теплопроводности воздух не обеспечивает быстрый нагрев растворов до температуры стерилизации, а длительный прогрев — приводит к разложению большинства лекарственных веществ. Сухим жаром стерилизуют некоторые термостойкие порошки, масла, стеклянную тару (ампулы, флаконы и необходимую посуду), вспомогательные материалы. Лучшими являются стерилизаторы с ламинарным потоком стерильного воздуха, нагретого до требуемой температуры, что улучшает создание равномерного температурного поля и устраняет загрязнения от обогреваемых стенок камеры и из воздуха, попадаемого в момент выгрузки объекта. Радиационная стерилизация. Лучистая энергия губительно действует на клетки живого организма, в том числе и на различные микроорганизмы. Принцип стерилизующего эффекта этих излучений основан на способности вызывать в живых клетках при определенных дозах поглощенной энергии такие изменения, которые неизбежно приводят их к гибели за счет нарушения метаболических процессов и коагуляции белка. Источником ионизирующих г-излучений служат долгоживущие изотопы 60Со27, 137Cs55, ускорители электронов прямого действия и линейные ускорители электронов. Для бактерицидного эффекта достаточно от 15 до 25 кГр, причем верхний предел необходим для инактивации споровых форм. В настоящее время накоплен большой опыт применения этого метода, точно установлены типичные дозы излучения, необходимые для надежной стерилизации, разработано радиационное оборудование для высокопроизводительного процесса стерилизации, решены вопросы безопасности работы установок для обслуживающего персонала. Этот метод по экономическим показателям превосходит асептическое изготовление растворов со стерильной фильтрацией, но несколько уступает тепловой стерилизации. Однако, в будущем может приблизиться к ней из-за неизбежного снижения относительной стоимости изотопов, которые являются побочным продуктом атомной энергетики. Ультразвуковая стерилизация. Прохождение ультразвука (УЗ) в жидкой среде сопровождается чередующимися сжатиями, разрежениями и большими переменными ускорениями. В жидкости образуются разрывы, называемые кавитационными полостями. В момент сжатия эти полости захлопываются. Избыточное давление, создаваемое УЗ-волной, накладывается на постоянное гидростатическое и суммарно может составлять в пузырьках несколько атмосфер. В качестве «зародышей» кавитационных полостей могут быть пузырьки газа, пара в жидкости, твердые частицы и места неровностей твердой поверхности. Большие импульсные давления кавитаций приводят к разрушению целостности клеточной мембраны микроорганизмов, споровых образований и других частиц. Важно установить оптимальные параметры процесса стерилизации, так как высокие импульсные давления могут приводить к механическому разрушению ампул. Стерилизующая частота звука должна быть в пределах 18-22 кГц. И, хотя метод очень эффективен, он не нашел широкого применения из-за сложности аппаратурного оснащения и возможных сложных химических превращений компонентов растворов. Вопросы стабильности компонентов при УЗ-стерилизации имеют много общего с аналогичными проблемами радиационной стерилизации. Для повышения устойчивости лекарств при ультразвуковом воздействии необходимо подобрать такие условия стерилизующей обработки, которые обеспечивают снижение вводимой в систему энергии на тех частотах ультразвука, которые одновременно со стерилизацией не приводят к разложению компонентов лекарственных препаратов. Чаще метод применим при производстве эмульсий и суспензий с целью лучшего диспергирования веществ в них и одновременно получения стерильных гетерогенных систем для парентерального применения. Стерилизация токами высокой и сверхвысокой частоты. К настоящему времени нет единой точки зрения на механизм инактивации микроорганизмов при ВЧ- и СВЧ-облучении. Существует мнение об исключительно тепловом механизме действия токов высокой частоты на биологические объекты. Принцип действия высокочастотного поля заключается в его активном воздействии на ориентацию молекул вещества. Изменение направленности поля вызывает изменение ориентации молекул и поглощение части энергии поля веществом. В результате происходит быстрый нагрев вещества во всех точках его массы. Менее широко распространены представления о том, что, помимо тепловых процессов, на гибель микроорганизмов оказывает влияние специфическое действие ВЧ- и СВЧ-излучения. С помощью СВЧ-энергии возможно стерилизовать в расфасованном виде готовую продукцию: глазные мази, пасты в тубах, лекарственные средства в конвалютах, порошки, таблетки, пористые лиофилизированные массы, не содержащие гидрофильные жидкости. Стерилизация ампулированных растворов и жидких лекарственных форм, укупоренных герметически нежелательна, так как в замкнутой емкости возникает избыток давления паров испарившейся жидкости, взрывающий ее. В результате наступает разгерметизация в виде растрескивания стенок ампул или срыва укупорочного материала. Метод также не нашел широкого применения из-за сложности аппаратурного оснащения и возможности неблагоприятного воздействия быстрого кратковременного нагрева инъекционного раствора. Стерилизация ультрафиолетовым излучением. Из-за возможности образования ядовитых продуктов и возможности разложения биологически активных компонентов инъекционных растворов под действием УФ-излучения, метод не нашел своего применения для стерилизации препаратов для инъекций. Однако он широко используется для стерилизации порошков, воды для инъекций, вспомогательных материалов, воздушной среды производственных помещений, технологического оборудования и других объектов. При стерилизации воздушной среды производственных помещений в качестве источников УФ-радиации используют специальные лампы БУВ (бактерицидная увиолевая), которые изготавливают в виде трубки из специального увиолевого стекла, способного пропускать УФ-лучи, с электродами из длинной вольфрамовой спирали, покрытой бария и стронция гидрокарбонатами. В трубке находится ртуть и аргон при давлении в несколько мм рт.ст. Источником УФ-лучей является разряд ртути, происходящий между электродами при подаче на них напряжения. Излучение лампы БУВ обладает большим бактерицидным действием, так как максимум излучения лампы близок к максимуму бактерицидного действия (254 нм). стерильный фильтрующий микроорганизм Количество и мощность бактерицидных ламп подбирается так, чтобы при прямом облучении на 1 м3 объема помещения приходилось не менее 2-2,5 Вт мощности излучателя. Промышленностью выпускаются лампы БУВ-15, БУВ-30, БУВ-60 и др. (цифра обозначает мощность в Ваттах), а также бактерицидные облучатели: настенный ОБН, состоящий из двух ламп БУВ-30; потолочный ОБП — из 4 ламп БУВ-30; передвижной маячного типа ОБПЕ — из 6 ламп БУВ-30. Облучатели используют только при отсутствии в помещении людей. Для стерилизации воды применяют аппараты с погруженными и непогруженными источниками УФ-радиации. В аппаратах первого типа источник УФ-излучения (бактерицидная увиолевая лампа, покрытая кожухом из кварцевого стекла) помещается внутри водопровода и обтекается водой. Данный способ стерилизации больших объемов воды для инъекций является наиболее экономичным. В аппаратах с непогруженными лампами последние помещаются над поверхностью облучаемой воды. В связи с тем, что обычное стекло практически непроницаемо для ультрафиолетовых лучей, водопровод в местах облучения делают из кварцевого стекла, а это значительно повышает стоимость аппарата. В настоящее время разработана возможность замены кварцевого стекла полиэтиленовым, свободно пропускающим УФ-радиацию. Как положительный фактор, следует отметить, что при стерилизации воды не происходит накопления пероксидных соединений и под действием УФ-излучения инактивируются некоторые пирогенные вещества, попавшие в воду. Стерилизация ИК и лазерным излучением. Электронная стерилизация. Эти перспективные виды стерилизации практически не находят сегодня применения, хотя возможности для этого имеются. Облучение инъекционных водных систем инфракрасным (ИК) излучением в областях поглощения воды (l = 2,7 мкм) может быть эффективным средством ее нагрева и тем самым является по сути еще одним вариантом тепловой стерилизации. Наличие достаточно мощных источников ИК-излучения позволяет надеяться на возможность создания оборудования для высокопроизводительной технологии. Преимуществом этого метода перед традиционным автоклавированием может считаться возможность отказа от небезопасного в обслуживании и нетехнологичного перегретого пара. Принципиально возможны способы стерилизации с применением лазерного и электронного излучения, при этом можно достичь высокой эффективности стерилизации как путем интенсивного нагрева вследствие поглощения мощного излучения в воде, так и за счет селективного поглощения излучения макромолекулами микроорганизмов в многоквантовых процессах. Однако исчерпывающих исследований применительно к какой-либо конкретной системе, совокупность которых дала бы основание о создании хотя бы основ таких методов стерилизации, пока не проведено. Размещено на Allbest.ru Подобные документы Методы изучения морфологии микроорганизмов. Правила работы в микробиологической лаборатории. Микроскопия в светлом поле. Установка света по Келеру. Изображения фиксированных препаратов, полученные в результате исследования метода изучения морфологии. лабораторная работа [925,0 K], добавлен 14.05.2009 Организация лабораторной микробиологической службы. Принципы микробиологической диагностики инфекционных заболеваний. Методы выделения и идентификации бактерий, вирусов, грибковых инфекций, простейших. реферат [3,8 M], добавлен 05.05.2006 Исследование возможности и процессов адаптации микроорганизмов в экстремальных условиях космоса при анализе характеристик их жизнеспособности и пластичности. Физиологические процессы микроорганизмов в космосе. Проблемы микробиологической безопасности. реферат [18,4 K], добавлен 10.12.2010 Споры – форма бактерий с грамположительным типом строения клеточной стенки. Роль спорообразования бактерий и грибов для практики. Строение и особенности химического состава бактериальной споры. Микробиологическое обоснование пастеризации и стерилизации. контрольная работа [223,5 K], добавлен 02.10.2011 Роль микроорганизмов в круговороте азота, водорода, кислорода, серы, углерода и фосфора в природе. Различные типы жизни бактерий, основанные на использовании соединений различных химических веществ. Роль микроорганизмов в эволюции жизни на Земле. реферат [20,2 K], добавлен 28.01.2010 Источник
- Применение
- Методы стерилизации
- Методы стерилизации, применяемые в микробиологической практике
- Стерилизация как совокупность физических, химических и механических способов освобождения от вегетативных и покоящихся форм микроорганизмов. Классификация фильтрующих перегородок, которые используются для стерильной фильтрации по механизму действия.
- Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
- Подобные документы
ГК «Униконс»
Продвижение и реализация комплексных пищевых добавок, антисептиков и др. продукции.
«Антисептики Септоцил»
Септоцил. Бытовая химия, антисептики.
«Петритест»
Микробиологические экспресс-тесты. Первые результаты уже через 4 часа.
«АльтерСтарт»
Закваски, стартовые культуры. Изготовление любых заквасок для любых целей.
- Вы здесь:
- Библиотека технолога
- Микробиология
- В.Н. Азаров. Основы микробиологии и санитарии
Стерилизация
Стерилизация — это обеспложивание, т. е. полное освобождение объектов внешней среды от микроорганизмов.
Стерилизацию проводят различными способами: физическими (воздействие высокой температуры, ультрафиолетовых лучей, использование бактериальных фильтров); химическими (использование различных антисептиков для консервирования питательных сред); биологическими (применение антибиотиков).
Целесообразность использования того или иного способов стерилизации обусловлена особенностями материала, подлежащего стерилизации, его физическими и химическими свойствами.
В лабораторной практике обычно применяют физические способы стерилизации.
Прокаливание в пламени горелки или спиртовки (фламбирование) — способ стерилизации, при котором происходит полное обеспложивание объекта, гак как погибают не только вегетативные клетки, но и споры микроорганизмов. Обычно прокаливают бактериологические петли, шпатели, предметные и покровные стекла, мелкие инструменты.
Стерилизацию сухим жаром проводят в сушильных шкафах (стерилизаторах), представляющих собой термостат с электрическим обогревом, в котором автоматически на заданием уровне может поддерживаться высокая температура. Этим способом стерилизуют лабораторную посуду, предварительно тщательно вымытую, высушенную и плотно завернутую в бумагу.
Стерильность сухим паром при 160-165 °С обеспечивается не менее чем за 90 мин, при 180 °С — не менее чем за 30 мин.
Жидкости (питательные среды, физиологический раствор и др.), предметы из резины и синтетических материалов стерилизовать сухим жаром нельзя, так как жидкости выкипают и выливаются, а резина и синтетические материалы разрушаются. Питательные среды и другие жидкости стерилизуют нагревом в парах воды.
Стерилизация паром может проводиться паром под давлением и текучим паром. Чаще применяют первый способ.
Стерилизацию паром под давлением производят в автоклаве. Способ основан на воздействии на стерилизуемые материалы насыщенного водяного пара под давлением, выше атмосферного. В результате такой обработки погибают вегетативные и споровые формы микроорганизмов.
Автоклав представляет собой двухстенный массивный котел, снаружи обшитый металлическим кожухом, с герметически закрывающейся крышкой, которая плотно прижимается к котлу откидывающимися болтами с барашками. За счет кипения воды и герметизации в автоклаве создается повышенное давление, позволяющее поднять температуру выше 100 °С.
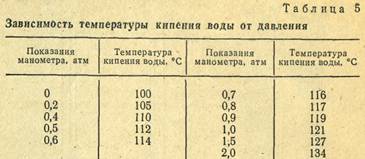
Каждому значению избыточного давления чистого водяного пара, которое фиксируется манометром, устанавливаемым на автоклаве, соответствует определенная температура кипения воды (табл. 5).
В автоклавах обрабатывают питательные среды, физиологический раствор, воду, лабораторные приборы и мелкое оборудование, имеющее резиновые детали, и др.
Температура и длительность автоклавирования питательных сред определяются их составом. Например, простые среды (мясопептонный агар, мясопептонный бульон) стерилизуют 20 мин при 120 °С. Однако при этой температуре нельзя стерилизовать среды, содержащие нативные белки, углеводы и другие легко изменяющиеся от нагревания вещества. Среды, имеющие углеводы, стерилизуют в автоклаве при температуре 112°С в течение 10-15 мин или дробно при 100 °С в кипятильнике Коха.
Различные жидкости, приборы, имеющие резиновые шланги, пробки, бактериологические фильтры и т. д. стерилизуют 20 мин при температуре 120 °С.
В автоклавах обезвреживают также инфицированный материал. Чашки и пробирки, содержащие культуры микробов, помещают в специальные металлические ведра или баки с отверстиями в крышке для проникновения пара и стерилизуют в автоклаве при температуре 120 °С в течение часа. Таким же образом стерилизуют инструменты после работы с бактериями, образующими споры.
К работе с автоклавом допускаются специально подготовленные люди, которые должны строго и точно выполнять правила, указанные в инструкции, прилагаемой к аппарату.
Различные питательные среды и другие материалы для заготовки впрок разливают в пробирки, колбы и закрывают ватными пробками. После обработки в автоклаве они хранятся длительное время, не подвергаясь порче, и используются по мере надобности.
В лабораторной практике для получения эффекта стерильности при температуре, не превышающей 100 °С, иногда пользуются кипятильником Коха. Это металлический цилиндрический сосуд, на дно которого наливается вода; над водой, на решете, помещают стерилизуемые предметы. При кипячении воды все предметы оказываются в атмосфере пара (при температуре 100 °С), вытекающего через неплотно закрывающуюся крышку, отчего и возникло выражение «стерилизация текучим паром».
Однократное прогревание текучим паром в течение часа не приводит к гибели споровых микробов. Достичь этого можно, прибегнув к двукратному повторному нагреванию, которое проводят с интервалом 24 ч по часу. Это так называемая дробная стерилизация.
Учитывая, что температура может существенно влиять на развитие психрофилов, мезофилов, термофилов, при выращивании каждой группы следует создавать необходимые температурные условия; их поддерживают в термостатах — лабораторных шкафах с двойными стенками, теплонагревательным элементом и терморегулятором.
Источник
Стерилизация (микробиология)
Стерилиза́ция — полное освобождение какого-либо предмета от всех видов микроорганизмов, включая бактерии и их споры, грибы, вирионы, а также от прионного белка, находящихся на поверхностях, оборудовании, в пищевых продуктах и лекарствах. Осуществляется термическим, химическим, радиационным, фильтрационным методами. ПрименениеПищевые продукты С давних времен частичная стерилизация пищи обеспечивалась за счет тщательной тепловой обработки во время приготовления. Нагревание пищи и воды позволяло снизить число случаев инфекционных заболеваний, увеличивая продолжительность жизни и трудоспособного возраста. Консервирование продуктов в герметичной упаковке стало логическим продолжением этого подхода к сохранению пищи. Медицина В медицине под стерилизацией понимается микробная деконтаминация неживых объектов. Принцип асептики предполагает исключение контакта пациента с поверхностями контаминированными условно-патогенной или даже патогенной микрофлорой. С этой целью стерилизовались скальпели, иглы и другой хирургический инструмент. Также стерилизация играет важную роль в производстве парентеральных препаратов. Нагревание медицинских инструментов было известно ещё в Древнем Риме, но было забыто в Средние века, что привело к резкому росту числа осложнений и летальности после хирургических операций. Методы стерилизации
Термические методы стерилизации Преимущества термических методов стерилизации:
Паровая стерилизация Осуществляется подачей насыщенного водяного пара под давлением в паровых стерилизаторах (автоклавах). Паровая стерилизация под давлением считается наиболее эффективным методом, так как чем выше давление, тем выше температура пара, стерилизующего материал; бактерицидные свойства пара выше, чем воздуха, поэтому для стерилизации применяют пересыщенный пар. Паровой стерилизации подвергают изделия из текстиля (бельё, вату, бинты, шовный материал), из резины, стекла, некоторых полимерных материалов, питательные среды, лекарственные препараты. Режимы паровой стерилизации 132 °C — 2 атмосферы(2 кгс/см 2 ) — 20 минут — основной режим. Стерилизуют все изделия (стекло, металл, текстиль, кроме резиновых). 120 °C — 1,1 атмосфера(1,1 кгс/см 2 ) — 45 минут — щадящий режим (стекло, металл, резиновые изделия, полимерные изделия — согласно паспорту, текстиль) 110 °C — 0,5 атмосферы(0,5 кгс/см 2 ) — 180 мин — особо щадящий режим (нестойкие препараты, питательные среды) Упаковочные материалы при паровой стерилизации:
Тиндализация — способ стерилизации, предложенный Дж. Тиндалем. Заключается в дробной обработке жидкостей и пищевых продуктов в текучем паре при 100°С или при трёх — четырёхкратном нагревании их до 100—120°С с промежутками в 24 ч. За это время споры бактерий, выжившие при 100°С, прорастают, и вышедшие из них вегетативные клетки бактерий погибают при последующем нагревании. Стерилизация лекарственных препаратов, а также для так называемого горячего консервирования пищевых продуктов в специальных аппаратах с терморегуляторами. Химические методы стерилизации Для газовой (холодной) стерилизации используют герметичные контейнеры с парами окиси этилена, формальдегида или специализированными многокомпонентными системами. Для химической стерилизации растворами применяются основных четыре группы веществ:
Концентрации и время стерилизации зависит от используемого антисептика или дезинфектанта. Стерилизация ионизирующим излучением
Источник Методы стерилизации, применяемые в микробиологической практикеСтерилизация как совокупность физических, химических и механических способов освобождения от вегетативных и покоящихся форм микроорганизмов. Классификация фильтрующих перегородок, которые используются для стерильной фильтрации по механизму действия.
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную нижеСтуденты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны. Размещено на http://www.allbest.ru Размещено на http://www.allbest.ru Под стерилизацией (sterilis — бесплодный) понимают совокупность физических, химических и механических способов освобождения от вегетативных и покоящихся форм микроорганизмов. Стерилизация должна обеспечивать уничтожение всей микрофлоры, патогенной и непатогенной, присутствующей в данном объекте. Она не должна приводить к порче материала или изменению его физического или химического состояния. Поэтому в зависимости от физических свойств стерилизуемых объектов и цели стерилизации применяют различные методы обеспложивания: горячие (влажная, дробная, сухая стерилизация) и холодные (механическая стерилизация, ионизация, стерилизация ультразвуком, ультрафиолетовыми лучами). Основное значение имеет тепловое воздействие на объект. 1. Механические методы стерилизации (стерилизующая фильтрация) Стерилизующая фильтрация. Микробные клетки и споры можно рассматривать как нерастворимые образования с очень малым (1-2 мкм) размером частиц. Подобно другим включениям, они могут быть отделены от жидкости механическим путем — фильтрованием сквозь мелкопористые фильтры. Этот метод стерилизации включен в ГФ ХI для стерилизации термолабильных растворов. По механизму действия фильтрующие перегородки, используемые для стерильной фильтрации, подразделяют на глубинные и поверхностные (мембранные) с размером пор не более 0,3 мкм. Глубинные фильтры характеризуются сложным механизмом задержания микроорганизмов (ситовым, адсорбционным, инерционным). Ввиду большой толщины таких фильтров удерживаются и частицы меньшего размера, чем размер пор фильтрующей перегородки. Глубинные фильтры бывают: керамические и фарфоровые (размер пор 3-4 мкм), стеклянные (около 2 мкм), бумажно-асбестовые (1-1,8 мкм). Недостатками керамических и фарфоровых фильтров является продолжительность стерилизации, потеря раствора в порах толстого фильтра, образование микротрещин из-за хрупкости материала и, следовательно, ненадежность стерилизации. Стеклянные фильтры малопроизводительны, бумажно-асбестовые фильтры не рекомендуются для стерилизации инъекционных растворов, поскольку они состоят из волокнистых материалов и имеется угроза отрыва волокон от фильтра. Попадая в организм с раствором, такие волокна могут вызывать различные патологические реакции. Получившие в последние годы большое распространение для стерилизующей фильтрации микропористые мембранные фильтры, лишены этих недостатков. Мембранные фильтры представляют собой тонкие (100-150 мкм) пластины из полимерных материалов, характеризующиеся ситовым механизмом задержания микроорганизмов и постоянным размером пор (около 0,3 мкм). Во избежание быстрого засорения фильтра мембраны используют в сочетании с префильтрами, имеющими более крупные поры. При стерилизации больших объемов растворов оптимальным является применение фильтров обоих типов. Использование глубинных и мембранных фильтров обеспечивает необходимую чистоту, стерильность и апирогенность растворов для инъекций. Стерилизующая фильтрация имеет преимущества по сравнению с методами термической стерилизации. Для многих растворов термолабильных веществ (апоморфина гидрохлорид, викасол, барбитал натрия и другие) он является единственно доступным методом стерилизации. Метод весьма перспективный в производстве глазных капель. 2. Химические методы стерилизации Эти методы основаны на высокой специфической (избирательной) чувствительности микроорганизмов к различным химическим веществам, что обусловливается физико-химической структурой их клеточной оболочки и протоплазмы. Механизм антимикробного действия многих таких веществ еще не достаточно изучен. Считают, что некоторые вещества вызывают коагуляцию протоплазмы клетки, другие — действуют как окислители, ряд веществ влияет на осмотические свойства клетки, многие химические факторы вызывают гибель микробиологической клетки благодаря разрушению ферментной системы. Основой любого варианта химической стерилизации является взаимодействие бактерицидного вещества с компонентами микробной клетки или споры. Химическая стерилизации подразделяется на стерилизацию растворами (веществами) и стерилизацию газами (газовая стерилизация). Стерилизация растворами или веществами. Стерилизацию растворами (веществами) серийно выпускаемой инъекционной продукции в заводских условиях не используют, так как введение в раствор постороннего биологического активного вещества нежелательно из-за возможного химического взаимодействия стерилизующего агента с действующими компонентами, а также из-за возможных побочных действий этого агента на организм человека. Еще одно принципиальное ограничение данного метода связано с тем, что практически любое бактерицидное вещество обладает определенной селективностью и его эффективность проявляется при высоких концентрациях или часто в определенных интервалах рН, недопустимых для живых организмов. Этот вид стерилизации используют для обеззараживания различной аппаратуры, трубопроводов и другого оборудования, применяемого в производстве стерильной продукции. Газовая стерилизация. Своеобразной химической стерилизацией является метод стерилизации газами. Преимуществом метода является возможность стерилизации объектов в пластмассовой упаковке, проницаемой для газов. В герметическую камеру вводят стерилизант — смесь этиленоксида и углерода диоксида в соотношении 9:1. Углекислый газ добавляют в связи со взрывоопасностью окиси этилена. При стерилизации стерилизант поступает в аппарат под давлением до 2 кгс/см2 (196133 Н/м2) при температуре 43-45°С. Продолжительность стерилизации зависит от проницаемости упаковки, толщины слоя материала и продолжается от 4 до 20 часов. Затем этиленоксид удаляют продуванием стерильным воздухом (азотом) или путем вакуумирования. При химической стерилизации газами погибают все вегетативные формы микроорганизмов и плесневые грибы. Для стерилизации донорского материала, растворов кровезаменителей или продуктов, полученных из крови, широко применяют в-пропиолактон. Главный недостаток химических методов стерилизации — необходимость освобождения простерилизованного объекта от остатков стерилизанта и продуктов возможного взаимодействия. Широкому распространению этого метода препятствуют длительность стерилизации, высокая стоимость, возможность побочного действия химического агента на обслуживающий персонал и, тем не менее, для ряда лекарственных препаратов — это единственно надежный способ стерилизации в современных условиях. Использование консервантов. Добавление консервантов условно можно отнести к методам химической стерилизации. Введение консервантов в растворы проводится в тех случаях, когда нельзя гарантировать сохранение стерильности. При этом возможно снижение температуры стерилизации или сокращение времени ее проведения. Механизмы воздействия консервантов на микроорганизмы очень различны и определяются их химическим строением. Основным результатом при этом является нарушение жизненных функций клетки, в частности, инактивация белковой части клеточных ферментов. В зависимости от степени инактивации наступает либо гибель клетки, либо замедление ее жизненных функций. 3. Физические методы стерилизации Тепловая (термическая) стерилизация. В настоящее время монопольное положение среди возможных методов стерилизации в фармацевтическом производстве занимает тепловая стерилизация. В зависимости от температурного режима тепловая стерилизация подразделяется на: · паром под давлением (автоклавирование); Стерилизация паром под давлением. Автоклавирование — это стерилизация растворов, устойчивых к нагреванию, паром под давлением 1,1 атм при температуре 119-121°С. В данных условиях погибают не только вегетативные, но и споровые микроорганизмы за счет коагуляции белка клетки. Этот традиционный способ стерилизации обладает сегодня преимуществом перед другими по трем причинам. Во-первых, он дает возможность стерилизации препаратов в конечной герметичной упаковке, что исключает опасность вторичной контаминации. Во-вторых, благодаря длительной практике использования он обеспечен достаточно надежной аппаратурой. И, в-третьих, на сегодняшний день он наиболее экономичен. При этом методе происходит комбинированное воздействие на микроорганизмы высокой температуры и влажности, при этом погибают самые стойкие споры. Коагуляция белковых веществ в этих условиях начинается при температуре 56°С. Стерилизацию паром под давлением проводят в стерилизаторах различной конструкции цилиндрической или квадратной формы. Стерилизаторы квадратной формы типа АП-7 (рис. 5.25.), АП-18 имеют двери с двух сторон: через одну происходит загрузка нестерильной продукции; через другую — выгрузка простерилизованной. Корпус автоклава нагревается глухим паром, чтобы не было его конденсации в рабочей камере. Затем в камеру для вытеснения воздуха подается острый пар. Отчет времени стерилизации начинается с момента достижения заданного давления по манометру. Стерилизаторы оснащены автоматической контрольной аппаратурой, с помощью которой на контрольной ленте записывается давление и время стерилизации. Условия стерилизации продукции указаны в промышленных регламентах или другой нормативно-технической документации. Стерилизацию растительных масел и жиров в заводских условиях осуществляют паром под давлением в герметически закрытых сосудах при температуре 119-121°С и давлении 1,0-1,1 атм. в течение 2 часов. Автоклавированию также подвергаются установки для стерилизующего фильтрования, фильтрующие перегородки и другой вспомогательный материал, используемый в технологическом процессе производства инъекционных лекарственных форм. Среди недостатков метода можно выделить невозможность стерилизации растворов, содержащих термолабильные вещества, опасность работы с паром под давлением, отсыревание многих материалов во время стерилизации и др. Стерилизация текучим паром. Растворы веществ, термически малоустойчивые, иногда стерилизуют при 100°С текучим паром (без примеси воздуха и избыточного давления). Насыщенный пар убивает только вегетативные формы микроорганизмов и при наличии в объекте споровых форм этот метод неэффективен. Тиндализация (дробная стерилизация). Для термолабильных веществ, а также для растворов в шприц-ампулах стерилизацию иногда проводят методом тиндализации. Суть метода заключается в трехкратном нагревании растворов до 40-60°С с перерывами в сутки, в течение которых объекты термостатируют при температуре 37±1°С для прорастания споровых форм в вегетативные. Стерилизация сухим жаром (воздушная стерилизация). Стерилизация сухим жаром, проводимая в аэростерилах или других аппаратах этого типа, также высокоэффективна. При этом погибают все формы микроорганизмов за счет пирогенетического разложения белковых веществ. Однако, высокая температура нагрева (160-200°С), длительное время воздействия (1-2 часа) и сухой горячий воздух оказывает повреждающее действие на стерилизуемые объекты и, следовательно, ограничивают возможности данного способа. Инъекционные растворы не подвергают стерилизации сухим жаром, так как из-за плохой теплопроводности воздух не обеспечивает быстрый нагрев растворов до температуры стерилизации, а длительный прогрев — приводит к разложению большинства лекарственных веществ. Сухим жаром стерилизуют некоторые термостойкие порошки, масла, стеклянную тару (ампулы, флаконы и необходимую посуду), вспомогательные материалы. Лучшими являются стерилизаторы с ламинарным потоком стерильного воздуха, нагретого до требуемой температуры, что улучшает создание равномерного температурного поля и устраняет загрязнения от обогреваемых стенок камеры и из воздуха, попадаемого в момент выгрузки объекта. Радиационная стерилизация. Лучистая энергия губительно действует на клетки живого организма, в том числе и на различные микроорганизмы. Принцип стерилизующего эффекта этих излучений основан на способности вызывать в живых клетках при определенных дозах поглощенной энергии такие изменения, которые неизбежно приводят их к гибели за счет нарушения метаболических процессов и коагуляции белка. Источником ионизирующих г-излучений служат долгоживущие изотопы 60Со27, 137Cs55, ускорители электронов прямого действия и линейные ускорители электронов. Для бактерицидного эффекта достаточно от 15 до 25 кГр, причем верхний предел необходим для инактивации споровых форм. В настоящее время накоплен большой опыт применения этого метода, точно установлены типичные дозы излучения, необходимые для надежной стерилизации, разработано радиационное оборудование для высокопроизводительного процесса стерилизации, решены вопросы безопасности работы установок для обслуживающего персонала. Этот метод по экономическим показателям превосходит асептическое изготовление растворов со стерильной фильтрацией, но несколько уступает тепловой стерилизации. Однако, в будущем может приблизиться к ней из-за неизбежного снижения относительной стоимости изотопов, которые являются побочным продуктом атомной энергетики. Ультразвуковая стерилизация. Прохождение ультразвука (УЗ) в жидкой среде сопровождается чередующимися сжатиями, разрежениями и большими переменными ускорениями. В жидкости образуются разрывы, называемые кавитационными полостями. В момент сжатия эти полости захлопываются. Избыточное давление, создаваемое УЗ-волной, накладывается на постоянное гидростатическое и суммарно может составлять в пузырьках несколько атмосфер. В качестве «зародышей» кавитационных полостей могут быть пузырьки газа, пара в жидкости, твердые частицы и места неровностей твердой поверхности. Большие импульсные давления кавитаций приводят к разрушению целостности клеточной мембраны микроорганизмов, споровых образований и других частиц. Важно установить оптимальные параметры процесса стерилизации, так как высокие импульсные давления могут приводить к механическому разрушению ампул. Стерилизующая частота звука должна быть в пределах 18-22 кГц. И, хотя метод очень эффективен, он не нашел широкого применения из-за сложности аппаратурного оснащения и возможных сложных химических превращений компонентов растворов. Вопросы стабильности компонентов при УЗ-стерилизации имеют много общего с аналогичными проблемами радиационной стерилизации. Для повышения устойчивости лекарств при ультразвуковом воздействии необходимо подобрать такие условия стерилизующей обработки, которые обеспечивают снижение вводимой в систему энергии на тех частотах ультразвука, которые одновременно со стерилизацией не приводят к разложению компонентов лекарственных препаратов. Чаще метод применим при производстве эмульсий и суспензий с целью лучшего диспергирования веществ в них и одновременно получения стерильных гетерогенных систем для парентерального применения. Стерилизация токами высокой и сверхвысокой частоты. К настоящему времени нет единой точки зрения на механизм инактивации микроорганизмов при ВЧ- и СВЧ-облучении. Существует мнение об исключительно тепловом механизме действия токов высокой частоты на биологические объекты. Принцип действия высокочастотного поля заключается в его активном воздействии на ориентацию молекул вещества. Изменение направленности поля вызывает изменение ориентации молекул и поглощение части энергии поля веществом. В результате происходит быстрый нагрев вещества во всех точках его массы. Менее широко распространены представления о том, что, помимо тепловых процессов, на гибель микроорганизмов оказывает влияние специфическое действие ВЧ- и СВЧ-излучения. С помощью СВЧ-энергии возможно стерилизовать в расфасованном виде готовую продукцию: глазные мази, пасты в тубах, лекарственные средства в конвалютах, порошки, таблетки, пористые лиофилизированные массы, не содержащие гидрофильные жидкости. Стерилизация ампулированных растворов и жидких лекарственных форм, укупоренных герметически нежелательна, так как в замкнутой емкости возникает избыток давления паров испарившейся жидкости, взрывающий ее. В результате наступает разгерметизация в виде растрескивания стенок ампул или срыва укупорочного материала. Метод также не нашел широкого применения из-за сложности аппаратурного оснащения и возможности неблагоприятного воздействия быстрого кратковременного нагрева инъекционного раствора. Стерилизация ультрафиолетовым излучением. Из-за возможности образования ядовитых продуктов и возможности разложения биологически активных компонентов инъекционных растворов под действием УФ-излучения, метод не нашел своего применения для стерилизации препаратов для инъекций. Однако он широко используется для стерилизации порошков, воды для инъекций, вспомогательных материалов, воздушной среды производственных помещений, технологического оборудования и других объектов. При стерилизации воздушной среды производственных помещений в качестве источников УФ-радиации используют специальные лампы БУВ (бактерицидная увиолевая), которые изготавливают в виде трубки из специального увиолевого стекла, способного пропускать УФ-лучи, с электродами из длинной вольфрамовой спирали, покрытой бария и стронция гидрокарбонатами. В трубке находится ртуть и аргон при давлении в несколько мм рт.ст. Источником УФ-лучей является разряд ртути, происходящий между электродами при подаче на них напряжения. Излучение лампы БУВ обладает большим бактерицидным действием, так как максимум излучения лампы близок к максимуму бактерицидного действия (254 нм). стерильный фильтрующий микроорганизм Количество и мощность бактерицидных ламп подбирается так, чтобы при прямом облучении на 1 м3 объема помещения приходилось не менее 2-2,5 Вт мощности излучателя. Промышленностью выпускаются лампы БУВ-15, БУВ-30, БУВ-60 и др. (цифра обозначает мощность в Ваттах), а также бактерицидные облучатели: настенный ОБН, состоящий из двух ламп БУВ-30; потолочный ОБП — из 4 ламп БУВ-30; передвижной маячного типа ОБПЕ — из 6 ламп БУВ-30. Облучатели используют только при отсутствии в помещении людей. Для стерилизации воды применяют аппараты с погруженными и непогруженными источниками УФ-радиации. В аппаратах первого типа источник УФ-излучения (бактерицидная увиолевая лампа, покрытая кожухом из кварцевого стекла) помещается внутри водопровода и обтекается водой. Данный способ стерилизации больших объемов воды для инъекций является наиболее экономичным. В аппаратах с непогруженными лампами последние помещаются над поверхностью облучаемой воды. В связи с тем, что обычное стекло практически непроницаемо для ультрафиолетовых лучей, водопровод в местах облучения делают из кварцевого стекла, а это значительно повышает стоимость аппарата. В настоящее время разработана возможность замены кварцевого стекла полиэтиленовым, свободно пропускающим УФ-радиацию. Как положительный фактор, следует отметить, что при стерилизации воды не происходит накопления пероксидных соединений и под действием УФ-излучения инактивируются некоторые пирогенные вещества, попавшие в воду. Стерилизация ИК и лазерным излучением. Электронная стерилизация. Эти перспективные виды стерилизации практически не находят сегодня применения, хотя возможности для этого имеются. Облучение инъекционных водных систем инфракрасным (ИК) излучением в областях поглощения воды (l = 2,7 мкм) может быть эффективным средством ее нагрева и тем самым является по сути еще одним вариантом тепловой стерилизации. Наличие достаточно мощных источников ИК-излучения позволяет надеяться на возможность создания оборудования для высокопроизводительной технологии. Преимуществом этого метода перед традиционным автоклавированием может считаться возможность отказа от небезопасного в обслуживании и нетехнологичного перегретого пара. Принципиально возможны способы стерилизации с применением лазерного и электронного излучения, при этом можно достичь высокой эффективности стерилизации как путем интенсивного нагрева вследствие поглощения мощного излучения в воде, так и за счет селективного поглощения излучения макромолекулами микроорганизмов в многоквантовых процессах. Однако исчерпывающих исследований применительно к какой-либо конкретной системе, совокупность которых дала бы основание о создании хотя бы основ таких методов стерилизации, пока не проведено. Размещено на Allbest.ru Подобные документыМетоды изучения морфологии микроорганизмов. Правила работы в микробиологической лаборатории. Микроскопия в светлом поле. Установка света по Келеру. Изображения фиксированных препаратов, полученные в результате исследования метода изучения морфологии. лабораторная работа [925,0 K], добавлен 14.05.2009 Организация лабораторной микробиологической службы. Принципы микробиологической диагностики инфекционных заболеваний. Методы выделения и идентификации бактерий, вирусов, грибковых инфекций, простейших. реферат [3,8 M], добавлен 05.05.2006 Исследование возможности и процессов адаптации микроорганизмов в экстремальных условиях космоса при анализе характеристик их жизнеспособности и пластичности. Физиологические процессы микроорганизмов в космосе. Проблемы микробиологической безопасности. реферат [18,4 K], добавлен 10.12.2010 Споры – форма бактерий с грамположительным типом строения клеточной стенки. Роль спорообразования бактерий и грибов для практики. Строение и особенности химического состава бактериальной споры. Микробиологическое обоснование пастеризации и стерилизации. контрольная работа [223,5 K], добавлен 02.10.2011 Роль микроорганизмов в круговороте азота, водорода, кислорода, серы, углерода и фосфора в природе. Различные типы жизни бактерий, основанные на использовании соединений различных химических веществ. Роль микроорганизмов в эволюции жизни на Земле. реферат [20,2 K], добавлен 28.01.2010 Источник |