- Новинка в наших Здравницах! Концентрат для безалкогольного напитка «Гуминовый комплекс»
- Гуминовый комплекс способ применения
- Питьевое применение содержащей гуминовые кислоты минеральной воды у пациентов с хроническим гепатитом при санаторном лечении
- Фульват жидкость для внутреннего применения 200мл
- Описание
- Состав и описание
- Гуминовый комплекс способ применения
- Гуминовый комплекс способ применения
Новинка в наших Здравницах! Концентрат для безалкогольного напитка «Гуминовый комплекс»
Биокомплекс природных гуминовых и фульвовых кислот –
аналог натурального мумиё
Концентрат для приготовления оздоравливающих напитков Гуминовый комплекс представляет собой высококонцентрированный комплекс природных гумино-фульвовых кислот.
Активированные гуминовые и фульвокислоты естественного происхождения имеют широкий спектр действия на организм человека. Напиток из концентрата эффективен при вирусных и бактериальных инфекциях, стрессах и переутомлении, аллергиях, дисбактериозах, интоксикациях, после антибиотико-, радио- и химиотерапии в качестве гепатопротектора, иммунопротектора, мощного антиоксиданта с выраженной противовоспалительной активностью. При употреблении активируется клеточный метаболизм и тканевое дыхание, что ускоряет регенеративные процессы, повышает тонус и выносливость организма.
Гуминовый комплекс помогает организму бороться с большинством вирусных инфекций. Он полезен при первых симптомах ОРВИ, гриппа и болезней, вызванных вирусом герпеса. Гуминовые кислоты подавляют активность вирусов и не позволяют им проникать в клетки. Напиток способствует быстрому выведению вируса из организма и скорейшему выздоровлению.
Повышает эффективность работы иммунной системы. Гуминовый комплекс является мощным антиоксидантом, связывает свободные радикалы, повышает защитные силы организма и помогает бороться со стрессом и переутомлением. Гуминовые вещества улучшают самочувствие, повышают выносливость при физических и умственных нагрузках.
Напиток Гуминовый комплекс нормализует работу желудочно-кишечного тракта. Он создаёт на поверхности слизистой оболочки ЖКТ барьерный слой, который защищает её от воздействия агрессивных факторов и не позволяет проникать в кровь токсинам и вредным веществам. Устраняет симптомы «протекающего кишечника». Гуминовые вещества благотворно влияют на микрофлору кишечника и быстро устраняют дискомфорт после приема антибиотиков. Эти соединения являются мощным энтеросорбентом и быстро устраняют диарею и другие нарушения пищеварения.
Гумино-фульвовые кислоты помогают организму справиться с интоксикацией, защищают и восстанавливают клетки печени, связывают все инородные вещества и выводят из организма тяжелые металлы, продукты распада никотина и алкоголя, пестициды, а также вещества, попадающие в организм в ходе радио- и химиотерапии и др. Отличаются антибактериальной активностью. Гуминовыми кислотами уничтожаются патогенные микроорганизмы и вместе с токсинами выводятся естественным путем без интоксикации. Гуминовая кислота оказывает и противоаллергический эффект — связывает и выводит из организма аллергены.
Напиток Гуминовый комплекс помогает снимать отёки, ускоряет заживление ран и восстановление тканей, обладает сильными противовоспалительными свойствами. Гуминовые кислоты незаменимы, если необходимо ускорить заживление ран, язв. Уменьшают реабилитационный период при переломах и ушибах, артритов, артрозах.
Гуминовая кислота способна распознавать и выводить липопротеиды и холестерин, то ее можно эффективно использовать в борьбе с атеросклерозом, который часто становится причиной инфарктов и других сердечных патологий.
Не вызывает привыкания и аллергических реакций.
Вода питьевая, комплекс гумино-фульвовых кислот (содержит минералы, аминокислоты, фитонутриенты ,полисахариды, полифенолы, кетоны, катехины, дубильные вещества, изофлавоноиды, хиноны. Макро- и микроэлементы в составе: кремний, натрий, калий, кальций, сера, железо).
Перед употреблением взболтать. 5 мл концентрата (1 чайная ложка) развести в 2 литрах воды очищенной, не хлорированной воды. Приготовленный напиток можно хранить в холодильнике до 7 дней. Перед применением взболтать. Принимать от 1 до 7 раз в день по одному стакану напитка, желательно за 20-30 минут до еды.
Разбавлять водой 1:400 , например: 10 миллилитров (2 чайные ложки) на 4 литра воды или на бутыль емкостью 19-20 л воды добавить 50мл концентрата.
Готовый напиток после разведения с водой должен быть использован в соответствии с инструкцией употребления воды.
Готовый к употреблению напиток используется для ингаляций и промывания глаз и носа.
Для компрессов следует намочить готовым раствором ткань и наложить ее на проблемные участки. Затем закрыть эту область полиэтиленом или вощеной бумагой и теплой шерстяной тканью.
Ограничения к применению: Индивидуальная непереносимость отдельных компонентов в составе продукта
Срок годности: 36 месяцев, при комнатной температуре не выше +25°С, в темном сухом месте. После вскрытия упаковки хранить в темном прохладном месте не более 12 месяцев.
Источник
Гуминовый комплекс способ применения
Научно-практический рецензируемый ежемеcячный журнал. Орган Министерства здравоохранения Республики Беларусь Журнал издается с 1924 года.
Адрес редакции: 220007 Минск, ул. Фабрициуса, 28-402.
Тел.: 368-21-66 (-67,-48), 368-86-82 Тел./факс: 368-21-66, 368-86-82 E-mail: zdrav@tut.by
Питьевое применение содержащей гуминовые кислоты минеральной воды у пациентов с хроническим гепатитом при санаторном лечении
Представлены результаты изучения эффективности питьевого применения минеральной воды, содержащей гуминовые кислоты, в санаторно-курортных условиях у 71 пациента с хроническим гепатитом. Показано, что включение в стандартную схему санаторного лечения пациентов с хроническим гепатитом питьевого применения хлоридно-гидрокарбонатной натриевой маломинерализованной минеральной воды с оптимизированным содержанием гуминовых кислот (около 20 мг/дм3) сопровождается более значимой положительной динамикой лабораторных показателей (аспартатаминотрансфераза, аланинаминотрансфераза, щелочная фосфатаза, гамма-глутамилтранспептидаза) и качества жизни.
Согласно данным ВОЗ, хронические заболевания печени являются широко распространенными и их число за последние годы значительно возросло. Резкому увеличению распространенности данной патологии способствуют рост заболеваемости острыми вирусными гепатитами, злоупотребление алкоголем, а также значительный удельный вес пациентов, страдающих ожирением и сахарным диабетом, что является частой причиной развития неалкогольной жировой болезни печени [1, 2]. В связи с гепатотоксичностью многих современных лекарственных средств актуален поиск доступных и эффективных методов терапии хронического гепатита.
Большого внимания в лечении хронических заболеваний печени заслуживает применение природных факторов, прежде всего минеральных вод. В принадлежащем ОАО «Мозырский НПЗ» санатории «Сосны» для лечения и реабилитации пациентов используется минеральная вода, характеризующаяся высокой (до 300 мг/дм3) концентрацией гуминовых кислот. Данная минеральная вода в связи со столь высоким содержанием органических веществ является уникальной, поскольку сходных по составу и бальнеотерапевтическим показателям источников минеральных вод в Европе существует лишь несколько: в Польше— в окрестностях г. Познань; в Германии — г. Брамштадт и в Российской федерации — г. Екатеринбург. Все они в настоящее время активно изучаются.
Ранее было проведено изучение физиологического действия данной минеральной воды с различным содержанием гуминовых кислот при внутреннем применении у животных с экспериментальным парацетамоловым гепатитом [3—6]. В результате выполненных комплексных исследований установлено, что наибольшую терапевтическую эффективность у животных с экспериментальным гепатитом оказывает внутренний курсовой прием (в течение 21 сут) минеральной воды с содержанием гуминовых кислот 21 ,5 мг/дм3, что сопровождается (по сравнению с контролем) достоверным улучшением антитоксической функции печени, повышением основного обмена, уменьшением воспалительных изменений, нормализацией активности печеночных ферментов(аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), щелочная фосфатаза (ЩФ) и лактатдегидрогеназа (ЛДГ)), повышением белковосинтетической функции (увеличение содержания общего белка и альбумина), а также положительной динамикой со стороны морфологических изменений органа. Все указанные сдвиги наиболее выражены на 21-е сутки поения животных и в фазе последействия минеральной воды.
Цель настоящего исследования — изучить терапевтическую эффективность питьевого применения минеральной воды с установленными оптимальными параметрами у пациентов с хроническим гепатитом в санаторно-курортных условиях.
Источник
Фульват жидкость для внутреннего применения 200мл
| Производитель: | ПЛАЗА-СИТИ |
| Завод производитель: | Плаза-Сити, Россия |
| Форма выпуска: | раствор для приема внутрь |
| Количество в упаковке: | 200 мл |
| Действующие вещества: | фолиевая кислота |
| Возраст от: | 18 лет |
| Дозировка: | 200 мкг/5 мл |
| Назначение: | Витамины группы В |
Описание
Состав и описание
Активное вещество:
Вода, экстракт шелухи овса, экстракт околоплодника кедровых орехов, экстракт кофе натурального жареного молотого.
Содержание активных веществ в 1 мл:
фульвовая кислота — 3 мг;
Фолат-0,04 мг
Описание:
Продукт действует на активацию иммунной системы организма человека. Позволяет защитить от агрессивного воздействия внешней окружающей среды, вирусов, инородных болезнетворных бактерий.
Фульвовая кислота вступает в реакцию с минералами и разбивает их на частицы ионного размера, образуя фульваты — наименьшие из возможных форм минералов. Именно в такой форме минералы легко усваиваются организмом человека. Низкий молекулярный вес обеспечивает проницаемость фульвовой кислоты через клеточную мембрану. Насыщенная полезными веществами и ионами, фульвовая кислота является отличным проводником для витаминов и минералов в теле растения или человека.
Изготовлен из натурального растительного сырья. Повышает усвоение витаминов, БАДов и микроэлементов. Обеспечивает чистку клеток, в том числе печени от ненужных скопившихся элементов.
Форма выпуска:
Флакон 200 мл
Источник
Гуминовый комплекс способ применения
Окисленные бурые угли Гусиноозерского месторождения Республики Бурятия содержат значительное количество гуминовых кислот (до 90% от органической массы угля). Гуминовые кислоты представляют собой высокомолекулярные, склонные к ассоциации полифункциональные природные лиганды. Наличие карбоксильных и фенольных групп в структуре гуминовых кислот обеспечивает образование прочных комплексов этих кислот с ионами металлов, в том числе с ионами тяжелых металлов. Поэтому представляется возможным использовать их в качестве сорбентов для очистки сточных вод и детоксикации почв от ионов тяжелых металлов.
Таблица 1. Зависимость степени извлечения Fe 3+ и Cu 2+ от расхода гуматов аммония
Расход сорбента, г/л
Расход сорбента, г/л
Для исследования взаимодействия ионов железа Fe 3+ , меди Cu 2+ , никеля Ni 2+ и цинка Zn 2+ с гуминовыми кислотами применяли исходные растворы FeCl3, CuSO4, Ni(NO3)2 и Zn(CH3COO)2 с концентрацией 100-1000 мг/л (в пересчете на металл) и водные растворы гуматов калия, натрия и аммония с концентрацией 20 г/л. Сорбцию проводили в статических условиях при перемешивании в течение 15 мин при температуре 20 0 С. Концентрацию ионов железа в маточном растворе контролировали фотоколориметрическим методом при взаимодействии с салициловой кислотой в слабощелочной среде, меди — с диэтилдитиокарбаматом натрия, никеля — с диметилглиоксимом в щелочной среде (в присутствии окислителя), а цинка — с родамином С до и после контакта с сорбентом.
Степени извлечения металлов рассчитывали по разности исходной и остаточной концентраций.
Изучена зависимость степени извлечения ионов Fe 3+ и Cu 2+ от расхода гуматов калия, натрия и аммония при рН 2-3 для различных концентраций СFe3+ и ССu 2+ и определены оптимальные расходы сорбента. Оптимальным расходом сорбента считали минимальное количество сорбента, необходимое при данных условиях для максимального извлечения металла.
В таблице 1 представлены результаты исследования зависимости степени извлечения ионов железа и меди от расхода гуматов аммония. Аналогичные зависимости характерны для гуматов калия и натрия. Как видно из таблицы, при увеличении исходного содержания железа (III) и меди (II) в растворе расход сорбента повышается.
Зависимость оптимального расхода сорбента от концентрации Fe 3+ и Cu 2+ в исходном растворе обрабатывали методом наименьших квадратов с использованием экспериментальных данных опыта (рис. 1). В интервале концентраций 100-1000 мг/л график с вероятностью 99,0% интерпретируется прямой, что позволяет рассчитывать оптимальные расходы сорбента для растворов промежуточных концентраций.
Оценка степени извлечения Ni 2+ и Zn 2+ проводилась только из растворов с концентрацией 1000 мг/л при рН 1 и 2 соответственно. Результаты приведены в таблице 2. Гуматы аммония, калия и натрия практически одинаково связывают Ni 2+ и Zn 2+ .
Интересно отметить, что при взаимодействии катионов железа с гуматами достигается высокая степень очистки воды (до 99%), тогда как катионы меди, никеля и цинка связываются с гуматами слабее (до 80%). Ионы Cu 2+ , Ni 2+ и Zn 2+ относятся к ярко выраженным комплексообразователям и помимо замещения Na + , K + и NH4 + в карбоксильных группах образуют координационные связи с другими группами (амино- и метоксигруппы, эфирный кислород и т.д.) — донорами электронов, присутствующими в структуре гуминовых кислот. Такие комплексные соединения — хелаты — обладают более высокой растворимостью по сравнению с обычными солями, чем можно объяснить довольно высокую концентрацию меди и никеля в маточном растворе.
Таблица 2. Зависимость степени извлечения Ni 2+ и Zn 2+ от расхода гуматов аммония
Источник
Гуминовый комплекс способ применения
Гуминовые соединения природного происхождения относятся к высокоэффективным веществам, обладающим полисистемным фармакологическим действием, обусловленным иммуно-стимулирующими, регенераторными, противовоспалительными свойствами [1]. В растворах они в основном присутствуют в диссоциированном состоянии (кислоты). Данные кислоты характеризуются подобием структурного ароматического углеродного скелета с функциональными группами (карбоксильные, гидроксильные, метоксильные и алкильные группы) и периферической группой соединений, обогащенных полисахаридными и полипептидными фрагментами. При гидролизе кислоты в раствор переходят в основном ее низкомолекулярные фрагменты, амино- и моносахариды. Гуминовые соединения по составу подобны аминокислотам, находящимся в растениях и бактериальной плазме в тех же соотношениях, что и в природной среде [2].
Биологическая эффективность препаратов на основе гуминовых кислот четко определяется местом их добычи, идентичностью по составу, природным композициям и их содержанием в водной среде, в основном в малых и относительно больших диапазонах концентраций. Их абсолютная активность определяется уровнем концентрации образующихся перекисных анионных радикалов в диапазоне от 10 до 20 мкг/л, что обеспечивает поддержание электрического равновесия клеточных мембран и органелл и сопровождается активацией энергетической системы клетки (окислительной фосфорилирующей системы и АТФ-продуцирующей способности АТФ-синтазы митохондрий клеток), а также усиливает каталитическое действие клеточных ферментов и коферментов, восстанавливает активность электронно-транспортных цепей клеточного гомеостаза, усиливает антиоксидантную активность и резервы адаптации клеточного иммунитета [3].
Механизм фармакологического действия данных препаратов связывают, как правило, с адсорбционной способностью кислот, ионообменом и комплексообразованием [2]. Однако не представляется возможным выделить из смеси гуминовых веществ действующее начало, так как разделение смеси кислот приводит к потере их фармакологических свойств. До настоящего времени ни одному из исследователей не удалось выделить в структуре макромолекул гуминовых кислот участок или функциональные группы, определяющие конкретный вид биологической активности [4]. Очевидно, что подобные особенности данных препаратов не связаны с единым механизмом действия, предполагающим исключительно контактные физико-химические процессы превращения веществ и их связывание.
В последние годы обращается внимание на принципиально иные механизмы действия природных соединений и воды, основанные на квантовых обменных процессах между квантово-сопряженными системами. В подобных сопряженных системах участником взаимодействия, с одной стороны, является водный раствор гуминовых кислот, а с другой – природный резервуар энергии делокализованных электронов (грунты) [5].
В квантовой физике под сопряженными объектами понимаются идентичные по физическим свойствам объекты, квантовое взаимодействие между которыми определяется делокализованными электронами в структурах аморфного вещества (фазы ассоциированной воды), что предполагает идентичность их строения, а также, возможно, подобие других особенностей макроскопического квантового объекта (формы, пространственной структуры, микроскопической организации, квантового состояния) [6, 7]. Как правило, такие условия возникают при разделении изотропного по составу макроскопического объекта. Например, воду из одного сосуда разливают в две емкости, между которыми устанавливается квантовое сопряжение, которое поддерживается до тех пор, пока химический состав образцов и структурная организация фазы ассоциированной воды существенно не изменились под влиянием внешней среды. Данное физическое явление известно в квантовой физике как квантовая нелокальность, которая может наблюдаться не только для элементарных частиц, но и для макроскопических объектов, находящихся в квантово-коррелированном состоянии [7, 8].
Однако само по себе квантовое сопряжение между взаимодействующими объектами недостаточно для реализации эффективного переноса электронов. Интенсификация обменных электронных процессов между сопряженными объектами требует дополнительных условий, которыми является возбуждение квантовой системы, реализуемое при возникновении фазовых неустойчивостей в ассоциированной воде, являющейся носителем делокализованных электронов [9].
В квантово-сопряженной системе растворов гуминовых соединений исходным донором электронов являются грунты залегания пелоидов. Гуминовые кислоты в пелоидах характеризуются высокими отрицательными значениями окислительно-восстановительного потенциала, которые достигают в анаэробных условиях грунтов максимальных величин в летнее время (Еh = –810мВ), а минимальных – в весенний период (Еh = –390 мВ). Продукты анаэробного микробиологического превращения пелоидов и образуемые из них надкислоты (при увлажнении грунтов и частичной аэрации) обеспечивают высокие электрон-донорные свойства полугидроморфных почв болот. Их абсолютная активность определяется уровнем концентрации образующихся перекисных анионных радикалов в диапазоне от 10 до 20 мкг/л, что обеспечивает поддержание электрического равновесия клеточных мембран и органелл и сопровождается активацией энергетической системы клетки (окислительной фосфорилирующей системы и АТФ-продуцирующей способности АТФ-синтазы митохондрий клеток), а также усиливает каталитическое действие клеточных ферментов и коферментов, восстанавливает активность электронно-транспортных цепей клеточного гомеостаза, усиливает антиоксидантную активность и резервы адаптации клеточного иммунитета.
Для реализации акцепторной способности препарата, находящегося в нелокальном квантовом сопряжении с донором электронов (электрически активными грунтами), необходимо возбуждение квантовой системы водного раствора препарата (акцептора электронов). Это достигается тем, что в процессе растворения препарата в воде гуминовые кислоты оказывают модулирующее влияние на состояние фазы ассоциированной воды. При этом происходит увеличение доли фазы ассоциированной воды [5]. В ней появляются дополнительные дефекты структуры с парамагнитным кислородом (О^^2), служащие ловушками для делокализованных электронов (2е-). Протекающие квантово-физические процессы могут быть представлены схемой, согласно которой на начальном этапе образуется короткоживущий супероксидный анион-радикал (О2-(*)(Н2О)асс.), а затем относительно стабильный пероксид-анион-радикал (НО2 -(*) (Н2О)асс.):
где (Н 2 О)асс. – структуры фазы ассоциированной воды [9].
Следовательно физический механизм усиления электрон-донорной способности водных растворов гуминовых препаратов, связанный с растворением препаратов, заключается в инициировании квантовой конденсации электронов (стимулированном запуске процесса квантовой конденсации) из пространственно сопряженных структур грунтов с низкими значениями окислительно-восстановительного потенциала с последующим накоплением нестабильных анион-радикалов в фазе ассоциированной воды, которая при попадании в организм распадается с переносом электронов на водные структуры мембран (акцепторы электронов).
Цель исследования: изучение электрон-донорной активирующей способности растворов гуминовых кислот (концентрата биодоступных органических кислот, полученного из реликтовых природных органических месторождений, производитель – ООО «Вио-Фарм» (далее «гуминовый концентрат»)) за счет нелокального взаимодействия их с электрон-донорными грунтами, согласующимися по составу и структуре с гуминовыми веществами, используемыми для приготовления препарата.
Материалы и методы исследования
Исследования процессов нелокального переноса электронов на водную среду проводились при постоянной температуре (35 °С) на свежеприготовленных растворах препарата («гуминовый концентрат») различной концентрации в термостатируемых условиях (термостат «Biosan»). Регистрация переноса электронов на водную среду осуществлялась по изменению значений окислительно-восстановительного потенциала (прибор рН-013 – высокоточный прибор для измерения рН, ОВП и температуры воды) и концентрации пероксидных анион-радикалов (кинетический хемилюминесцентный анализатор ЛИК [9]). Растворы препарата готовились на предварительно термостабилизированной воде в различных концентрациях в полимерных емкостях (0,5 л) и снова помещались в термостат. Определение значений окислительно-восстановительного потенциала растворов проводилось периодически с интервалом в несколько минут между измерениями.
Нелокальная активирующая способность растворов оценивалась по изменению концентрации пероксидных анион-радикалов (НО2-(*)) в дистиллированной воде, находящейся в непосредственном контакте с исследуемым раствором препарата при комнатной температуре из-за окрашивания растворов препарата, что затрудняет фиксацию анион-радикалов при использовании хемилюминесценции.
Результаты исследования и их обсуждение
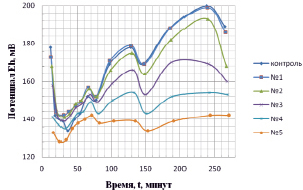
Анализ зависимости, приведенной на рис. 1, показывает, что абсолютные величины потенциала (Eh), устанавливающего процесс накопления электронов в форме анион-радикалов в воде, зависят от количества вносимого в воду препарата. Чем выше концентрация препарата, тем ниже значения окислительно–восстановительного потенциала. Снижение потенциала (активация раствора) протекает во времени в течение первых 20 мин.
Кроме того, полученные кинетические зависимости изменений Еh-потенциала указывают на периодическую осцилляцию его значений, что отражает наличие в растворах конкурирующих процессов активации и дезактивации (обменное взаимодействие с нелокальным источником электронов [9]) во времени. Синхронные изменения Eh в контрольном и опытных образцах свидетельствуют о вовлечении в обменные электронные процессы не только нелокальных источников электронов, но и о наличии вневременных изменений в собственных состояниях растворов (нелокальность 2 рода [10, 11]). При этом временные осцилляции потенциалов синхронизированы во времени, что позволяет утверждать, что процесс квантового взаимодействия образцов носит периодический макроскопический характер.
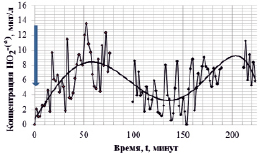
Параллельно осуществлялись измерения динамики концентрации пероксидных анион-радикалов в дистиллированной воде, находившейся в контакте со свежеприготовленным раствором препарата. Как следует из данных, представленных на рис. 2, в динамике концентрации пероксидных анион-радикалов (аппроксимирующая линия) отмечаются временные неравномерные колебания. Так, в интервале 0–50 мин происходит рост активности, а затем последующее ее падение. Повторный «всплеск» активности отмечается в интервале экспозиции 180–220 мин (в условиях настоящего эксперимента).
Подобное изменение каталитической активности раствора отражает, так же как и на предыдущем графике, эффекты не только пространственной, но и временной нелокальности процессов активации, проявляющихся в знакопеременных направлениях потоков электронов между двумя квантовыми объектами.
Активные состояния растворов сохраняются в течение 20–80 мин от начала экспозиции. В последующие интервалы времени растворы теряют свою активность и по истечении времени порядка 170 мин они приобретают электрон-акцепторные свойства, что может оказывать отрицательное влияние на организм человека.
Рис. 1. Динамика изменений значений окислительно-восстановительного потенциала растворов гуминовых кислот (препарат «гуминовый концентрат»). Разведения в отстоянной водопроводной воде: № 1 – контроль; № 2 – 15 мл/л; № 3 – 30 мл/л; № 3 – 60 мл/л; № 4 – 90 мл/л; № 5 – 120 мл/л концентрата раствора кислот (концентрация – 1 г/л)
Рис. 2. Динамика изменений средних значений концентрации (сплошная кривая) и временные осцилляции концентрации (кривая с маркерами) пероксидных анион-радикалов в дистиллированной воде при неконтактном действии смесевого раствора гуминовых кислот (объем активирующего раствора с концентрацией препарата «гуминовый концентрат» 90 мл/л – 1 л, объем воды в полипропиленовой емкости, размещенной в емкости с активирующим раствором – 250 мл). Стрелка указывает на момент разведения препарата
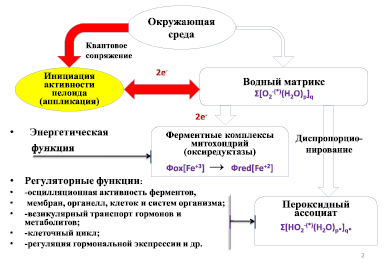
Рис. 3. Схема основных транспортных путей переноса электронов в квантово–сопряженной системе «грунт – раствор препарата – организм» в процессе взаимодействия организма человека с активированным раствором препарата «гуминовый концентрат»
Из этого следует, что эффекты квантовой нелокальности электрически активных структур пелоидов (препаратов) и технологии, реализующие эти процессы, являются определяющими, обеспечивающими перенос электронов из квантово-сопряженных структур грунтов на водные растворы препарата. Это формирует высокую биологическую эффективность свежеприготовленных растворов гуминовых кислот.
Полученные экспериментальные результаты показывают, что инициация процесса активации препарата на основе гуминовых кислот при его растворении в воде отрывает дополнительный канал поступления электронов из квантово-сопряженных грунтов на водную квантово-коррелированную структуру (рис. 3).
Электроны, накопленные в фазе ассоциированной воды, поступают на водный матрикс митохондрий, что обеспечивает увеличение их энергетической функции (нелокальная активация синтеза АТФ АТФ-синтазой [5]). При этом дополнительно в водной фазе клеток происходит наработка пероксидных ассоциатов, выполняющих регуляторные, транспортные и контрольные функции в клеточных структурах [5, 9].
Поступление электронов в организм восстанавливает нарушения в структурно-физическом состоянии внутриклеточной фазы ассоциированной воды, ответственной за системный гомеостаз клетки, включая колебательную активность ферментов, мембран, органелл клеток и систем организма. При этом интенсифицируется внутриклеточный везикулярный транспорт метаболитов и гормональных регуляторов, нормализуется баланс экспрессии гормональных регуляторов, восстанавливается клеточный цикл и нормальный уровень апоптоза клеток [9].
Растворы препарата «гуминовый концентрат» являются высокоактивными электрон-донорными средами, обеспечивающими эффективный перенос электронной активности в организм человека. Их абсолютная активность определяется уровнем концентрации нарабатываемых пероксидных анион-радикалов в диапазоне от 10 до 20 мкг/л, что обеспечивает поддержание электрической неравновесности мембран и органелл клеток и сопровождается активизацией энергетической системы клетки (системы окислительного фосфорилирования и АТФ-продуцирующую способность АТФ-синтазы митохондрий клеток), а также увеличивает каталитическое действие клеточных ферментов и ко-ферментов, восстанавливает активность электрон-транспортных цепей гомеостаза клеток, усиливает антиоксидантную активность и резервы адаптации клеточного иммунитета [11].
Исходя из предложенного механизма действия препарата «гуминовый концентрат», данное средство относится к препаратам системного гомеостатического действия, оказывающим регуляторное и энергетическое действие на клеточные структуры организма. Эта способность препарата определяется его нелокальным сопряжением с электрон-донорными иловыми отложениями, обеспечивающими поставку электронов в фазу ассоциированной воды в процессе разведения препарата водой, с последующим переносом заряда на мембраны клеточных структур организма при принятии водного раствора «гуминовый концентрат» in vivo.
Установлено, что перенос электронов от донора к акцептору в системе «грунт – фаза ассоциированной воды – мембраны» происходит во времени в знакопеременных направлениях, что необходимо учитывать при лечебном, бальнеологическом и профилактическом использовании препарата.
В целом препарат «гуминовый концентрат» представляет собой высокоактивную электрон-донорную среду, обеспечивающую поддержание электронной неравновесности мембран и органелл клеток, а также осуществляющую активизацию энергетической системы клеток, регуляцию их метаболической активности (включая регуляторные опероны ДНК) и транспортные функции в системах лиганд-рецепторного взаимодействия и эндосомальных циклов.
Источник