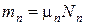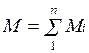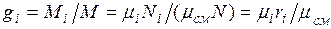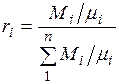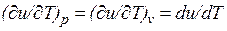ЛЕКЦИЯ 3. Способы задания состава смеси
Способы задания состава смеси. Соотношения между ними
Смеси идеальных газов. Закон Дальтона
В ТТД чистым веществом наз. вещество, все молекулы которого одинаковы. Смесь, состоящая из нескольких чистых веществ наз. раствором. Чистыми веществами явл., например, вода, этиловый спирт, азот, аммиак и т.п. Чистые вещества, составляющие смесь, наз. компонентами.
При рассмотрении смесей газов исходят из того, что смесь идеальных газов, не вступающих в химическое взаимодействие друг с другом, так же явл. идеальным газом и подчиняется таким же законам. При этом каждый газ, входящий в состав газовой смеси, ведет себя так, как будто он один при данной температуре Т занимает весь объём смеси, т.е. равномерно распространяется по всему объёму смеси и оказывает на стенки сосуда своё давление, наз. парциальным.
В 1801г. английский учёный Дальтон экспериментально установил связь между парци- альными давлениями отдельных газов и давлением смеси. При постоянной температуре полное давление смеси нескольких газов равно сумме их парциальных давлений:

где pі— парциальное давление i-го газа; n-количество газов, составляющих газовую смесь.
Газовая смесь может быть задана массовыми, объёмными и мольными долями.
Газовая смесь, заданная массовым составом, характеризуется массовыми долями. Массовой долей компонента gi наз. отношение массы отдельного компонента mi, входящего в смесь, к массе всей смеси Мсм, т.е.
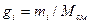
Очевидно, что масса газовой смеси равна сумме масс всех входящих в неё газов:

Определим сумму массовых долей отдельных газов:
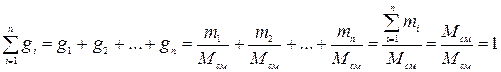
Массовые доли часто задаются в процентах (%).
Газовая смесь, заданная объёмным составом, характеризуется объемными долями (ri). Объёмная доля каждого газа выражается отношением приведенного объёма газа Vi к полному объёму смеси Vсм.
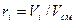
Приведенным Vi наз. объём, который занимал бы компонент газа, если бы его давление рi и температура Тi равнялись давлению рсм и температуре Тсм.
Парциальный объём каждого газа определяется по закону Бойля-Мариотта. При T=const.=Tсм

Из уравнений (2.26) имеем: 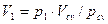
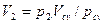
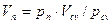
Сложив отдельно левые и правые части уравнений (2.27), получим:

По закону Дальтона 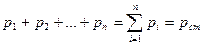
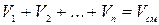
составляющих смесь, равна объёму смеси газов (закон Амала).
Сумма объёмных долей газов, составляющих смесь, равна единице
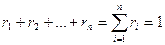
Объёмные доли часто задаются в процентах (%).
Газовая смесь, заданная мольным составом, характеризуется мольными долями. Мольной долей 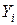
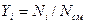
Вполне очевидно, что сумма молей всех газов, составляющих смесь, равна общему числу молей газовой смеси, т.е. 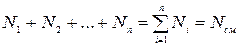
Сумма мольных долей смеси газов равна единице: 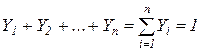
Если известен массовый состав смеси, то по нему можно найти её мольный состав. Массы отдельных газов mi и полную массу смеси Мсм можно выразить через число молей следующем образом: 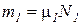
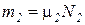
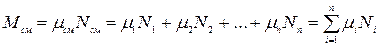
2.8. Теплоёмкость. Массовая, объёмная и молярная теплоемкости.
Теплоемкости при постоянных объёме и давлении
Теплоёмкостью наз. количество теплоты, необходимое для повышения температуры тела на один градус. Теплоёмкость не является постоянной величиной и в общем случае изменяется с изменением температуры и давления. Теплоёмкость единицы количества вещества наз. удельной теплоёмкостью. Удельная теплоёмкость тела зависит от химического состава, параметров состояния рабочего тела, а также от вида процесса, в котором телу сообщается
теплота, поскольку теплота есть функция процесса. Размерность удельной теплоёмкости:
Дж/(кг(м 3 , (моль))) К).
В ТТД различают удельные массовую с, (Дж/(кг К)), объемную с’ , (Дж/(м 3 К)) и мольную сµ (Дж/(моль К)) теплоёмкости.
Зависимости между удельными теплоёмкостями устанавливаются из следующих выражений:
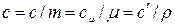
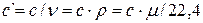
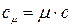
Различают истинную и среднюю теплоёмкости.
Истинной теплоёмкостьюназ. производная от количества теплоты, подведённой к телу, по температуре этого тела и определяется выражением:
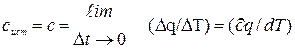
То есть истинная теплоёмкость тела – это его теплоёмкость при данной температуре.
Средней теплоёмкостью наз. теплоёмкость в интервале температур Т2 – Т1, она обозначается Сm. При уменьшении разности температур средняя теплоёмкость приближается к истинной.
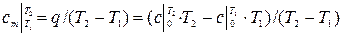
Удельной изохорной теплоемкостью 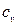
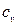
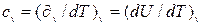
Удельной изобарной теплоемкостью 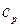
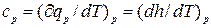
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Смеси идеальных газов



ЛЕКЦИЯ 2
Все зависимости, полученные выше для идеальных газов, справедливы и для их смесей, если в них подставлять газовую постоянную, молекулярную массу и теплоемкость смеси.
Закон Дальтона.В инженерной практике часто приходится иметь дело с газообразными веществами, близкими по свойствам к идеальным газам и представляющими собой механическую смесь отдельных компонентов различных газов, химически не реагирующих между собой. Это так называемые газовые смеси. В качестве примера можно назвать продукты сгорания топлива в двигателях внутреннего сгорания, топках печей и паровых котлов, влажный воздух в сушильных установках и т. п.
Основным законом, определяющим поведение газовой смеси, является закон Дальтона: полное давление смеси идеальных газов равно сумме парциальных давлений всех входящих в нее компонентов:
Парциальное давление pi — давление, которое имел бы газ, если бы он один при той же температуре занимал весь объем смеси.
Способы задания смеси.Состав газовой смеси может быть задан массовыми, объемными или мольными долями.
Массовой долей называется отношение массы отдельного компонента Мi, к массе смеси М:
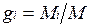
Очевидно, что 
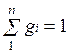
Массовые доли часто задаются в процентах. Например, для сухого воздуха 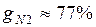
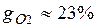
Объемная доля представляет собой отношение приведенного объема газа V, к полному объему смеси V: 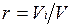
Приведенным называется объем, который занимал бы компонент газа, если бы его давление и температура равнялись давлению и температуре смеси.
Для вычисления приведенного объема запишем два уравнения состояния i-го компонента:
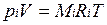
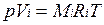
Первое уравнение относится к состоянию компонента газа в Смеси, когда он имеет парциальное давление pi и занимает полный объем смеси, а второе уравнение — к приведенному состоянию, когда давление и температура компонента равны, как и для смеси, р и Т. Из уравнений следует, что
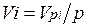
Просуммировав соотношение (2.2) для всех компонентов смеси, получим с учетом закона Дальтона 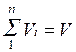
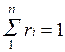
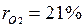
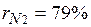
Иногда бывает удобнее задать состав смеси мольными долями. Мольной долей называется отношение количества молей Ni рассматриваемого компонента к общему количеству молей смеси N.
Пусть газовая смесь состоит из N1 молей первого компонента, N2 молей второго компонента и т. д. Число молей смеси 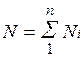
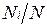
В соответствии с законом Авогадро объемы моля любого газа при одинаковых р и Т, в частности при температуре и давлении смеси, в идеально газовом состоянии одинаковы. Поэтому приведенный объем любого компонента может быть вычислен как произведение объема моля 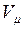
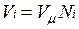
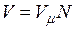
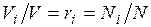
Газовая постоянная смеси газов. Просуммировавуравнения (2.1) для всех компонентов смеси, получим 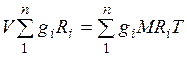
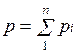
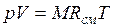
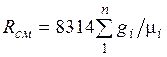
Из уравнения (2.3) следует, что смесь идеальных газов также подчиняется уравнению Клапейрона. Поскольку 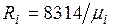
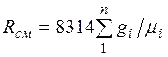
Кажущаяся молекулярная масса смеси. Выразим формально газовую постоянную смеси R, введя кажущуюся окулярную массу смеси 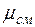
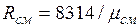
Сравнивая правые части соотношений (2.5) и (2.6), найдем
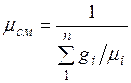
Изопределения массовых долей следует, что
Просуммировав это соотношение для всех компонентов и учитывая, что 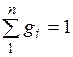
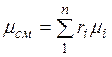
Соотношение между объемными и массовыми долями. Учитывая (2.7), получаем 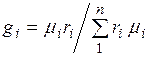
Поскольку 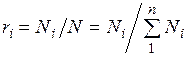
Разделив числитель и знаменатель этой формулы на массу смеси М, получим
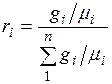
Аналитическое выражение первого закона термодинамики
Первый закон термодинамики представляет собой частный случай всеобщего закона сохранения и превращения энергии применительно к тепловым явлениям. В соответствии с уравнением Эйнштейна 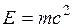

Закон сохранения и превращения энергии является фундаментальным законом природы, который получен на основе обобщения огромного количества экспериментальных данных и применим ко всем явлениям природы. Он утверждает, что энергия не исчезает и не возникает вновь, она лишь переходит из одной формы в другую, причем убыль энергии одного вида дает эквивалентное количество энергии другого вида.
В числе первых ученых, утверждавших принцип сохранения материи и энергии, был наш соотечественник М. В. Ломоносов (1711 — 1765 гг.).
Пусть некоторому рабочему телу с объемом V и массой М, имеющему температуру Т и давление р, сообщается извне бесконечно малое количество теплоты 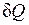
Повышение температуры тела свидетельствует об увеличении кинетической энергии его частиц. Увеличение объема тела приводит к изменению потенциальной энергии частиц. В результате внутренняя энергия тела увеличивается на dU. Поскольку рабочее тело окружено средой, которая оказывает на него давление, то при расширении оно производит механическую работу 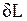
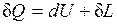
т. е. теплота, сообщаемая системе, идет на приращение ее внутренней энергии и на совершение внешней работы.
Полученное уравнение является математическим выражением первого закона термодинамики. Каждый из трех членов этого соотношения может быть положительным, отрицательным или равным нулю. Рассмотрим некоторые частные случаи.
1. 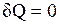
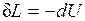
Следовательно, работа расширения, совершаемая системой в адиабатном процессе, равна уменьшению внутренней энергии данной системы. При адиабатном сжатии рабочего тела затрачиваемая извне работа целиком идет на увеличение внутренней энергии системы.
2. 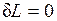
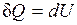
т. е. количество теплоты, подведенное к системе при постоянном объеме, равно увеличению внутренней энергии данной системы.
3. dU=0 – внутренняя энергия системы не изменяется и
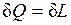
т.е. сообщаемая системе теплота превращается в эквивалентную ей внешнюю работу.
Для системы, содержащей 1 кг рабочего тела
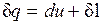
Проинтегрировав уравнения (2.8) и (2.9) для некоторого процесса, получим выражение первого закона термодинамики в интегральной форме:
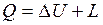
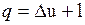
Внутренняя энергия системы включает в себя:
кинетическую энергию поступательного, вращательного и колебательного движения частиц;
потенциальную энергию взаимодействия частиц;
энергию электронных оболочек атомов;
В большинстве теплоэнергетических процессов две последние составляющие остаются неизменными. Поэтому в дальнейшем под внутренней энергией будем понимать энергию хаотического движения молекул и атомов, включающую энергию поступательного, вращательного и колебательного движений как молекулярного, так и внутримолекулярного, а также потенциальную энергию сил взаимодействия между молекулами.
Кинетическая энергия молекул является функцией температуры, значение потенциальной энергии зависит от среднего расстояния между молекулами и, следовательно, от занимаемого газом объема V, т. е. является функцией V. Поэтому внутренняя энергия U есть функция состояния тела.
Для сложной системы она определяется суммой энергий отдельных частей, т. е. обладает свойством аддитивности. Величина и=U/М, называемая удельной внутренней энергией (Дж/кг), представляет собой внутреннюю энергию единицы массы вещества.
В дальнейшем для краткости будем называть величину и просто внутренней энергией. Поскольку внутренняя энергия есть функция состояния тела, то она может быть представлена в виде функции двух любых независимых параметров, определяющих это состояние:
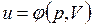
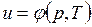
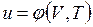
Ее изменение в термодинамическом процессе 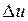
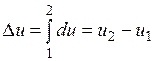
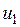
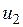
Внутренняя энергия идеального газа, в котором отсутствуют силы взаимодействия между молекулами, не зависит от объема газа или давления 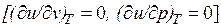
Для задач технической термодинамики важно не абсолютное значение внутренней энергии, а ее изменение в различных термодинамических процессах. Поэтому начало отсчета внутренней энергии может быть выбрано произвольно. Например, в соответствии с международным соглашением для воды за нуль принимается значение внутренней энергии при температуре 0,01 °С и давление 610,8 Па, а для идеальных газов — при 0 °С вне зависимости от давления.
Источник