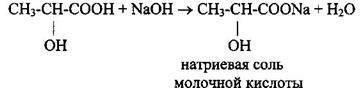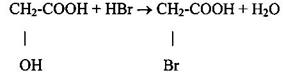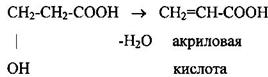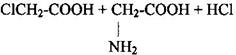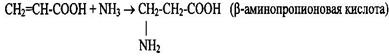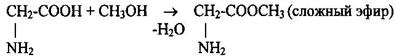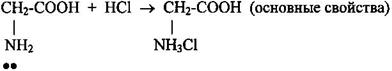Способ получения @ -галогензамещенных адипиновых кислот
Сущность изобретения: Продукт — ахлорзамещенная адипиновая кислота, БФ СеНдОдС ; т. пл. 93°С пр. Продукт — а -бромзамещенная адипиновая кислота БФ СбНэ04Вг;т.пл. 122-123°С. Продукт -а-иодзамещенная адипиновая кислота БФ СбН9041.т. пл. 129-130°С, пр. Реагент 1:1,2- циклогександион. Реагент 2: галогенид двухвалентной меди. Реагент 3: смесь галогенида двухвалентной меди и галогенида щелочного металла. Реагент 4: 30%-ный Н202. Условия реакции: при 0 — 30°С молярное соотношение циклогександион : галогенид двухвалентной меди: Н202 1 : 1.2-2,0 : :1,2-2,0 или молярное соотношение 1,2- циклогександион : галогенид двухвалентной меди : галогенид щелочного металла : Н202 — 1 : 0.1-0,2 : 1.2-2.0 : 1,2-2,0. 1 табл.
РЕСПУБЛИК (s))s С 07 С 51/285, 55/32
ПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (21) 4859212/04 (22) 22.06.90 (46) 23.05.92. Бюл. N. 19 (71) Институт органической химии им. Н.Д.Зелинского (72) Г.И.Никишин, А,А,Маэурчик и Е,К.Старостин (53) 547.547.29.07 (088,8) (56) Гауптман 3., Графе Ю., Ремане Х. Органическая химия, — Иэд-во. Химия, М., 1979, с. 439.
Gal W., Оау-Lussac С, Lieblgs Annalen
der Chemic 155, р. 250.
Nasakl N., Terno L., MasaJasu Sh., Hiroshi G., Japan KokaL 7399115, кл. 16864, опублик., 1973, С.А. 80: С, 95273. (54) СПОСОБ ПОЛУЧЕНИЯ а-ГАЛОГЕНЗАМЕЩЕННЫХ АДИПИНОВЫХ КИСЛОТ
Изобретение относится к органической химии, и касается, в частности, способа получения й-хлор,- а-бром- и й-иодадипиновых кислот. Эти кислоты находят применение в тонком органическом синтезе, в производстве гербицидов, в синтезе Р-оксикислот по реакции Реформатского.
Известен способ получения .а-брома дипиновой кислоты прямым бромированием адипиновой кислоты г ри +160 С. Выход а -бромадипиновой кислоты составляет 5%, Наряду с а -бромэамещенной адипиновой кислотой образуются также ир -бромэамещенные продукты, что в значительной степени затрудняет выделение целевого продукта.
Наиболее близким по технической сущности и достигаемому результату является. Ы 1735268 А1 (57) Сущность изобретения: Продукт — ахлорзамещенная адипиновая кислота, БФ
С6Н904С1; т. Пл. 93 С пр. Продукт — а -бромэамещенная адипиновая кислота БФ
С6Н904Вг; т.пл. 122-123 С. Продукт — а -иодзамещенная адипиновая кислота БФ
C6Hg04L т. пл. 129-130 С, пр. Реагент 1: 1,2циклогександион. Реагент 2: галогенид двухвалентной меди. Реагент 3: смесь галогенида двухвалентной меди и галогенида щелочного металла. Реагент 4; 30 -ный
Н202, Условия реакции: при 0 — 30 С молярное соотношение циклогександион; галогенид двухвалентной меди, Hz0z = 1: 1,2-2,0:
:1,2-2,0 или молярное соотношение 1,2циклогександион: галогенид двухвалентной меди: галогенид щелочного металла:
Н202 = 1: 0,1-0,2: 1,2-2.0: 1,2-2.0. 1 табл. способ получения а-бром или а-хлор адипиновых кислот путем окисления 2-бромили 2-хлорциклогексанона азотной кислотой в присутствии ЙН4ЧОз и Май02 при
+38 С при перемешивании в течение 15 ч, Получают а-бромадипиновую кислоту с выходом «50, а-Иодциклогексанон при прямом иодировании ввиду большой неустойчивости выделен не был и в связи с этим а-иодадипиноновая кислота не получена.
Недостатками данного способа являются относительно невысокий выход целевого продукта, а также образование больших количеств сточных вод кислого характера и выброс в атмосферу вредных нитрозных газов, двухстадий ность процесса.
Цель изобретения — повышение выхода целевого продукта и экологической без1735268 опасности окружающей среды, а также упрощение процесса, Поставленная цель достигается спосо6оМ получения а-галогензамещенных адипиновых кислот HOOCCHXCH2CH2CHzCOOH (X = Cl, Br, 1) путем обработки 1,2-циклогександиона галогенидом двухвалентной меди или смесью галогенида двухвалентной меди с галогенидом щелочного металла и 30 ным раствором перекиси водорода при молярном соотношении 1,2-циклогександион: галогенид двухвалентной меди: Hz02, равном 1; 1,2-2,0: 1,2-2,0, либо при молярном соотношении 1,2-циклогександион: галогенид двухвалентной меди: галогенид щелочного металла: Н202, равном 1: 0,1-0,2:
:1,2-2,0: 1,2-2,0, при температуре Π— +30 С.
Выход целевого продукта 78-85 .
Отличительными признаками процесса являются: использование в качестве исходного 1,2-циклогександиона и обработка его галогенидом двухвалентной меди и галогенидом щелочного металла с добавлением к реакционной массе 307;-ного раствора
H2Oz в качестве окислителя и проведение процесса при молярном соотношении 1.,2циклогександион: галогенид двухвалентной меди: Н202, равном 1: 1,2-2,0: 1,2-2,0, либо при молярном соотношении 1,2-циклогександион: галогенид двухвалентной меди:
: галогенид щелочного металла: H20z, равном 1: 0,1-0,2: 1,2-2,0: 1,2-2,0, при температуре 0 — +30 С, что позволяет упростить процесс, улучшить экологию и повысить выход целевого продукта.
Пример 1. К 11,2 r (0,1 моль) 1,2-циклогександиона, растворенных в 150 мл воды, добавляют 25,5 r СиО2 х 2 Н20 и к этому раствору при перемешивэнии добавляют в течение 45 мин 18,0 мл. 307ь-ного раствора
Н20, поддерживая температуру +15 C охлаждением водяной баней, После этого раствор подкисляют 2NHz$04 до рН 2 и перемешивают еще 30 мин, затем экстрагируют эфиром 3 х 100 мл и эфирный экстракт обрабатывают насыщенным раствором йэ2СОз. Водный слой отделяют, подкисляют2й Н2$04до рН 2 и экстрагируют эфиром
После удаления эфира выделяют l4,05 r а -хлорадипиновой кислоты (78 ). После перекристаллизации из воды т. пл. +93 C.
Найдено, : С 40,22; Н 5,02; О — 19,62
Вычислено;7ь: С 39,91; Н 5,02; Cl 19,63
По данным ГЖХ чистота продукта98 .
Пример 2. К 11,2 r (0,1 моль) 1,2-циклогександиона, растворенных в 150 мл воды, добавляют 36,0 г СиВг2 х Н20 и к этому раствору при перемешивании в течение
45 мин добавляют 18,0 мл 30 -ного раствора HzOz, поддерживая температуру +15 С охлаждением водяной баней. После этого раствор подкисляют 2N Hz$04 до рН 2 и
5 перемешивают еще.30 мин, затем экстрагируют эфиром 3 х 100 мл и эфирный экстракт обрабатывают насыщенным раствором
Ма2СОз. Водный слой отделяют подкисляют 2N H2S04 до рН 2 и экстрагируют эфи10 ром 3 х 100 мл.
После удаления эфира выделяют 17,85 г а -бромадипиновой кислоты (80 ), После перекристаллизации из воды т. пл, +122123 С.
15 Найдено,g: С 32,03; Н 4,02; Вг 35,71
Вычислено,7ь: С 31,95; Н 3,96; Br 35,93.
По данным ГЖХ чистота продукта—
Пример 3. К 11,2 г (О;1 моль) 1,2-цик20 логександиона, растворенных в 150 мл воды, добавляют 47,8 r Cul и к этому раствору при перемешивании в течение 45 мин добавляют 18,0 мл 30 -ного раствора Н202, поддерживая температуру+15 С охлажде25 нием водяной баней. После этого раствор подкисляют2NHz$04дорН 2и перемешивают еще 30 мин, затем экстрагируют эфи- . ром 3 х 100 мл и эфирный экстракт обрабатывают насыщенным раствором
30 йа2СОз. Водный слой отделяют, подкисляют 2N H2$04 до рН 2 и экстрагируют эфиром
3х 100 мл, После удаления эфира выделяют 21,4 г а -иодадипиновой кислоты (797), После
35 перекристаллизации из воды т, пл, +129130оС
Найдено,7ь: С 26,32; Н 3,41; J 47,11
Вычислено,ф,: С 26,46; Н 3,32; J 46,70
flo данным ГЖХ чистота продукта
Примеры 4-23 проводят по методике примеров 1-3.
Сравнительные примеры 13-16, 19 и 23 свидетельствуют о том, что примеры 1-12, 45 17, 18 и 20-22 являются оптимальными условиями синтеза а-галогензамещенных адипиновых кислот.
Увеличение избытка Н202 более двукратного является нецелесообразным, по50 скольку приводит к уменьшению выхода целевых продуктов (примеры 13 и 14).
При этом повышение температуры свыше +30 С также нецелесообразно (пример
15), так как приводит к уменьшению выхода
55 целевого продукта.
Нецелесообразно проведение реакции и при температурах ниже О С (пример 16). тэк как наблюдается уменьшение растворимости веществ, выпадение их в осадок и, как
Источник
Способы получения галогензамещённых кислот
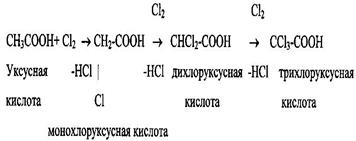
1 Замещение водорода в кислотах жирного ряда на галоген.
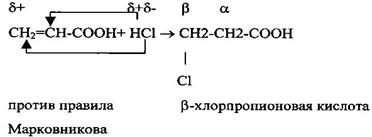
2 Присоединение галогенов или галогеноводорода к непредельным кислотам.
Химические свойства
Атомы галогена и карбоксильная группа в галогензамещённых кислотах обладают в основном обычными, характерными для этих функций свойствами.
Так, галоген способен к реакциям замещения, карбоксильная группа проявляет кислотные свойства.
 |
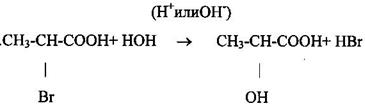 |
| α-бромпропионовая α-гидроксипропионовая кислота кислота |
В этих реакциях участвовал галоген.
3 Образование солей и сложных эфиров с участием карбоксильной группы.
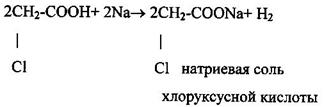 |
 |
Гидроксикислоты
Гидроксикислоты – производные углеводородов, в молекуле которых присутствуют две функциональные группы — гидроксильная и карбоксильная.
Способы получения гидроксикислот
1 Гидролиз галогензамещённых кислот:
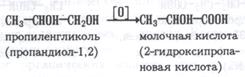
2 Окисление гликолей
3 Получение из альдегидов и кетонов через циангидрины
Химические свойства
1 Образование солей и сложных эфиров (кислотные свойства)
2 Реакции с участием гидроксигруппы (спиртовые свойства)
3 Дегидратация гидроксикислот
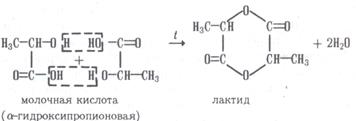
При дегидратации α-гидроксикислот образуется циклический продукт – лактид:
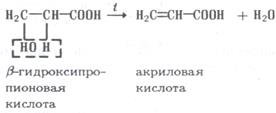
Дегидратация β-гидроксикислот приводит к образованию непредельных кислот:
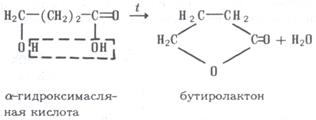
При дегидратации γ- и δ-гидроксикислот возникают сложные эфиры – лактоны:
Аминокислоты
Аминокислоты – соединения, содержащие аминогруппу (-NН2) и карбоксильную группу (-СООН). Наибольшее значение имеют α-аминокислоты.
Способы получения
1 Замена галогена в галогензамещённых кислотах на аминогруппу при действии избытка аммиака.
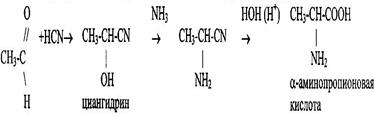
2 Из альдегидов и кетонов действием синильной кислоты и аммиака.
3 Присоединение аммиака к непредельным кислотам
Химические свойства
Аминокислоты проявляют в реакциях амфотерные свойства — аминогруппа со свойствами основания, карбоксильная группа с кислотными свойствами.
1 Образование солей и сложных эфиров (кислотные свойства)
2 Реакции по аминогруппе:
Углеводы
Углеводы— это природные органические соединения, состав которых выражается общей формулой Сn(Н2О)m, (n, m›3).
Класс углеводов объединяет:
Моносахариды – С6Н12О6 — глюкоза, фруктоза
Строение моносахаридов мы рассмотрим на примере глюкозы.
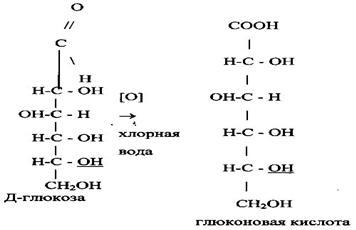
Глюкоза — альдегидоспирт (доказано экспериментально).
D (+) — глюкоза (альдегидная форма)
У D — глюкозы гидроксигруппа у самого нижнего асимметричного атома стоит справа, у L — глюкозы — она стоит слева.
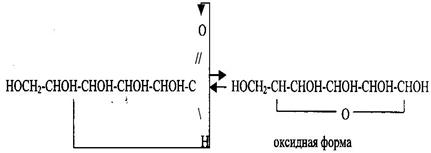
Кроме альдегидной формы глюкоза может иметь циклическую (оксидную) форму. Это таутомерная модификация, находящаяся в равновесии с альдегидной формой:
Таутомерия
Оксидная форма может иметь два циклических изомера, называемых α- и β- формами:
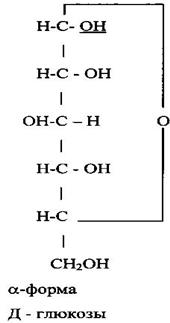 |  |
Гидроксигруппа у С-1, возникшая при переходе в циклическую форму, отличается от остальных гидроксигрупп.
При действии метилового спирта и хлороводорода образуется два производных циклической формы. Такие соединения называют гликозидами, а в случае глюкозы — глюкозидами (глюкос — сладкий).
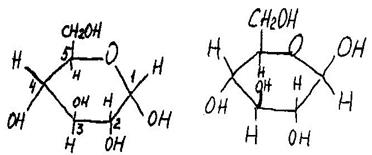
Циклические, формулы, записанные выше, недостаточно наглядно передают пространственное строение молекулы. Поэтому используется более удобное написание этих формул:
α – D – глюкоза β – D – глюкоза
Химические свойства
Для глюкозы характерны реакции присоединения синильной кислоты, реакции замещения с гидразином, фенилгидразином.
3 Алкилирование приводит к образованию простых эфиров, которые являются производными циклических форм. Легче всего реагирует гликозидный гидроксил:
α- D – глюкоза глюкозид
4 Спиртовое брожение:
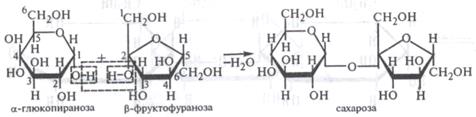
Дисахариды
В молекулы дисахаридов входят циклические формы моносахаридов. Известны два типа дисахаридов, различие между которыми зависит от того, участвуют ли в создании связи через кислород оба гликозидных гидроксила (стоят у С-1) — невосстанавливающиеся дисахариды (сахароза) – а или один гликозидный и один спйртовой (4) – восстанавливающие дисахариды (целлобиоза, мальтоза, лактоза) – б.
а)
б)
α-D – глюкоза мальтоза Химические свойства невосстанавливающих дисахаридов определяют гидроксильные группы, а восстанавливающих — альдегидная или кетонная группа и гидроксилы. Поэтому восстанавливающие дисахариды вступают в реакции, характерные для моносахаридов.
Дисахариды легко гидролизуются при нагревании вводными растворами минеральных кислот или при действии ферментов, что приводит к образованию моносахаридов.
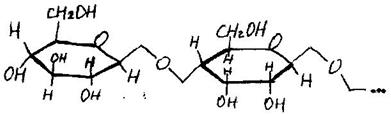
Полисахариды
Молекулы полисахаридов можно рассматривать как продукты конденсации большого числа молекул моносахаридов друг с другом. Состав (СбН10О5)n. Являются продуктами фотосинтеза.
Крахмал — полисахарид, построенный из нескольких тысяч остатков α — глюкозы.
Целлюлоза (клетчатка) — имеет линейное строение, но состоит из остатков β-глюкозы.
При гидролизе крахмал и целлюлоза образуют глюкозу (конечный продукт). При этом гидролиз целлюлозы протекает при более жестких условиях
|
Несмотря на химическую инертность, целлюлоза под воздействием некоторых химически активных реагентов образует многие производные. Например,
|
На основе нитратов целлюлозы получают различные пороха, а также служат для синтеза нитролаков, нитрокраски и эмалей.
Ацетаты целлюлозы используют в производстве ацетатного волокна, а также для получения пластмасс, негорючей фото- и кинопленки, специальных лаков.
Источник