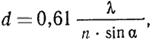Фиксация мазка физическим способом
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ АГЕНСТВО ПО ОБРАЗОВАНИЮ
ДАГЕСТАНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Предметом изучения цитологии, гистологии и эмбриологии являются клеточно-тканевые структуры организмов на микроскопическом уровне, а предметом изучения – микроскопический препарат. Поэтому для успешного освоения этих наук необходимо владеть гистологической техникой – приемами и методами изготовления микроскопических препаратов и способами их изучения. В настоящем руководстве изложены основные сведения по технике гистологических исследований, оно знакомит студентов с правилами работы и методами наблюдения под микроскопом, методикой приготовления препаратов. Особое внимание уделено методам окрашивания различных клеточно-тканевых структур и гистохимическим исследованиям. Методики применимы на растительных и животных объектах.
Методические указания рекомендованы для студентов, специализирующихся по кафедре физиологии человека и животных, могут быть использованы на лабораторных занятиях по цитологии, гистологии и эмбриологии, большом практикуме, при выполнении курсовых и дипломных работ.
Автор: Газимагомедова И.К. – доц. каф. зоологии и физиологии, канд. биол. наук
Приготовление постоянного микротомного препарата Взятие и фиксация материала …………………………….
Уплотнение (заливка в парафин) ………………………….
Окрашивание и заключение в бальзам ………………….
Методы окрашивания гистологических препаратов …
Методы окраски клеток и неклеточных структур соединительной ткани ……………………………………..
Выявление элементов нервной системы
Гистохимические методы исследования .
Приготовления препаратов давленных объектов. Методы изучения митоза и мейоза ………………………
1. Световая Микроскопия
1.1. Устройство микроскопа
Световой микроскоп является основным прибором используемым студентами на занятиях. Он имеет следующие основные характеристики: источник излучения – свет; максимально-полезное увеличение — х2000-2500; объект – живой и неживой; для окрашивания используют цветные красители; даёт перевернутое, цветное изображение объекта.
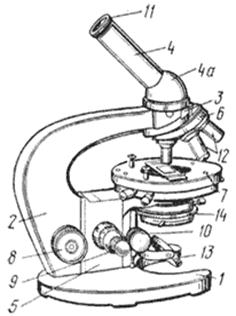
В микроскопе различают оптическую (объектив, окуляр), осветительную (источник света, зеркало, конденсор и диафрагма) и механическую (штатив, предметный столик, колонка с макро- и микровинтами, тубус) части (рис. 1).
Рис.1. Световой микроскоп.
1 — основание штатива; 2 — колонка штатива; 3 — головка тубусодержателя; 4 — наклонный тубус; 4а — расширенная часть наклонного тубуса; 5 — коробка микромеханизма; 6 — револьверная система; 7 — столик микроскопа; 8 — макрометрический винт; 9- микрометрический винт; 10 — винт конденсора; 11 — окуляр; 12 — объективы; 13 — зеркало; 14 — конденсор с ирисовой диафрагмой.
Оптическая часть . Главная оптическая часть микроскопа — система линз объектива — обеспечивает увеличение изображения. Обычные увеличения объектива: 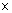
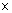
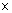
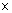
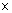
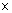
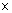
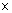
Полное увеличение микроскопа оценивают как произведение увеличений объектива и окуляра, например, при объективе 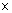
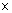
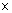
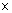
Основной характеристикой микроскопа как оптической системы является разрешающая способность . Изображения, даваемые объективом, можно увеличить во много раз, применяя сильный окуляр или, например, путем проекции на экран (до 10 5 раз).
Разрешающая способность объектива, т.е. минимальное расстояние между двумя видимыми точками (минимальный размер объекта):
где: λ – длина волны света, используемого для освещения объекта; n – коэффициент преломления среды (воздух или масло); α – угол между оптической осью объектива и наиболее отклоняющимся лучом, попадающим в объектив (максимально 90°); n ∙ sin α – апертура линз.
Разрешение микроскопа зависит от длины волны – чем она меньше, тем меньшего размера деталь мы можем увидеть, – и от апертуры (апертура – функция светособирающей способности линз, для сухих линз равна 1, а для иммерсионных линз достигает 1,4), – чем она выше, тем выше разрешение. Обычно в световых микроскопах используются источники освещения в видимой области спектра (400 – 700 нм), поэтому максимальное разрешение микроскопа в этом случае может быть не выше 200 — 350 нм (0,2 – 0,35 мкм).
Если использовать ультрафиолетовый свет (260 – 280 нм), то можно повысить разрешение до 130-140 нм (0,13 – 0,14 мкм). Это будет пределом теоретического разрешения светового микроскопа, определяемым волновой природой света. Таким образом, все, что может дать световой микроскоп как вспомогательный прибор к нашему глазу – это повысить разрешающую способность его примерно в 1000 – 2500 раз. Это и есть “полезное” увеличение микроскопа, выше которого мы будем только увеличивать контуры изображения, не открывая в нем новых деталей. Следовательно, при использовании видимой области света 0,2–0,3 мкм является конечным пределом разрешения светового микроскопа (минимальное расстояние на котором различимы два объекта).
Но все же в световом микроскопе можно видеть частицы меньшей величины, чем 0,2 мкм. Это метод “темного поля” , или, как его называли раньше, метод “ультрамикроскопии”. Суть его в том, что, подобно пылинкам в луче света (эффект Тиндаля), в клетке при боковом освещении светятся мельчайшие частицы (меньше 0,2 мкм), отраженный свет от которых попадает в объектив микроскопа (клетка выглядит как освещенный объект на темном поле).
Осветительная часть. Источник света может быть встроен в микроскоп, а может находиться и вне микроскопа (пример — обычная настольная лампа).
Зеркало собирает лучи от источника света и направляет их на препарат снизу. При искусственном освещении используется вогнутая поверхность зеркала, а при дневном – плоская.
Конденсор состоит из линз, которые фокусируют лучи света на препарате. Поднимая и опуская конденсор (с помощью винта), можно настраивать фокусировку лучей. При подъеме конденсора попадающие на препарат лучи рассеиваются, при опускании концентрируются на препарате, но на более ограниченном участке. Обычно работают при конденсоре, поднятом до уровня столика.
Диафрагма — это система непрозрачных пластинок с отверстием посередине, которая вмонтирована в конденсор и ограничивает световой поток, падающий на препарат. При использовании объективов с большим увеличением отверстие диафрагмы следует уменьшить — для ослабления сферической аберрации.
Механическая часть. Макро- и микровинты колонки поднимают и опускают тубус для фокусировки изображения объекта на сетчатке глаза наблюдателя. Макровинт используется при работе на малом увеличении, а микровинт — на большом. Предметный столик может перемещаться в горизонтальной плоскости, что позволяет менять участки препарата, попадающие в поле зрения.
В итоге, световые лучи проходят следующий путь: источник света → зеркало → конденсор → диафрагма → препарат → объектив → тубус → окуляр. Т.е. микроскопия ведётся в проходящем свете, для чего препарат должен быть достаточно тонким.
1.2. Техника микроскопирования
Первоначально нужно установить правильное освещение. Поставить микроскоп от края стола на расстояние не менее 5 см колонкой к наблюдателю, зеркалом к источнику света. Объектив малого увеличения установить против отверстия в столике на расстоянии 1 см , привести конденсор в крайнее верхнее положение. Открыть диафрагму конденсора. Зеркало направить к источнику света вогнутой стороной (при искусственном освещении) или плоской (при рассеянном дневном свете). Смотря левым глазом в окуляр, переворачивать зеркало до получения равномерного освещения поля зрения.
Само изучение препарата начинают с осмотра его глазом, после чего препарат помещают на предметный столик, покровным стеклом вверх, прижимая клеммами, чтобы срез точно лег под объектив. Препарат начинают изучать при малом увеличении, пользуясь макровинтом микроскопа, установить объектив малого увеличения так, чтобы расстояние между его нижней линзой и покровным стеклом было равно около 0,5 — 1 см . Наблюдая в окуляр, медленно вращать макровинтом до получения четкого изображения.
Изучить препарат при малом увеличении.
Перевести препарат на большое увеличение. Для этого сменяют объектив на 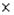
Для изучения очень мелких структур используют иммерсионный объектив ( 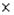
2. Приготовление постоянного микротомного препарата
Клетки и ткани можно изучать в живом состоянии путем изготовления витальных, временных препаратов для однократного изучения, либо убитые — на соответствующе приготовленных постоянных препаратах, которые хранятся длительное время.
По характеру взятого материала различают следующие виды гистологических препаратов: 1) срезы органов (толщиной 5-15 нм), 2) мазки (крови, костного мозга и т.д.),
3) пленки (брюшины, мягкой мозговой оболочки), или тотальные препараты . Чаще всего используются срезы.
Приготовление постоянных гистологических препаратов включает следующие этапы: 1) взятие и фиксация материала; 2) промывка и обезвоживание; 3) уплотнение (заливка в парафин); 4) приготовление срезов; 5) окрашивание; 6) обезвоживание и заключение препаратов в консервирующую среду (рис. 2).
2.1. Взятие и фиксация материала
Необходимое условие при взятии материала – сохранение прижизненной организации тканей. Для этого материал берут «живьем» и быстро убивают, обычно погружая в специальные фиксирующие жидкости, в целях сохранения витальной структуры, т.е. проводят фиксацию.
Рис. 2. Этапы приготовления гистологического препарата для световой микроскопии.
В зависимости от строения органа взятие материала осуществляется по-разному. Из однородных органов (печень, селезенка) кусочек можно вырезать из любого участка. Из неоднородных органов (почка, надпочечник) необходимо так вырезать кусочек, чтобы попали все слои. Величина кусочка зависит от структуры органа, целей исследования и способов дальнейшей обработки. Из соответствующего органа вырезают обычно небольшие кусочки (0,5 x 1 x 1 см ).
Фиксация — сохранение картины тканевой структуры изолированных органов. Задачи фиксации – это убить клетку, остановить активность внутриклеточных ферментов и распад клеточных компонентов, стабилизировать макромолекулы путем их химического сшивания, предотвратить процессы аутолиза (самопереваривания) тканей и их бактериальное загрязнение, а также избежать потери компонентов клетки или появления отсутствующих в живой клетке структур (артефактные структуры). К сожалению, еще не найден такой химический фиксатор, который бы удовлетворял всем этим требованиям. Даже наилучшие способы фиксации вызывают изменения в фиксируемом материале.
Способы фиксации – использование фиксирующих жидкостей, криофиксация (мгновенное замораживание в жидком азоте) и лиофилизация (замораживание с последующим высушиванием в вакууме). При лиофилизации выпадает необходимость проводить обезвоживание и уплотнение материала.
Фиксирующие средства бывают простые и сложные. К первым относятся спирты, ацетон, кислоты, формалин, сулема, пикриновая кислота, тетраоксид осмия. Сложными являются смеси различных веществ, например жидкость Ценкера, жидкость Карнуа, жидкость Буэна и т.д. Так, для лучшей фиксации ядер употребляют хромовые или хромосмиевые смеси, для фиксации цитоплазмы смеси Карнуа или Буэна. Фиксирующие свойства зависят от рН среды, температуры, продолжительности фиксации.
Часто для фиксации клеток используются альдегиды и их смеси с другими веществами. Широкое применение нашел формалин (формол) в виде 5-15% раствора (продажный формалин — это 35-40% водный раствор формальдегида). Формалин быстро проникает в ткань, сохраняет структуру объекта, липиды и жиры в тканях. Менее пригодна фиксация в формалине для ядерных структур. Действие формалина основано на метилировании тканевых белков: при отщеплении воды формалин вступает с тканевыми белками в метильное соединение, образуя метиленовые мостики. Т.е. формалин хорошо связывается с белками, сшивая их с помощью метиленовых мостиков, вызывая их денатурацию. С липидами формальдегид реагирует слабо (за исключением фосфатидилэтаноламина). С углеводами альдегиды не реагируют, их фиксация, сохранность, достигается, по-видимому, за счет стабилизации окружающих белков.
В последнее время, особенно для электронной микроскопии, широко используется глютаровый альдегид, который более эффективно сшивает молекулы и тем самым обладает сильным фиксирующим действием.
В качестве фиксаторов применяют спирты (этанол, метанол), они значительно больше искажают прижизненную структуру — вызывают необратимую денатурацию белков, осаждение нуклеиновых кислот и полисахаридов. Осаждающим действием обладают также сулемовые фиксаторы и фиксаторы с пикриновой кислотой. Фиксаторы, содержащие тетраоксид осмия (OsО4), хорошо сохраняют липиды.
Требования, предъявляемые к фиксируемому материалу : 1) свежесть материала, для нормального протекания жизненных процессов перед фиксацией; 2) небольшие размеры материала — 0,5x1x1 см, для быстрейшего проникновения фиксатора во избежание артефактов. Если материал нежелательно разрезать на части или он обладает плотной кутикулой и т.д., то в нескольких местах делают неглубокие надрезы бритвой или проколы иглой.
Требования, предъявляемые к фиксатору : 1) свежесть; 2) достаточное количество. Объем фиксатора должен в 20-40 раз превышать объем фиксируемого материала, объект со всех сторон должен быть окружен фиксатором. Если часть материала плавает на поверхности фиксатора, то сверху накладывают тонкий слой ваты. Как до, так и после фиксации объект не должен подсыхать на воздухе.
100% или 96% спирт……………………6 частей
Ледяная уксусная кислота…………… 1 часть
Фиксатор готовят перед употреблением. Фиксируют от 30 мин до 3 ч, затем кусочки можно хранить в 70% спирте.
100% или 96% этиловый спирт………. 3 части
Ледяная уксусная кислота ..…………….1 часть
Продолжительность фиксации – 2-12 ч. Иногда в нем хранят материал при 0-3 о С.
Двухромовокислый калий………………2,5 г
Сернокислый натрий…………………….1 г
Дистиллированная вода…………………100 мл
Ледяная уксусная кислота………………5 мл (добавляют перед употреблением)
Фиксируют 1-24 ч. Затем 24 ч промывают в водопроводной воде до обесцвечивания воды. Материал обесцвечивают в 70% спирте, где его можно хранить. Цвет фиксатора – насыщенно красно-бордовый. Как только сулема будет удалена, раствор перестанет обесцвечиваться.
100% или 96% спирт…………………….10 мл
Ледяная уксусная кислота………………2 мл
Формалин 40%. ……………………….2 мл
Фиксируют от 5 мин и более. Фиксатор пригоден для приготовления временных давленых препаратов.
5% формалин: 1 часть 40% формалина + 7 частей дистиллированной воды.
10% формалин: 1 часть 40% формалина + 3 части дистиллированной воды.
20% формалин: 1 часть 40% формалина + 1 часть дистиллированной воды.
Кусочек ткани помещают в 5% формалин на 1 сут. Перенося в 10% формалин не менее чем на 5-6 сут, где их можно сохранять. Перед дальнейшей обработкой – обезвоживанием — материал помещают в 20% формалин на 1 сут. Затем промывают проточной водой 1 сут.
Методика проведения фиксации. Берется чистая стеклянная посуда (пробирки, бюксы или стаканчики) с фиксатором, объем которого в 20-40 раз больше объема материала. На дно посуды кладут гигроскопическую или стеклянную вату для равномерного пропитывания объекта. Материал с помощью пинцета быстро помещается в фиксирующую смесь (фиксатор должен быстро проникать в ткани и не вызывать грубых нарушений тканевых структур) и посуда плотно закрывается. Вместе с материал в пробирку кладется фиксационная этикетка, сделанная из плотной бумаги, размером 1х1 см, на которой простым карандашом отмечаются название изучаемого материала, фиксатора и дата фиксации.
Если ткань богата водой или кровью, фиксатор следует дважды сменить.
После фиксации образцы промывают проточной водой (в некоторых случаях спиртом) от 1 до 3 ч, иногда дольше. Промывкой материала удаляется излишнее количество фиксатора. В зависимости от способа фиксации существуют разные способы промывки. После фиксации в смеси с пикриновой кислотой промывка производится 70-80% спиртом. При фиксации в смесях, содержащих сулему, трихлоруксусную кислоту, используют 90-96% спирт. При формалиновой фиксации и фиксации хромовыми смесями промывку производят проточной водой под краном, или неоднократной сменой воды (10-12 раз) в течение 24-48 ч. Материал, фиксированный в смесях с преобладанием спирта (фиксатор Карнуа) промывке не подвергается.
Существуют разные приспособления для промывки: 1) обычные стеклянные склянки с пробкой или завязанные марлей и резиновым шлангом, соединенные с краном; 2) для мелких объектов применяются специальные фарфоровые сита; 3) стеклянные трубочки, обвязанные с обеих сторон марлей.
Удобно провести промывку материала следующим образом: материал вместе с этикеткой переносят в марлевые узелки, перевязывают их ниткой и помещают в высокий стакан с водой. Сверху в стакан кладут воронку и все ставят под кран с проточной водой.
Далее необходимо получить срезы материала для их последующего окрашивания. Для этого образцы уплотняют, т.е. заливают в парафин или целлоидин, чтобы в последующем их можно было тонко резать. Предварительно образцы обезвоживают, чтобы гидрофобный уплотнитель смог проникнуть в ткань. Обезвоживание производится проведением материала по батарее спиртов возрастающей концентрации, что позволяет избежать разрывов и деформаций ткани.
Методика обезвоживания. Материал вынимают из марлевых узелков и вместе с этикеткой последовательно помещают в стаканчики или бюксы со спиртами (метанол или этанол) возрастающей концентрации – 70%, 80%, 96%, 100%. Чем нежнее материал, тем ниже первоначальная концентрация спирта (начинают с 20% спирта). Время выдерживания в каждом спирте зависит от толщины материала и строения органа: от 30 мин, 1-6 ч, и до 6-12 ч. В 96% и 100% спиртах выдерживают дважды. При перекладывании материала из слабого раствора спирта в спирт большей концентрации кусочки необходимо обсушить фильтровальной бумагой.
Схема и сроки выдерживания в спиртах растительного материала:
Источник