Фармакологическая рецепция способы передачи сигнала с рецепторов
Рецепторы — макромолекулы, функция которых заключается в связывании веществ-посредников и в преобразовании этой связи в действие, т, е. изменение клеточной функции. Рецепторы отличаются по своей структуре и способу преобразования контакта с лигандом в клеточный ответ (преобразование сигнала).
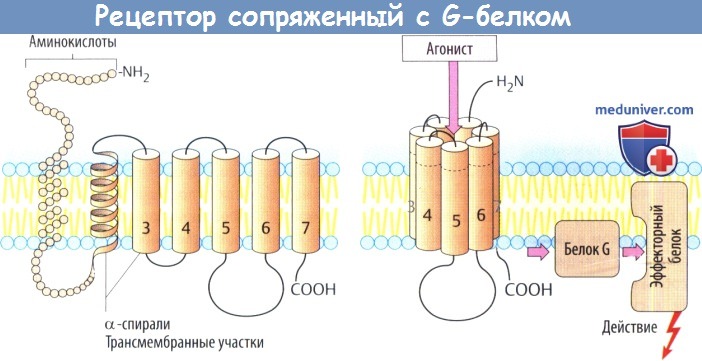
а) Рецепторы, сопряженные с белком G, состоят из цепи аминокислот, которая направлена в сторону мембраны и от нее в виде серпантина. С вне-мембранными петлевыми участками молекулы связаны углеводные остатки через различные точки N-гликозилирования.
Семь а-спиральных, охватывающих мембрану участков образуют окружность возле центральной ниши, которая несет участки для связывания медиаторных веществ. Связывание молекулы медиатора или структурно связанной молекулы агониста вызывает изменение конформации белка, в результате чего он вступает во взаимодействие с белком G (белок, связывающий нуклеотид гуанил).
Белки G располагаются в нижнем слое плазмолеммы и состоят из трех субъединиц, обозначаемых а, β и γ. Существует несколько белков G, которые отличаются в основном своей a-единицей. Контакте рецептором активирует белок G, что, в свою очередь, приводит к активации другого белка (фермента, ионного канала). Многие медиаторы действуют через рецепторы, сопряженные с белком G.
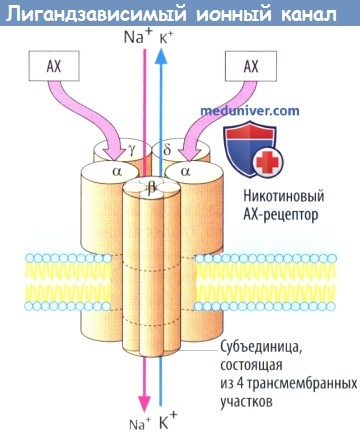
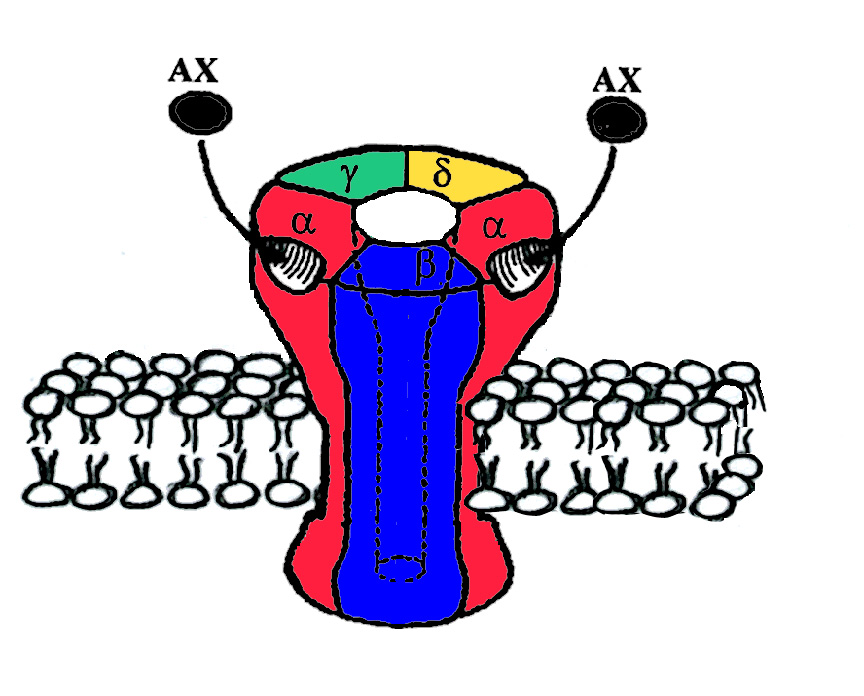
б) Примером лигандзависимого ионного канала является никотиновый холинорецептор на концевой пластинке двигательного нерва. Рецепторный комплекс образован пятью субъединицами, каждая из которых содержит четыре трансмембранных участка.
Одновременное связывание двух молекул АХ двумя а-субъединицами приводит к открытию ионного канала со входом Na + (и выходом некоторого количества К + ), деполяризации мембраны и активации потенциала действия. Нейронные N-холинорецепторы, очевидно, состоят лишь изо- и β-субъединиц.
Ряд рецепторов медиатора γ-аминомасляной кислоты (ГАМК) принадлежат к данной группе: подтип ГАМКA связан с хлорными каналами (и с участком связывания бензодиазепинов). Глутамат и глицин оба действуют через лигандзависимые ионные каналы.
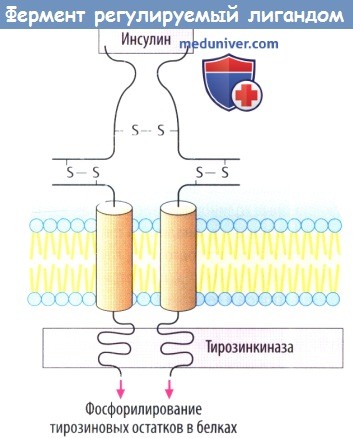
в) Белок инсулинового рецептора представляет собой управляемый лигандом фермент, каталитический рецептор. При связывании инсулина с внеклеточным участком «отключается» активность тирозинкиназы внутри клетки. Фосфорилирование белка приводит к изменению клеточной функции в результате образования других сигнальных белков. Рецепторы гормонов роста тоже принадлежат к классу каталитических рецепторов.
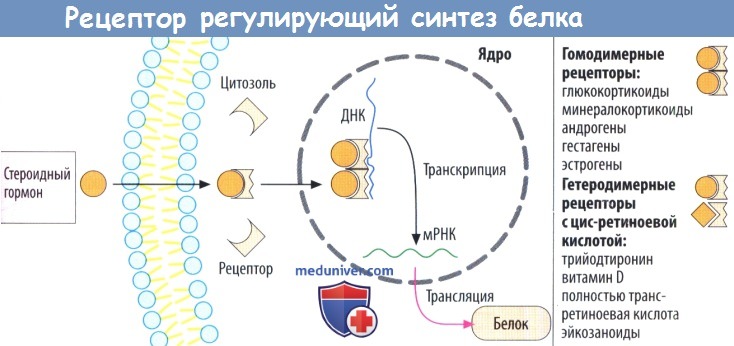
г) Рецепторы, регулирующие синтез белка, стероидов и гормонов щитовидной железы, находятся в цитозоле и в клеточном ядре соответственно. Белки рецепторов также расположены внутриклеточно, в зависимости от гормона — в цитозоле (глюкокортикоиды, минералокортикоиды, андрогены и гестагены) или в клеточном ядре (эстрогены, гормоны щитовидной железы).
При связывании гормона открывается скрытый в норме участок белка рецептора, что дает возможность последнему связаться с особой последовательностью нуклеотидов ДНК в гене и регулировать его транскрипцию. Из этого следует, что комплексы лиганд-рецептор работают как факторы, регулирующие транскрипцию. Обычно происходит активация или усиление и, редко, блокада транскрипции.
Комплексы гормон-рецептор взаимодействуют парно с ДНК. Эти пары (димеры) могут состоять из двух идентичных комплексов гормон-рецептор (гомодимерная форма, например, с гормонами надпочечников или половыми гормонами). Комплекс тиреоидный гормон-рецептор встречается в гетеродимерной форме и сочетается с комплексом цис-ретиноевая кислота-рецептор.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Фармакологическая рецепция способы передачи сигнала с рецепторов
Все клетки, от прокариот до клеток растений и животных, способны воспринимать сигналы извне и реагировать на них стереотипным образом, который позволяет им выживать, приспосабливаться и функционировать в соответствии с потребностями всего организма.
Эта реакция клеток выражается не просто в форме неких физических или химических явлений или изменений в их локальном окружении. Скорее, следут сказать, что клетка экспрессирует целый ансамбль сенсорных белков, или рецепторов, узнающих специфические внешние сигналы.
В ответ на эти сигналы рецепторы активируют разнообразные внутриклеточные регуляторные белки, которые, в свою очередь, обеспечивают адекватную реакцию клетки. Процесс узнавания внешнего сигнала и передачи соответствующей информации на внутриклеточные мишени называется преобразованием сигнала.
Клетка реагирует на все виды сигналов. Бактерии реагируют на питательные ингредиенты, токсины, тепло, холод, свет и химические сигналы, исходящие от других бактерий.
Клетки многоклеточных организмов экспрессируют рецепторы, специфичные по отношению к гормонам, нейромедиаторам, аутокринным и паракринным агентам (гормоноподобные вещества, секретируемые самой клеткой или ее окружением), к запаху и к молекулам, регулирующим рост или дифференцировку, а также к белкам, расположенным на поверхности клеток. Типичная клетка млекопитающих экспрессирует около пятидесяти различных рецепторов, которые проявляют чувствительность к разнообразным сигналам, а всего у млекопитающих экспрессируется несколько тысяч рецепторов.
Несмотря на большое разнообразие клеток и огромное количество веществ, которые они узнают, основные классы белков и процессы, участвующие в системе преобразования сигнала в клетках, достаточно консервативны.
• Рецепторы, связанные с G-белком, состоящие из семи спиралей, проходящих через мембрану. Они обеспечивают активацию гетеротримерных ГТФ-связывающих белков, которые называются G-белками. Эти белки связаны с внутренней стороной плазматической мембраны и передают сигналы на разные внутриклеточные белки.
• Протеинкиназные рецепторы часто представляют собой димеры белков, проходящих через мембрану, которые фосфорилируют внутриклеточные субстраты и, таким образом, изменяют форму и функции белков-мишеней. Эти протеинкиназы часто содержат домены, ответственные за взаимодействие с другими белками и принимающие участие в организации комплексов сигнальных белков, расположенных на внутренней поверхности плазматической мембраны.
• Фосфопротеинфосфатазы аннулируют эффект протеинкиназ, удаляя фосфатные группы.
• Прочие ферменты, молекулы которых проходят через мембрану, например, гуанилатциклаза, обладают структурой, близкой к рецепторным проте-инкиназам, однако характеризуются различными ферментативными активностями. Гуанилатциклаза катализирует превращение ГТФ в 3’5′-циклоГТФ, который участвует в распространении сигнала.
• Ионные каналы, хотя и имеют ряд отличий в деталях структуры, обычно представляют собой олигомеры субъединиц, из которых каждая состоит из нескольких трансмембранных сегментов. Эти субъединицы способны менять свою конформацию и относительное расположение, тем самым регулируя ионные потоки через центральную пору.
• Двухкомпонентные системы могут обладать трансмембранным расположением или локализуются в цитозоле. Число субъединиц у них также варьирует, но каждая двухкомпонентная система содержит гистидинкиназный домен или субъединицу, находящуюся под контролем сигнальной молекулы, и регулятор ответа, в структуре которого присутствует остаток аспарагиновой кислоты (Asp), способный фосфорилироваться.
• Некоторые рецепторы представляют собой трансмембранный каркас, который меняет конформацию или обладает способностью к олигомеризации своих доменов, расположенных с клеточной стороны. Это происходит в ответ на появление внеклеточных сигнальных молекул или лигандов. Таким образом, происходит отбор регуляторных белков, взаимодействующих между собой в определенных местах мембраны.
• Ядерные рецепторы представляют собой факторы транскрипции, часто гетеродимеры, которые находятся в цитоплазме до момента их активации агонистами, или постоянно присутствуют в ядре. Биохимические процессы, участвующие в преобразовании сигнала в разных клетках, поразительно сходны. Для обнаружения и обработки сигнала, клетки бактерий, грибов, растений и животных используют аналогичные белки и мультибелковые комплексы.
Например, у растений, грибов и в клетках животных обнаружены обладающие близкой структурой гетеротримерные G-белки и соответствующие им рецепторы, сохранившиеся в ходе эволюции. Аналогичным образом, в бактериях, грибах и у животных обнаружен 3’5′-циклический АМФ (цАМФ), представляющий собой внутриклеточную сигнальную молекулу; во всех клетках эукариот аналогичную роль играет Са2+. Во всех клетках в регуляции активности ферментов участвуют протеинкиназы и фосфопротеинфосфатазы.
Хотя основные биохимические компоненты и процессы передачи сигнала достаточно консервативны и используются многократно, они часто вовлекаются в самые разнообразные процессы и принимают участие в реализации множества различных физиологических реакций. Например, цАМФ образуется в бактериях, грибах и у млекопитающих с участием близких по свойствам ферментов, и в каждом организме белки-мишени для этого метаболита различны; так, для некоторых видов миксомицетов он является феромоном.
Часто для регуляции определенного процесса, например транскрипции, ионного транспорта, подвижности и метаболизма, клетки используют одни и те же сигнальные белки. Такие системы передачи сигнала собираются в сигнальные сети с тем, чтобы клетка могла координировать реакции на множественные сигналы с выполняемыми в данный момент функциями. В настоящее время в последовательностях отдельных процессов системы передачи сигнала, и в сети в целом, можно обнаружить присутствие элементов, характерных для компьютерных сетей.
Это усилители, логические шлюзы, контроль обратной и прямой связи, и память.
В дальнейших статьях вначале рассматриваются принципы организации клеточных систем передачи сигнала и общие вопросы стратегии, а затем обсуждаются соответствующие биохимические компоненты и процессы, а также пути конкретной реализации изложенных принципов.
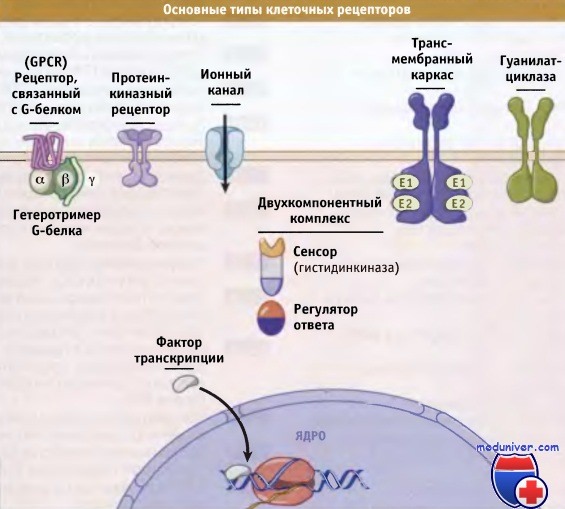
которые характеризуются общими механизмами действия и общностью структуры.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Лекция № 2. ФАрмакодинамика.
15. Фармакодинамика лекарственных веществ, определение, содержание.
16. Рецепторный механизм действия лекарственных веществ, типы рецепторов.
17. Взаимодействие лекарств со специфическими рецепторами биологически активных веществ. Роль цАМФ, фосфатидилинозитола и других вторичных медиаторов (мессенджеров) в механизмах действия лекарственных средств.
18. Краткая характеристика конечных фармакологических эффектов, вызываемых лекарственными веществами.
19. Виды действия лекарственных веществ. Характеристика местного, рефлекторного, резорбтивного, избирательного (элективного) и общеклеточного действия.
20. Виды действия лекарственных веществ. Характеристика прямого и косвенного, обратимого и необратимого, главного и побочного действия.
Лекция № 2.
15. Фармакодинамика лекарственных веществ.
Фармакодинамика – наука об изменениях функций организма под влиянием лекарств и о механизмах действия лекарств. Или проще – это то, что лекарство делает с организмом.
15. Содержание фармакодинамики: механизм развития эффекта, его характер, сила и длительность.
15. Типы (механизмы) действия лекарственных веществ. Это: 1) действие на специфические рецепторы; 2) физико-химическое действие на мембраны клеток; 3) прямое химическое взаимодействие.
15. Краткая характеристика типов (механизмов) действия лекарственных веществ.
1. Действие на специфические рецепторы. Лекарство связывается со специфическим белком (рецептор), локализованном: 1) в толще наружной мембраны клетки (чаще всего), 2) в цитозоле или 3) органеллах (ядро, митохондрии и т.д.) следствием такого связывания является изменение скорости протекания биохимических реакций в клетке (фармакологический эффект).
2. Например, лечебный эффект присыпок имеет физическую природу. Они предохраняют пораженные участки кожи от раздражения.
3. Прямое химическое взаимодействие. Некоторые лекарства непосредственно взаимодействуют молекулами в организме. Этот принцип лежит в основе применения антидотов при отравлениях химическими веществами.
16. Рецепторный механизм действия лекарственных веществ.
Типы рецепторов: 1) регуляторные белки, 2) ферменты, 3) транспортные белки, 4) структурные белки.
Регуляторные белки. Через них сигнальная молекула (медиатор, лекарство) передает информацию в клетку по 4 механизмам (рис. 2.1).
МЕХАНИЗМЫ ПЕРЕДАЧИ СИГНАЛА В КЛЕТКУ.

Цитозоль
МЕХАНИЗМЫ ПЕРЕДАЧИ ИНФОРМАЦИИ В КЛЕТКУ.
Механизмы передачи информации в клетку: 1) связывание лекарств с внутриклеточным рецептором, 2) регуляция активности внутриклеточной части трансмембранного рецептора, 3) регуляция открытия каналов для Na + или Cl — и с участием G-белков.
Первый механизм передачи лекарством информации в клетку – связывание с внутриклеточным рецептором.
Гидрофобная молекула (например, гидрокортизон) проникает в цитозоль клеток-мишеней и связывается с первым рецептором. Комплекс проникает в ядро и связывается с ДНК (второй рецептор). Активируется геном и запускается синтез специфических белков. Развивается фармакологический эффект.
Второй механизм передачи лекарством информации в клетку – регуляция внутриклеточной части трансмембранного рецептора. Например, инсулин связывается с наружной частью трансмембранного рецептора. После этого возрастает каталитическая активность внутриклеточной части этого же рецептора, которая называется тирозинкиназой, она фосфорилирует аминокислоту тирозин, входящую в состав белков. Изменяется метаболизм клетки, развивается фармакологический эффект.
Третий механизм передачи лекарством информации в клетку – регуляция открытия каналов для натрия или хлора.
Передатчики нервного импульса (например, ацетилхолин) водорастворимы и не могут проникнуть через гидрофобный слой наружной клеточной мембраны. Поэтому, чтобы получить сигнал от нервной системы и отреагировать на него изменением функции, в процессе эволюции клетки выработали так называемые приемники сигналов. Они встроили в мембрану белки-рецепторы, своеобразные сенсоры, как это видно на рисунке 2.2.
ые изменения. Белок зашевелился, стал как бы толще. При этомрвал
НИКОТИНОВЫЙ АЦЕТИЛХОЛИНОВЫЙ РЕЦЕПТОР.
Никотиновый ацетилхолиновый рецептор. На хромосомах в ядре клетки он имеет свой ген, который контролирует его синтез. Через него передается, в частности, нервный импульс с одной нервной клетки на другую.
Рецептор состоит из β-, γ-, δ- и двух α-субъединиц. Они образуют цилиндрическую структуру. Когда 2 молекулы ацетилхолина, выделившиеся в синапс соединяются с двумя α-субъединицами, происходит конформационные изменения.
Белок зашевелился, стал как бы толще. При этом в его центре открывается гидрофильный канал, через который натрий по градиенту концентрации проникают из синапса в клетку. Быстрота передачи этого сигнала- миллисекунды. Это чрезвычайно важно для моментальной передачи информации через синапсы.
Четвертый механизм передачи лекарством информации в клетку- с участием G-белков.
Включает три взаимодействующие между собой компонента (рис. 2.1): 1) встроенного в мембрану белка-рецептора; 2) внутриклеточного G-белка; 3) эффекторного элемента (фермент).
Этот тип передачи сигнала в клетку наиболее широко распространен в организме. Сначала внеклеточная сигнальная молекула (например: лекарство, медиатор) связывается с трансдермальным поверхностным рецептором. Рецептор, активизирует G-белок, расположенный на внутренней поверхности плазматической мембраны. G-белок изменяет функцию эффекторного элемента (например, аденилатциклазы). Эффекторный элемент изменяет концентрацию внутриклеточного вторичного посредника (например, цАМФ). цАМФ фосфорилирует белки, изменяется их функция. Развивается лечебный эффект.
Для чего нужны G-белки?
G-белки усиливают передаваемый сигнал от миллисекунд до десятков секунд. Экономится нервная энергия.
Рецепторы, сопряженные с G-белками относятся к семейству “серпентинных” (змеиных) рецепторов, называемых так потому, что их полипептидные цепи пересекают плазматическую мембрану 7 раз (рис. 2.3).






Механизмы передачи сигнала в клетку.
этому семейству принадлежат рецепторы для: 1) адренэргических аминов, 2) серотонина, 3) ацетилхолина (мускариновые), 4) многих пептидных гормонов. С их помощью воспринимаются, в частности, запахи, свет.
Это означает, что после достижения начального высокого эффекта (например, сокращение мышцы) ответ клетки постепенно уменьшается в течение секунд или минут, даже несмотря на постоянное присутствие сигнальной молекулы. Десенситизация обратима. Так, через 15 минут после удаления сигнальной молекулы, ее повторное воздействие ведет к реакции, сравнимой по величине с начальной.
Down – регуляция рецепторов.
Рецептор, при его чрезмерной стимуляции может погружаться в цитозоль и клетка с помощью лизосомальных ферментов «переваривает» его до аминокислот. Мембрана, где был рецептор, восстанавливается.
Если хирургически перерезать нервы, иннервирующие мышцу, то мышца не получит сигнал от нервной системы и не сможет сократиться. Реакция мышцы на денервацию направлена на синтез дополнительных рецепторов. Они синтезируются и встраиваются в наружную клеточную мембрану. Клетка «хочет» получить сигнал на сокращение. Сигнал не поступает (нерв перерезан), хотя рецепторов много и они особенно восприимчивы к медиатору. Рецепторы располагаются даже в других местах, вдали от места соединения нерва с мышцей. Это и есть так называемая Uр-регуляция рецепторов – синтез новых рецепторов клеткой и встраивание их в мембрану.
Рецепторы постоянно обновляются. Срок жизни рецептора – несколько дней. Взамен состарившемуся и разрушенному клеткой она строит новый. Это динамичный процесс.
Таким образом, лекарство – источник сигнала встроенный в мембрану рецептор принимает сигнал (нервный импульс, гормон, лекарство), G-белок усиливает сигнал. Эффекторный элемент (фермент) реализует этот сигнал, запуская синтез в клетке вторичных посредников. Они изменяют скорость протекания биохимических реакций в клетках и непосредственно реализуют сигнал, посылаемый нервной, гормональной системой или лекарством.
цАМФ. Участвует в передаче следующих эффектов: 1) мобилизация энергетических запасов при стрессе (распад гликогена в печени или триглицеридов в жировых клетках – эффекты катехоламинов (эпинефрин, изопреналин).
2) задержка воды почками – эффекты вазопрессина;
3) поддержание гомеостаза Са +2 – эффекты гормонов паращитовидных желез;
4) увеличение частоты и силы сокращений сердца – эффекты катехоламинов (эпинефрин, изопреналин);
5) регуляция биосинтеза стероидов в надпочечниках и половых железах – эффекты кортикотропина и фолликулостимулирующего гормона;
6) расслабление гладких мышц (например, бронхов) и многие другие эффекты эпинефрина.
К огда нервный или гормональный стимул завершается, эффекты цАМФ прекращаются путем активации фермента, разрушающего цАМФ.
Одним из механизмов лечебного действия кофеина и теофиллина является ингибирование распада цАМФ.
2). цГМФ. В отличие от цАМФ, участвует в передаче сигналов лишь некоторых типах клеток. В слизистой кишечника и гладких мышцах сосудов цГМФ функционирует параллельно с цАМФ-системой (как запасной). Механизм его действия фосфорилирование белков.
Повышенная концентрация цГМФ вызывает расслабление гладкой мускулатуры сосудов за счет дефосфорилирования легких цепей миозина.
Некоторые гормоны, медиаторы и факторы роста связываются с трансмембранным рецептором. Сигнал передается на G-белок, который активирует фосфолипазу С. Она расщепляет фосфолипиды плазматической мембраны с образованием двух вторичных посредников: 1) диацилглицерол, 2) инозитолтрифосфат.
Диацилглицерол. Активирует протеинкиназу С, которая фосфорилирует ферменты и изменяет их активность.
И 
Через фосфоинозитиды действует литий, используемый для лечения маниакально-депрессивных состояний.
Ферменты, как рецепторы лекарств.
При связывании с лекарствами они могут ингибироваться или (реже) активироваться. Например, дигидрофолатредуктаза – рецептор для метотрексата.
Транспортные белки как рецепторы лекарств. Например Nа + , К + , АТФаза – рецептор для сердечных гликозидов.
Структурные белки как рецепторы лекарств. Например, тубулин (белок митотического веретена) – рецептор для противоопухолевого и противовоспалительного средства колхицина.
В каждом случае взаимодействия лекарства с рецептором образуется лекарственно-рецепторный комплекс, приводящий к изменению метаболизма в клетке и органе. Развивается фармакологический эффект. Его величина пропорциональна количеству лекарственно-рецепторных комплексов.
Фосфорилирование: общий механизм.
Почти все механизмы передачи сигнала в клетку с помощью вторичных посредников обусловлены фосфорилированием.
В процессе эволюции организм не выработал специальные рецепторы для лекарств. Рецепторы действуют через рецепторы для медиаторов и гормонов. Почти все лекарства (исключение составляют средства для общей анестезии, мази, присыпки) действуют через рецепторы.
Для возбуждения или блокады рецепторов и получения лечебного эффекта врачи используют как сами медиаторы (норэпинефрин, дофамин и другие), так и лекарства, обладающие сродством к рецепторам. Чаще всего последние являются структурными аналогами медиаторов.
Рецепторы классифицируют по их чувствительности к естественным медиаторам и гормонам. Например, чувствительные к ацетилхолину рецепторы называют холинэргическими, чувствительные к эпинефрину (адреналину) – адренэргическими.
Некоторые вещества возбуждают соответствующий рецептор не путем непосредственного взаимодействия с ним, а за счет освобождения медиаторов из связанной (физиологически неактивной) формы или путем угнетения ферментов, разрушающих медиаторы.
Рецепторы занимают небольшую часть наружной клеточной мембраны. Например, ацетилхолиновые – только 1/6000 часть поверхности клетки
16. Лекарственные вещества как агонисты (в том числе частичные) и антагонисты лигандов.
Лекарства, действие которых связано с возбуждением рецепторов называют агонистами (например, холинэргические агонисты. Возбуждают ацетилхолиновые рецепторы). Агонисты бывают: 1) полные (вызывают максимальный ответ) и 2) частичные. Последние связываются с рецепторами и возбуждают их. Но фармакологический эффект слабее, чем от природного регулятора. Вещества, препятствующие действию специфических агонистов, называются антагонистами (блокаторами).
Конечные фармакологические эффекты лекарств (рис. 2.4).
Изменения, вызываемые всеми лекарствами в организме, имеют общие черты.
Источник