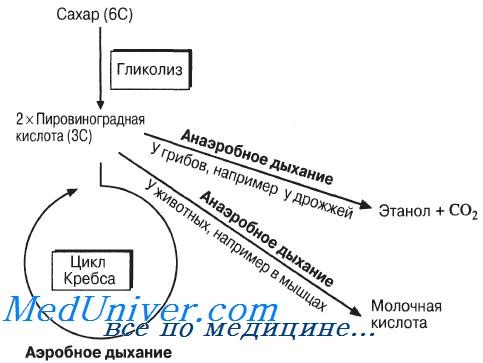
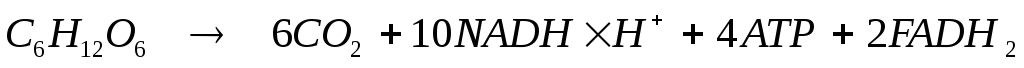Субстраты дыхания
В первую очередь растения используют в качестве дыхательного материала углеводы. При этом дыхательный коэффициент(молярное отношение СО2, выделившегося в процессе дыхания, к поглощённому за этот же промежуток времени О2) равен единице (
При недостатке углеводов могут быть использованы и другие субстраты. Особенно ярко это проявляется на проростках, развивающихся из семян, в которых в качестве запасного питательного вещества содержаться белки или жиры. Так как эти соединения по сравнению с сахарами являются более восстановленными, для их окисления требуется больше кислорода и дыхательный коэффициент становится меньше единицы. При этом жиры предварительно расщепляются до глицерина и жирных кислот, которые могут быть превращены в углеводы через глиоксилатный цикл. Использованию же белков в качестве субстрата дыхания предшествует их расщепление до аминокислот.
Пути дыхательного обмена
Существует два основных пути превращения дыхательного субстрата или окисления углеводов:
Дихотомический:гликолиз + цикл Кребса;
Относительная роль этих путей дыхания может меняться в зависимости от типа растений, возраста, фазы развития, а также в зависимости от условий внешней среды (например, дыхание осуществляется в диапазоне температур -50….+50 0 С).
Рассмотрим оба пути:
Гликолиз – процесс анаэробного распада глюкозы, идущий с освобождением энергии, конечным продуктом которого является пировиноградная кислота (ПВК).
Реакции гликолиза протекают в растворимой части цитоплазмы (цитозоле), где гликолитические ферменты организованы в мультиэнзимные комплексы с участием актиновых филаментов цитоскелета, и в хлоропластах.
Цепь реакций, составляющих путь гликолиза можно разбить на 3 этапа:
П
Первое субстратное фосфорилирование (синтез 2 АТФ за счёт окисления 2 молекул фосфоглицеринового альдегида (ФГА) до 2 молекул фосфоглицериновой кислоты (ФГК), при этом также образуется 2 NADH
Второе субстратное фосфорилирование (синтез 2 АТФ за счёт окисления 2 молекул ФГК до ПВК).
Таким образом, суммарное уравнение гликолиза выглядит следующим образом:
Функции гликолиза в клетке:
Связь между дыхательными субстратами и циклом Кребса.
Источник АТР и NADH
Некоторые его интермедиаты используются для синтетических процессов в клетке (например, ФЕП необходима для образования фенольных соединений и лигнина).
В хлоропластах запасённый крахмал метаболизируется в триозы, которые затем транспортируются из него.
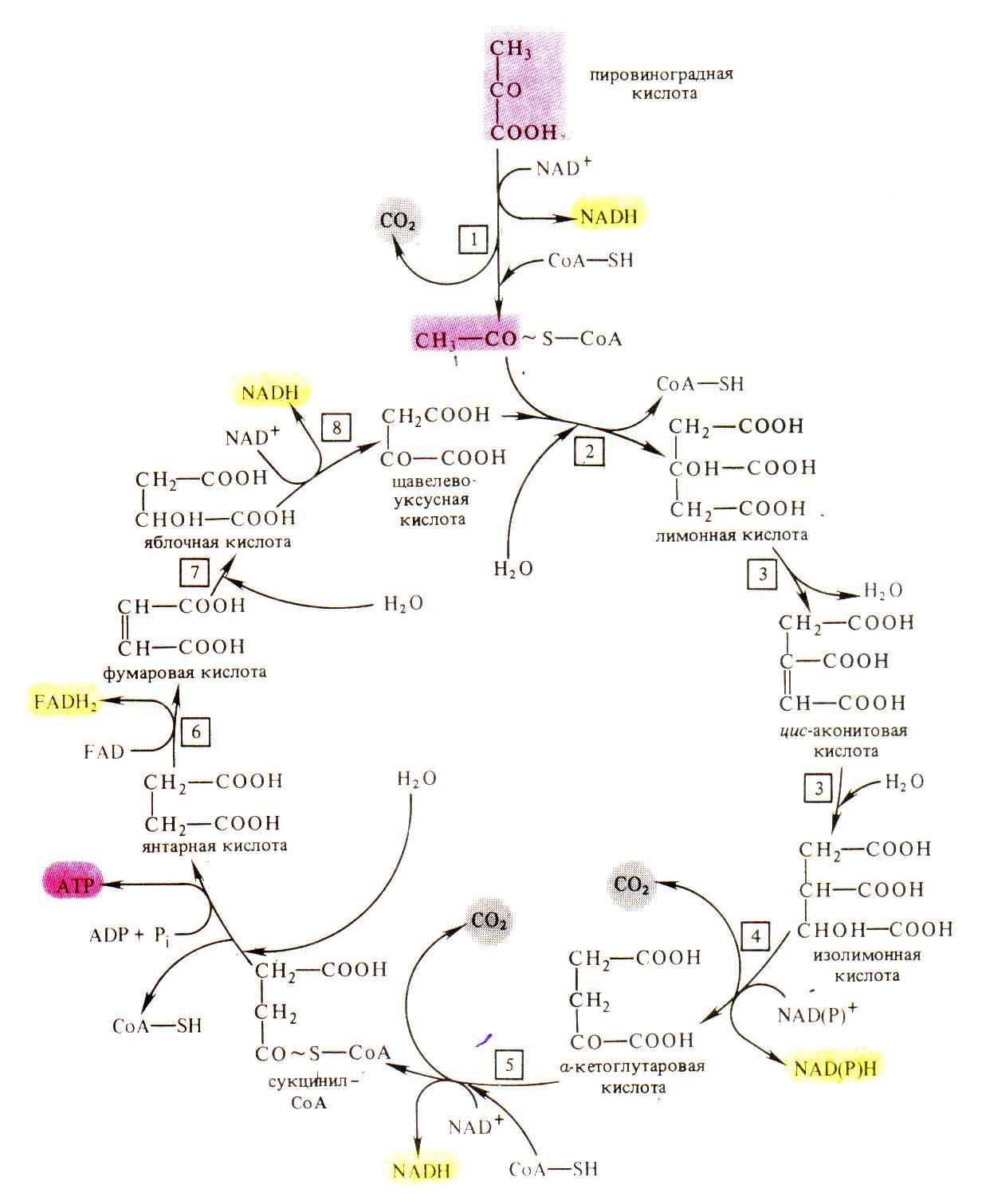
Цикл Кребса. В анаэробных условиях ПВК подвергается различным типам брожения. В присутствии же достаточного количества кислорода пируват полностью окисляется до углекислого газа и воды в цикле Кребса. Все участники этого процесса локализованы в матриксе или во внутренней мембране митохондрий.
Первым этапом окислительного расщепления ПВК является процесс образования активного ацетила в ходе окислительного декарбоксилирования при участии пируватдегидрогеназного мультиферментного комплекса (3 фермента и 5 коферментов).
В результате образуется ацетил коэнзим А:
Дальнейшее окисление ацетил — Со А осуществляется в ходе циклического процесса (цикла Кребса) начиная со взаимодействия со щавелевоуксусной кислотой (ЩУК):
В результате одного оборота цикла:
Сумарне рівняння аеробного окислення:
Сумарне рівняння гліколізу і циклу Кребса:
Глиоксилатный цикл(в животных клетках отсутствует). Можно рассматривать как модификацию цикла Кребса. Он активно функционирует в прорастающих семенах масличных растений, где запасные жиры превращаются в сахара (глюконеогенез). Локализован не в митохондриях, а в специализированных микротельцах –глиоксисомах.
В отличие от цикла Кребса, в каждом обороте участвует не одна, а две молекулы ацетил-СоА А (образуется при β-окислении жирных кислот)и используется для синтеза янтарной кислоты, которая выходит из глиоксисом, превращается в ЩУК и участвует в глюконеогенезе (обращённом гликолизе).
Пентозофосфатный путь окисления (ПФП, пентозный шунт). Окисление глюкозы по этому пути связано с отщеплением от глюкозы первого атома углерода в виде СО2.
Протекает этот процесс в растворимой части цитоплазмы клеток и в хлоропластах. ПФП дыхания особенно активен в тех клетках и тканях растений, в которых интенсивно идут синтетические процессы, такие, как синтез липидных компонентов мембран, нуклеиновых кислот, клеточных стенок, фенольных соединений.
В ПФП выделяют 2 этапа:
окисление глюкозы до рибулозо-5-фосфата с образованием 2NADPH*H + ;
рекомбинация сахаров для регенерации исходного субстрата при участии ферментов транскетолаз, трансальдолаз и изомераз.
Суммарное уравнение ПФП выглядит таким образом:
Основное значение ПФП не энергетическое, а пластическое:
1 — NADPH*H + , образующийся не в митохондриях, а в цитоплазме, используются главным образом в различных синтетических процессах (так как в отличие отNAD + , который присутствует в клетках в основном в более устойчивой окисленной форме,NADPH*H + — в восстановленной).
2 – В ходе ПФП синтезируются пентозы, входящие в состав нуклеиновых кислот и нуклеотидов (ATP,GTP,UTP,NAD,FAD,коэнзим А тоже являются нуклеотидами, в состав которых входит рибоза).
3 – Углеводы С3– С7необходимы для синтеза различных веществ. Например, из эритрозы синтезируется шикимовая кислота – предшественник многих ароматических соединений, таких как аминокислоты, витамины, дубильные и ростовые вещества, лигнин клеточных стенок и др.
4 – Компоненты ПФП принимают участие в темновой фиксации СО2. Только 2 из 15 реакций цикла Кальвина специфичны для фотосинтеза, остальные участвуют в ПФП.
5 – Триозы С3из ПФП могут превращаться в 3-ФГК и участвовать в гликолизе.
Активность ПФП в норме в общем дыхательном обмене составляет 10-40%. Активность увеличивается при неблагоприятных условиях: засухе, калийном голодании, инфекции, затенении, засолении, старении.
Дыхательная электронтранспортная цепь и окислительное фосфорилирование.
Цикл Кребса, глиоксилатный и ПФП функционируют только в условиях достаточного количества О2. В то же время О2непосредственно не участвует в реакциях этих циклов. Он необходим для заключительного этапа дыхательного процесса, связанного с окислением накопленных восстановленных коферментовNADH*H + иFADH2 в дыхательной электронтранспортной цепи (ЭТЦ) митохондрий. С переносом электронов по ЭТЦ сопряжен и синтез АТФ.
Дыхательная ЭТЦ, локализованная во внутренней мембране митохондрий состоит из четырех мультиэнзимных комплексов, в состав которых входят (по мере увеличения окислительно-восстановительного потенциала):
Из матрикса митохондрий при транспорте каждой пары электронов от NADH*H + к О2в трех участках ЭТЦ через мембрану наружу (в межмембранное пространство) переносятся по крайней мере шесть протонов Н + , при окисленииFADH2– таких участков лишь два.
В результате на мембране создается электрохимический потенциал ионов Н + , включающий химический или осмотический градиент (ΔрН) и электрический градиент.Согласно хемиоосмотичской теории Митчелла такой электрохимический трансмембранный потенциал ионов Н + и является источником энергии для синтеза АТФ за счет транспорта протонов через протонный канал мембранной АТФ-азы.
А
Процесс фосфорилирования АДФ с образованием АТФ, сопряженный с переносом электронов при ЭТЦ митохондрий, называется окислительным фосфорилированием.
При окислении NADH*H + коэффициент фосфорилирования =3, FADH2= 2, то есть энергии хватает на синтез соответственно 3 и 2 молекул АТФ.
Таким образом можно рассчитать общий энергетический выход (в молекулах АЬФ) окисления глюкозы:
При этом 10 NADH*H + = 30 АТФ, а 2 FADH2 = 4 АТФ. В итоге имеем 4 +30+4 =38 АТФ = 380 ккал/моль = 1591 кДж/моль энергии.
Источник
Дополнительные способы окисления дыхательных субстратов
Дыхание — это окисление органического вещества, являющегося субстратом дыхания. Субстратами для дыхания служат углеводы, жиры и белки.
Углеводы. При наличии углеводов большинство клеток использует в качестве субстратов именно их. Полисахариды (крахмал у растений и гликоген у животных и грибов) вовлекаются в процесс дыхания лишь после того, как они будут гидролизованы до моносахаридов.
Липиды (жиры или масла). Липиды составляют «главный резерв» и пускаются в дело в основном тогда, когда запас углеводов исчерпан. Предварительно они должны быть гидролизованы до глицерола и жирных кислот. Жирные кислоты богаты энергией и некоторые клетки, например мышечные, в норме получают именно от них часть необходимой им энергии.
Белки. Поскольку белки выполняют ряд других важных функций, они используются для производства энергии лишь после того, как будут израсходованы все запасы углеводов и жиров, например при длительном голодании (разд. 8.9.3). Белки предварительно гидролизуются до аминокислот, а аминокислоты дезаминируются (лишаются своих аминогрупп). Образовавшаяся в результате дезаминирования кислота вовлекается в цикл Кребса или превращается сначала в жирную кислоту, чтобы затем подвергнуться окислению.
Главную роль в клеточном дыхании играют два типа реакций — окисление и декарбоксилирование.
Окисление
В клетке происходят окислительные реакции трех типов.
1. ОКИСЛЕНИЕ МОЛЕКУЛЯРНЫМ КИСЛОРОДОМ.
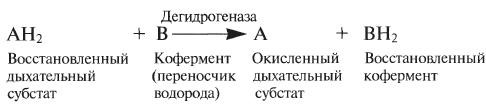
2. ОТЩЕПЛЕНИЕ ВОДОРОДА (ДЕГИДРИРОВАНИЕ). При аэробном дыхании окисление глюкозы происходит путем последовательных реакций дегидрирования. Отщепляемый при каждом дегидрировании водород используется для восстановления кофермента, называемого в этом случае переносчиком водорода:
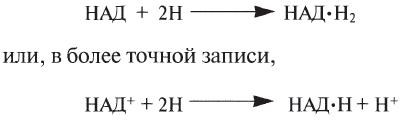
Большая часть этих реакций происходит в митохондриях, где переносчиком водорода служит обычно кофермент НАД (никотинамидадениндинуклеотид):
НАД*Н (восстановленный НАД) затем вновь подвергается окислению с высвобождением энергии. Ферменты, катализирующие реакции дегидрирования, называются дегидрогеназами. В ряде последовательных реакций дегидрирования весь отщепляемый от глюкозы водород передается переносчикам водорода. Этот водород окисляется затем кислородом до воды, а высвобождаемая при этом энергия используется для синтеза АТФ. Феномен выделения энергии при окислении (горении) водорода можно наблюдать, если поднести горящую свечку к пробирке с водородом. При этом раздастся легкий короткий хлопок, вроде миниатюрного взрыва. В клетке выделяется такое же количество энергии, но выделяется оно в ряде окислительно-восстановительных реакций при переходе водорода от одного переносчика к другому по так называемой дыхательной цепи.
3. ПЕРЕНОС ЭЛЕКТРОНОВ. Это происходит, например, при переходе одной ионной формы железа (Fe2+) в другую (Fe3+)
Электроны могут передаваться от одного соединения к другому, как водород в реакциях описанных выше. Соединения, между которыми совершается этот перенос, называются переносчиками электронов. Протекает этот процесс в митохондриях.
Декарбоксилирование
Декарбоксилирование — это отщепление углерода от данного соединения с образованием СО2. В молекуле глюкозы, помимо водорода и кислорода, содержится еще шесть атомов углерода. Поскольку для описанных выше реакций нужен только водород, углерод удаляется в реакциях декарбоксилирования. Образующийся при этом диоксид углерода представляет собой «побочный продукт» аэробного дыхания.
Источник
Анаэробное образование сукцината и облегчение его окисления возможные механизмы адаптации клетки к кислородному голоданию
Показаны важная роль анаэробного образования сукцината при аноксичееких и гипоксических состояниях, а также активация окисления сукцината в условиях гипоксии. Сделан вывод, что для поддержания знергсжки животных клеток в условиях кислородного голодания при аноксии и гипоксии целесообразно использовать субстраты, способные участвовать в анаэробном образовании сукцината, тогда как в гипоксическнх условиях имеет смысл использовать собственно сукцинат.
Ключевые слова: анаэробные процессы, гипоксия, митохондрии, субстраты.
Кислородное голодание встречается при многих физиологических состояниях и заболеваниях сердечно- сосудистой системы, легких, крови, отравлениях различными лекарственными препаратами и ядами. В зависимости от глубины кислородного голодания различают гипоксию и аноксию. На уровне митохондрии (MX) состояния гипоксии и аноксии отличаются по степени восстановленности дыхательных переносчиков. При аноксии, характеризующейся отсутствием доставки кислорода к клеткам, все переносчики дыхательной цепи полностью восстановлены. При гипоксии, когда частично сохранена доставка кислорода, наиболее удаленные от кислорода пиридин-нуклеотиды — НАД и НАДФ, как правило, восстановлены на 100%, тогда как часть флавопротеидов и цитохромныи участок дыхательной цепи остаются в значительной мере окисленными [1,2]. Такие различия в степени восстановленности пиридиннуклеотидов и флавопротеидов позволили предположить [З], что в условиях гипоксии имеется возможность для преимущественного окисления янтарной кислоты, поскольку, сукцинатдегидрогеназа в отличие от большинства других дегидрогеназ является флавинзависимым ферментом. При этом всегда возникал вопрос, откуда берется сукцинат, если НАД- зависимые субстраты окисляться не могут. С другой стороны, известно, что в аноксических условиях сукцинаг не окисляется, а накапливается в результате образования из НАД-зависимых субстратов и аминокислог [4 -7]. Мы предположили, что анаэробное образование сукцината (АОС) можег идти не только при аноксии, но и при гипоксии.
Цель настоящей работы заключалась в анализе функционального значения образования и окисления янтарной кислоты при кислородном голодании. Рассмотрим сначала аноксические условия. Аноксию моделировали in vitro путем инкубации густой суспензии MX (15 20 мг белка на мл) в закрытой ячейке, когда за несколько секунд МX полностью восстанавливают растворенный в инкубационной среде кислород, либо путем внесения в инкубационную среду антиминина А, блокирующею дыхательную цепь на уровне циюхрома b, что предотвращает окисление в дыхагельнои цепи как пиридиннуклеотидов, так и флавопротеидов.
Образование сукцината из различных субстратов измеряли методом Н-ЯМР-спектроскопии [7]. Оказалось, что АОС в изолированных митохондриях печени, сердца и коркового слоя почек крысы интенсивно идет из а-кетоглутаpaтa с малатом, а-кетоглутарата с аммонием и из малата (рис. 1).
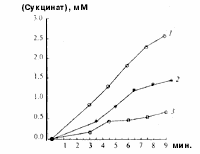 |
 |
В митохондриях печени морской свинки кроме указанных источников сушественный вклад в процесс АОС вносит фосфоенолпируват в присутствии бикарбоната.
В литературе доминирует представление о том, что адаптивная роль АОС обусловлена поддержанием образования богатых энергией соединений. Однако выполненые нами исследования [8,9] показали, что энергетический выход процесса АОС мал и в лучшем случае способен лишь затормозить падение oтношения АТФ/АДФ и величины трансмембранного электрохимического потенциала ионов водорода в изолированных MX. Но на уровне клеток активация АОС в присутствии глюкозы оказалась энергетически весьма эффективной: существенно препятствовала падению отношения АТФ/АДФ в изолированных кардиомионитах и культивируемых клетках почки [Ч].
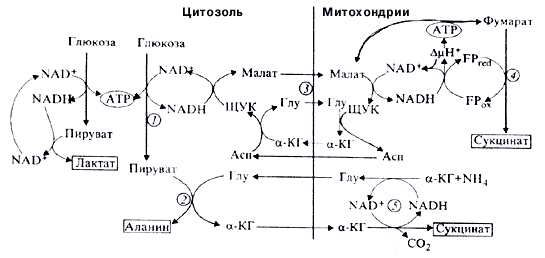
Сопоставив полученные данные с литературными данными, мы предположили, что АОС траст особую адаптивную роль в клетках животных. Не исключая из рассмотрения собственный вклад ДОС в энергетику клеток, можно полагать, чю зтот процесс выполняет также роль дополнительного акцептора воссгановительных эквивалентов, обеспечиваюшего их отток из цитозоля, из реакций гликолитичсской оксидоредукции, например, так, как это показано на рис.2.
В результате может поддерживаться высокая активность гликолиза при относительно небольшом приросте лактата. Соответственно конечными продуктами анаэробного обмена при этом являются не только лактат и пируват, но еще аланин и сукцинат.
Не исключено, что повышение устойчивости клеток и MX к аноксии при активации АОС обусловлено тем, что процесс АОС обеспечивает протекание ряда ферментативных реакций в цикле трикарбоновых кислот и в дыхательной цепи, несмотря на отсутствие кислорода. Поддержание редокс-превращений субтратов и дыхательных переносчиков является важным фактором морфофункциональной стабилизации MX (10).
Анализ гипоксической ситуации мы провели на двух моделях:
1) при инкубации MX в среде с пониженным в шесть раз парциальным давлением кислорода и
2) при торможении дыхательной цепи MX ротеноном, блокирующим перенос восстановительных эквивалентов от пиридиннуклеотидов до флавопротеидов, вследствие чего создастся ситуация, подобная гипоксии: восстановленные пиридиннуклеотиды и соответственно НАД-зависимые субстраты окисляться не могут, а флавопротеиды сохраняются в окисленном состоянии.
Оказалось, что в условиях ротенонового блока может происходить дисмутация а-кетоглутарата в присутствии аммония (реакция 5 на схеме рис.2), что проявляется в виде poтеноннечувствительного дыхания, ингибируемого малонатом (11).
Другие субстратные композиции, также и даже в большей мере, чем дисмутация а-кетоглутарата, способны поддерживать на фоне ротенонового блока генерацию трансмембранного потенциала, подобно экзогенному сукцинату (рис.3). Отсюда мы сделали вывод, что реакции АОС могут происходить не только в условиях аноксии при полном восстановлении дыхательной цепи,но и в том случае, когда имеется достаточно высокий уровень восстановленности пиридиннуклеотидов при гипоксии.
Рис.2. Схема возможного взаимодействия гликолитической оксидоредукции (1) некоторых реакций АОС <4,5>. Показано уменьшение образования лактата при вовлечении части пирувата в переаминирование (2) при использования восстановительных эквивалентов, поставляемых малат-аспартатным челноком (3). в реакциях восстановительного обращения цикла трикарбоновых кислот до сукцината (4) и в анаэробной дисмутации а-кетоглутарата (5).
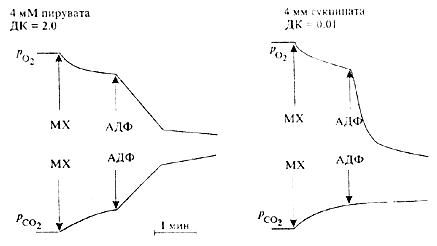
Для решения вопроса о возможности ускорения окисления сукцината относительно НАД-зависимых субстратов в гипоксических условиях мы использовали подход, позволяющий по скоростям потребления кислорода и образования углекислого газа отличать окисление сукцината от пирувата, а-кетоглутарата или изоцитрата. Как показано на рис.4, скорости дыхания и окислительного фосфорилирования при окислении сукцината намного выше, чем при окислении пирувата. Окисление пирувата сопряжено со значительным выделением в среду углекислоты, соответственно величина дыхательного коэффициента ДК достигает 2,0. Тогда как при окислении сукцината величина ДК нс превышает 0,01. Таким образом, по характерным кинетическим кривым регистрации потребления кислорода и образования СО2 можно уверенно отличать окисление пирувата (а также а-кегоглутарата или изоцитрата) от окисления сукцината.
В случае совместного внесения в инкубационную среду обоих субстратов, при последовательном увеличении отношения сукцицат/пируват происходило быстрое падение ДК и АДФ/0 с одновременным увеличением скоростей дыхания и степени восстановления трансмембранного потенциала после фосфорилирования АДФ, что характерно для сукцината (таблица1).
Возможно, это отражает предпочтительное окисление сукцината, хотя величина Км для сукцината в нормоксических условиях выше, чем для пирувата (таблица2).
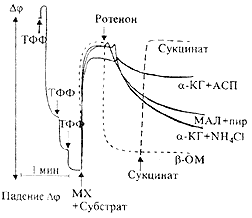
Рис.3. Изменение мембранного потенциала, измеренного по распределению липофильного катиона тетрафенилфосфония (ТФФ) между средой и матриксом MX печени, под влиянием ротенона и экзогенных субстратов (сукцината и субстратов — источников АОС). Условия инкубации, как на рис.1. Концентрация MX 4 мг белка на мл. Видно, что ЦАД-эаииснмые субстраты, способные участвовать в АОС, в отличие от б-оксимасляной кислоты, в разной степени поддерживают мембранный потецциал, подобно добавке сукцината.

Возможно, это отражает изменение как активности транспортных систем MX, так и соответствующих дегидрогеназ, в частности активацию сукцинатдегидрогеназы при увеличении степени восстановленности дыхательных переносчиков и, напротив, торможение окисления НАД-зависимых субстратов при росте отношения НАДН/НАД. Такое увеличение сродсгва к сукцинату при снижении PQ хорошо согласуется с ранее полученными нами данными о значительном (на 45 %) снижении содержания сукцината в ткани печени крыс, находившихся в течение 15-30 мин. в условиях гипоксии (в барокамере на высоте 8000 м).
Таблица 1. Изменение скоростей дыхания митохондрий печени, дыхательного коэффициента, отношения АДФ/0 и степени восстановления трансмембранного потенциала после фосфорилирования добавленного АДФ в зависимости от соотношения экзогенных сукцината и пирувата в инкубационной среде.
 |
 |
Таблица 2. Сравнение кажущихся констант сродства для сукцината и пирувата, рассчитанных в oбратных координатах 1/S и 1/V Лайнуивера-Бэрка по скоростям потребления кислорода изолированными митохондриями печени крысы.
 |
Представленные данные свидетельствуют о важной роли анаэробного образования сукцицата при аноксических и гипоксических состояниях, а также об активации окисления сукцината в условиях гипоксии. Отсюда следует, что в качестве средств поддержания энергетики животных клеток в условиях кислородного голодания при ацоксии и гипоксии целесообразно использовать субстраты, способные участвовать в анаэробном образовании сукцината, тогда как в гипоксических условиях имеет смысл использовать собственно сукцинат.
Источник