- Как регулируется активность ферментов?
- Способы регуляции активности ферментов
- 1.Доступность субстрата или кофермента
- 2. Компартментализация
- 3. Генетическая регуляция
- 4. Ограниченный (частичный) протеолиз проферментов
- 5. Аллостерическая регуляция
- 6. Белок-белковое взаимодействие
- 7. Ковалентная (химическая) модификация
- 3. Регуляция активности ферментов
Как регулируется активность ферментов?
Активность ферментов в клетке непостоянна во времени. Ферменты чутко реагируют на ситуацию, в которой оказывается клетка, на факторы, воздействующие на нее как снаружи, так и изнутри. Главная цель такой чувствительности ферментов – отреагировать на изменение окружающей среды, приспособить клетку к новым условиям, дать должный ответ на гормональные и иные стимулы, а в некоторых ситуациях – предоставить клетке шанс выжить.
Способы регуляции активности ферментов
В клетке имеется несколько способов регуляции активности ферментов – одни способы подходят для любых ферментов, другие более специфичны.
1.Доступность субстрата или кофермента
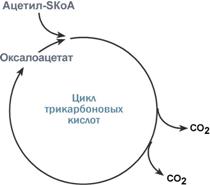
Роль оксалоацетата для работы ЦТК
Здесь работает закон действия масс – фундаментальный закон химической кинетики: при постоянной температуре скорость химической реакции пропорциональна произведению концентрации реагирующих веществ. Или упрощенно – скорость, с которой вещества реагируют друг с другом, зависит от их концентрации. Таким образом, изменение количества хотя бы одного из субстратов прекращает или начинает реакцию.
Например, для цикла трикарбоновых кислот (ЦТК) таким субстратом является оксалоацетат (щавелевоуксусная кислота). Наличие оксалоацетата «подталкивает» реакции цикла, что позволяет вовлекать в окисление молекулы ацетил-SКоА.
2. Компартментализация
Компартментализация – это сосредоточение ферментов и их субстратов в одном компартменте (одной органелле) – в эндоплазматическом ретикулуме, митохондриях, лизосомах, ядре, плазматической мембране и т.п.
3. Генетическая регуляция
Генетическая регуляция (изменение количества фермента) может происходить в результате увеличения или снижения его синтеза. С этой точки зрения ферменты можно подразделить на три группы:
- Конституитивные – такие ферменты, которые образуются в клетке постоянно, независимо от наличия субстрата (нейрональная NO-синтаза, ферменты гликолиза, β-окисления жирных кислот, репарации ДНК).
- Индуцируемые – синтез этих ферментов возрастает при наличии соответствующих стимулов — индукторов.
- Репрессируемые – образование таких ферментов в клетке при необходимости подавляется.
Изменение скорости синтеза фермента (индукция или репрессия) обычно зависит от количества определенных гормонов или метаболитов процесса.
Примеры индуцируемых ферментов:
- гормоны глюкокортикоиды стимулируют синтез ферментов глюконеогенеза, что обеспечивает стабильность концентрации глюкозы в крови при длительном голоданиии и устойчивость ЦНС к стрессу,
- исчезновение пищеварительных ферментов при длительном голодании и индукция их синтеза в восстановительный период в результате возобновления секреции гормонов ЖКТ,
- при беременности и после родов в молочной железе индуцируется синтез фермента лактозосинтазы под воздействием лактотропного гормона,
- токсические субстраты (например, этанол и барбитураты) стимулируют в печени синтез «своего» изофермента цитохрома Р450, который окисляет и обезвреживает эти вещества,
- при активации цитокинами моноцитов и макрофагов в них начинается синтез индуцируемой NO-синтазы.
Примеры репрессируемых ферментов:
- в печени репрессия фермента синтеза холестеролаГМГ-SKoA-редуктазы под влиянием холестерина и желчных кислот,
- в печени репрессия синтеза ферментов глюконеогенеза под действием инсулина,
- подавление синтеза триптофана бактериями при деятельности триптофанового оперона.
4. Ограниченный (частичный) протеолиз проферментов
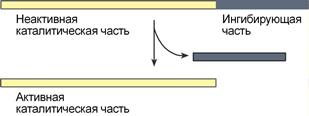
Ограниченный (частичный) протеолиз проферментов подразумевает, что синтез некоторых ферментов осуществляется в виде более крупного предшественника и при поступлении в нужное место этот фермент активируется через отщепление от него одного или нескольких пептидных фрагментов. Подобный механизм защищает внутриклеточные структуры от повреждений.
Схема активации фермента способом
«ограниченного протеолиза»
Примером служит активация протеолитических ферментов желудочно-кишечного тракта (трипсиноген, пепсиноген, прокарбоксипептидазы), факторов свертывающей системы крови, лизосомальных ферментов (катепсины).
Секреция ряда ферментов за пределы клетки в неактивном состоянии позволяет предохранить клетки от повреждения (пищеварительные ферменты) или сохранить белок в плазме крови до наступления определенного момента (факторы свертывания крови, белки системы комплемента, калликреин-кининовой и ренин-ангиотензиновой систем).
5. Аллостерическая регуляция
Аллостерические ферменты построены из двух и более субъединиц: одни субъединицы содержат каталитический центр, другие имеют аллостерический центр и являются регуляторными. Присоединение эффектора к аллостерической (регуляторной) субъединице изменяет конформацию белка и, соответственно, активность каталитической субъединицы.
Аллостерические ферменты обычно стоят в начале метаболических путей, и от их активности зависит течение многих последующих реакций. Поэтому они часто называются ключевыми ферментами.
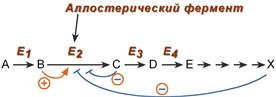
Общий принцип аллостерической регуляции
В качестве отрицательного регулятора может выступать конечный или промежуточный метаболит биохимического процесса или продукт данной реакции, т.е включается механизм обратной отрицательной связи . Если регуляторами являются начальный метаболит или субстрат реакции, то говорят о прямой регуляции , она может быть как положительной, так и отрицательной. Также регулятором могут быть метаболиты биохимических путей, каким то образом связанных с данной реакцией.
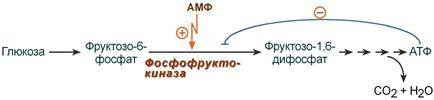
Регуляция фосфофруктокиназы конечным продуктом
Например, фермент энергетического окисления глюкозы, фосфофруктокиназа, регулируется промежуточными и конечными продуктами этого распада. При этом АТФ, лимонная кислота, фруктозо-1,6-дифосфат являются ингибиторами, а фруктозо-6-фосфат и АМФ – активаторами фермента.
- В большинстве клеток организма (кроме печени) при регуляции синтеза холестерола аллостерическим ингибитором ключевого фермента этого процесса ГМГ-КоА-редуктазы выступает сам холестерол, что быстро и точно регулирует его количество,
- Фермент ЦТК изоцитрат-дегидрогеназа активируется при помощи АМФ и АДФ и ингибируется влияниями АТФ и НАДН.
6. Белок-белковое взаимодействие
Термин белок-белковое взаимодействие обозначает ситуацию, когда в качестве регулятора выступают не метаболиты биохимических процессов, а специфичные белки. В целом ситуация схожа с аллостерическим механизмом: после влияния каких-либо факторов на специфичные белки изменяется активность этих белков, и они, в свою очередь, воздействуют на нужный фермент.
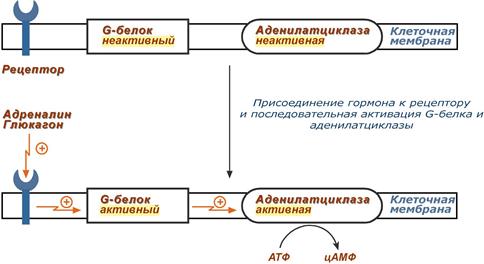
1. К примеру, мембранный фермент аденилатциклаза является чувствительным к воздействию мембранного G-белка, который сам активируется при действии на клетку некоторых гормонов (например, адреналина и глюкагона).
Упрощенная схема активации аденилатциклазы
Более подробно механизм активации G-белка можно посмотреть здесь.
2. Еще примером белок-белкового взаимодействия может быть регуляция активности протеинкиназы А через механизм ассоциации-диссоциации .
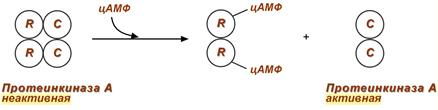
Протеинкиназа А является тетрамерным ферментом, состоящим из 2 каталитических (С) и 2 регуляторных (R) субъединиц. Активатором для протеинкиназы А является цАМФ. Присоединение цАМФ к регуляторным субъединицам фермента вызывает их отхождение от каталитических субъединиц. Каталитические субъединицы при этом активируются.
Активация протеинкиназы А при помощи цАМФ
7. Ковалентная (химическая) модификация
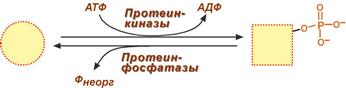
Ковалентная модификация заключается в обратимом присоединении или отщеплении определенной группы, благодаря чему изменяется активность фермента. Чаще всего такой группой является фосфорная кислота, реже метильные и ацетильные группы. Фосфорилирование фермента происходит по остаткам серина и тирозина. Присоединение фосфорной кислоты к белку осуществляют ферменты протеинкиназы, отщепление – протеинфосфатазы.
Изменение активности фермента
при фосфорилировании-дефосфорилировании
Ферменты могут быть активны как в фосфорилированном , так и в дефосфорилированном состоянии .
Например, в мышцах ферменты гликогенфосфорилаза и гликогенсинтаза
- при нагрузке фосфорилируются, при этом фосфорилаза гликогена становится активной и начинает расщепление гликогена и сжигание глюкозы, а гликогенсинтаза при этом неактивна.
- во время отдыха при синтезе гликогена оба фермента дефосфорилируются, синтаза при этом становится активной, фосфорилаза – неактивной.
Источник
3. Регуляция активности ферментов
Способность к регуляции делает ферменты важными участниками и своеобразными организаторами клеточных процессов в организме человека. Регуляция скорости ферментативных реакций в клетке — основной механизм не только контроля и координации метаболических путей, но и роста и развития клетки, а также ее ответа на изменение окружающей среды.
Существует два основных способа контроля скорости ферментативных реакций:
— Контроль количества фермента.
Количество фермента в клетке определяется соотношением скоростей его синтеза и распада. Этот способ регуляция скорости ферментативной реакции является более медленным процессом (проявляется спустя несколько часов), чем регуляция активности фермента (практически мгновенный ответ).
— Контроль активности фермента.
Активность фермента может регулироваться путем взаимодействия с определенными веществами, изменяющими конформацию активного центра.
Некоторые способы регуляции активности ферментов представлены на рисунке 10.
Регуляция субстратом реакции
Регуляция ферментативной активности, осуществляемая в центре присоединения субстрата, носит название изостерической.
Одним из относительно простых способов регуляции активности ферментов является регуляция с помощью изменения концентрации субстратов реакции. Чем больше в распоряжении фермента имеется молекул веществ, превращения которых он осуществляет, тем выше (до определенных пределов) скорость процесса. При насыщении всех молекул фермента субстратом скорость реакции достигает максимального уровня. В дальнейшем скорость реакции может понизиться по мере исчерпания запасов субстрата и вновь возрасти при их восстановлении.
Слишком большая концентрация субстрата также может понижать скорость ферментативной реакции. Этот феномен носит название субстратного торможения.
В качестве примера субстратного торможения можно привести фермент, расщепляющий биологически активное вещество ацетилхолин — ацетилхолинэстеразу (АХЭ). К активному центру АХЭ субстрат (ацетилхолин) присоединяется двумя концами молекулы одновременно. При увеличении концентрации ацетилхолина с одной молекулой фермента могут одновременно реагировать две молекулы субстрата, но разными концами. В этом случае реакция, суть которой заключается в разрыве сложноэфирной связи в середине молекулы ацетилхолина (с образованием холина и уксусной кислоты), оказывается невозможной, и молекулы ацетилхолинэстеразы, нагруженные субстратом, оказываются тем не менее лишенными активности.
Уменьшение концентрации ацетилхолина в среде приведет к диссоциации неактивного комплекса и снимет торможение. Этот механизм имеет важное физиологическое значение для регуляции концентрации ацетилхолина, который выполняет в нервной системе и мышцах роль медиатора, передающего возбуждение с одной клетки на другую.
Аллостерическая регуляция. Фермент изменяет активность с помощью нековалентно связанного с ним эффектора. Связывание происходит в участке, пространственно удаленном от активного (каталитического) центра (allos — иной). Это связывание вызывает конформационные изменения в молекуле белка, приводящие к изменению определенной геометрии каталитического центра. Активность может увеличиться — это активация фермента, или уменьшиться — это ингибирование.
«Сообщение» о присоединении аллостерического активатора передается посредством конформационных изменений каталитической субъединице, которая становится комплементарной субстрату, и фермент «включается». При удалении активатора фермент вновь переходит в неактивную форму и «выключается». Аллостерическая регуляция является основным способом регуляции метаболических путей.
Обычно ферментативные реакции в клетке организованы в метаболические цепи или циклы, где самая медленная стадия лимитирует скорость всей цепи, то есть последовательности реакций, объединяемых общими субстратами (рис.9).
В таких цепях нередко наблюдается так называемая регуляция по типу обратной связи. Она служит для того, чтобы скорректировать работу цепи с потребностями клетки в конечном продукте. Принцип регуляции заключается в том, что ферменты, стоящие в начале цепи, ингибируются отдаленными метаболитами или конечными продуктами.
Такая регуляция чаще всего происходит по аллостерическому типу, когда молекула регулятора связывается с ферментом в специальном регуляторном центре. Аллостерические ферменты часто выполняют ключевую роль в регуляции обмена веществ, поскольку обладают способностью определять количество важных метаболитов и изменять в соответствии с этим свою активность.
В каждой метаболической цепи есть фермент, который задает скорость всей цепочке реакций. Он называется регуляторным ферментом.
Ферменты, регулирующие скорость метаболических путей:
— обычно действуют на ранних стадиях метаболических путей, в местах ключевых разветвлений метаболических путей;
— катализируют в условиях клетки практически необратимые реакции, протекающие наиболее медленно (ключевые).
Метаболическая цепь: А, В, С, D — метаболиты, Е1, Е2, Е3, Е4 — ферменты
Химическая модификация молекул ферментов (рис.10)
Химическая модификация белков осуществляется за счет присоединения к аминокислотным остаткам в молекуле белка определенных групп: фосфатной группы (при участии протеинкиназ), остатка жирной кислоты (с помощью ацилтрансфераз), углеводных компонентов (гликозил-трансферазы, гликозидазы).
Белки, как правило, имеют лабильную структуру, упаковка которой сильно зависит от свойств химических групп, входящих в состав молекулы. Поэтому присоединение к молекуле белка дополнительных группировок существенно влияет на структуру, а следовательно, и на ферментативную активность молекулы. Такая регуляция носит приспособительный (адаптационный) характер.
Пример. Регуляция активности ферментов путем фосфорилирования-дефосфорилирования. Фермент изменяет активность в результате ковалентной модификации. `
В этом случае фосфатная группа — ОРО3 2- присоединяется к гидроксильным группам в остатках серина, треонина или тирозина. В зависимости от природы фермента фосфорилирование может его активировать или, наоборот, инактивировать. Реакция присоединения фосфатной группы и ее отщепление катализируют специальные ферменты — протеинкиназы и протеинфосфатазы.
Фосфорилирование — распространенный способ изменить свойства некоторых клеточных белков. Так, при фосфорилировании компонентов цитоскелета (комплекса структурных белков, обеспечивающих поддержание прочности и функционирования клетки) изменяются прочность его взаимодействия с мембраной и форма клеток. Фосфорилирование белков — регуляторов сокращения активирует сократительную реакцию мышцы.
Регуляция с помощью химической модификации белка приводит к долговременным последствиям: модифицированные молекулы сохраняют свои функции измененными до тех пор, пока специальные ферменты не отщепят модифицирующую белок химическую группу и не вернут его в исходное состояние.
Регуляция путем белок-белковых взаимодействий (ассоциации-диссоциации субъединиц в олигомерном ферменте). (рис.10) Например, фермент протеинкиназа в неактивной форме построена как тетрамер R2C2 (R и С — разные субъединицы). Активная протеинкиназа представляет собой субъединицу С, для освобождения которой необходима диссоциация комплекса. Активация фермента происходит при участии цAMP, который способен присоединиться к субъединице R, после чего изменяется конформация, комплементарность субъединиц R и С и происходит диссоциация комплекса: R2C2 + 2cАМР 2С + 2(R -цАМР)
Протеинкиназа фосфорилирует соответствующие ферменты, изменяет их активность и, следовательно, скорость метаболизма в клетке.
Активация ферментов путем частичного протеолиза
Чачтичный протеолиз-разрушение белковой структкры до аминокислотных остатков,для того.чтобы слизистая пожелудочной не разрушилась от трипсина
. Некоторые ферменты синтезируются первоначально неактивными и лишь после секреции из клетки переходят в активную форму. Неактивный предшественник называется проферментом. Активация профермента включает модификацию первичной структуры с одновременным изменением конформации. Например, трипсиноген, синтезированный в поджелудочной железе, затем в кишечнике превращается в трипсин путем удаления фрагмента с N-конца гексапептида. Расщепление определенных пептидных связей «запускает» новые взаимодействия R-групп по всей молекуле, приводя к новой конформации, в которой R-группы активного центра занимают оптимальное положение для катализа (рис.10).
Роль липидного окружения.
Изменение вязкости микроокружения белковых молекул управляет взаимодействием между белками в олигомерных комплексах и регулирует активность мембраносвязанных ферментов.. Этот тип регуляции, который обнаружен в случае многих мембранных белков, обеспечивает тонкую настройку их работы на сиюминутные потребности клетки.
Источник