- Для бактериофага характерен способ репродукции
- Адсорбция бактериофага
- Инъекция бактериофага
- Репродукция бактериофага
- Выход дочерних популяций бактериофага
- Негативные колонии бактериофага
- Бактериофаги
- БАКТЕРИОФАГИ КАК АЛЬТЕРНАТИВА АНТИБИОТИКАМ В ЛЕЧЕНИИ ИНФЕКЦИЙ
- Что такое бактериофаги
- Убить убийцу
- Практика, обогнавшая теорию
- Естественное против искусственного
- Бактериофаги сегодня
Для бактериофага характерен способ репродукции
Взаимодействие бактериофагов с клеткой специфично, так как они, как правило, инфицируют бактерии только определённого вида (рис. 5-11). Подобно вирусам животных, репродуктивный цикл литических бактериофагов включает адсорбцию свободного фага на клетке, инъекцию ДНК, репродукцию фага, выход дочерних популяций.
Адсорбция бактериофага
Прикрепление фага к бактерии происходит при помощи поверхностных структур бактериальной стенки, служащих рецепторами для вирусов. Например, рецепторы для фагов ТЗ, Т4 и расположены в липополисахаридном слое, для Т2 и Т6 — в наружной мембране. На бактериях клеточной оболочки (протопласты, L-формы) бактериофаги не адсорбируются. Некоторые фаги в качестве рецепторов используют F-пили. Помимо рецепторов, адсорбция фага зависит от рН среды, температуры, наличия катионов и некоторых соединений (например, триптофана для Т2-фага). При избытке фага на одной клетке может адсорбироваться до 200-300 вирусных частиц.
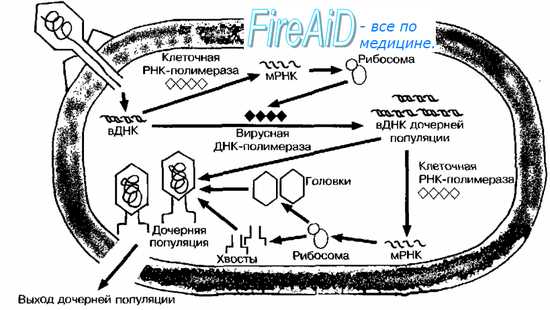
Инъекция бактериофага
После адсорбции происходит ферментативное расщепление клеточной стенки лизоцимом, находящимся в дистальной части отростка. Базальная пластина хвоста лизирует прилегающий фрагмент клеточной стенки, выделяя присутствующий в отростке лизоцим. Одновременно в чехле высвобождаются ионы Са2+, активизирующие АТФазу, что вызывает сокращение чехла и вталкивание стержня хвоста через ЦПМ в клетку. Затем вирусная ДНК впрыскивается в цитоплазму (внедрение вирусной ДНК). Поскольку диаметр канала лишь немного превышает диаметр молекулы ДНК (около 20 нм), то ДНК способна попадать в цитоплазму только в форме нити.
Репродукция бактериофага
Проникнув в клетку, ДНК фага «исчезает»; уже через несколько минут обнаружить вирус не удаётся. В этот, так называемый скрытый период (эклипс) вирус берёт на себя генетическое управление клеткой, осуществляя полный цикл репродукции фага. К его окончанию составляющие фага соединяются в зрелый вирион.
Синтез фаговых белков. В первую очередь синтезируются ферменты, необходимые для образования копий фаговой ДНК. К ним относятся ДНК-полимераза, киназы (для образования нуклеозидтрифосфатов) и тимидилат синтетаза. Они появляются в клетке через 5-7 мин после её заражения. Клеточная РНК-полимераза транскрибирует вирусную ДНК в мРНК, которая транслируется бактериальными рибосомами в «ранние» белки фага, включая вирусную РНК-полимеразу и белки, способные посредством различных механизмов ограничивать экспрессию бактериальных генов. Вирусная РНК-полимераза осуществляет транскрипцию «поздних» белков (например, белков оболочки и эндолизина), необходимых для сборки фаговых частиц дочернего поколения. Некоторые вирусы расщепляют ДНК клетки-хозяина до нуклеотидов, чтобы использовать их для синтеза собственных нуклеиновых кислот.
Репликация нуклеиновых кислот реализуется за счёт активности вновь синтезированных вирусных ДНК-полимераз, производящих множественные копии вирусных нуклеиновых кислот.
Выход дочерних популяций бактериофага
Вновь синтезированные белки формируют в цитоплазме пул предшественников, входящих в состав головок и хвостов дочерних вирусных частиц. Другой пул содержит ДНК потомства. Специальные аффинные области в вирусной ДНК индуцируют объединение предшественников головок вокруг агрегатов нуклеиновой кислоты и образование ДНК-содержащих головок. Заполненная головка затем взаимодействует с хвостовой частью, образуя функциональный фаг. Весь процесс (от адсорбции до появления вновь синтезированных вирусов) занимает около 40 мин. После образования потомства («урожай», или выход фага, составляет 10-200 из одной инфицирующей частицы) клетка хозяина лизируется, высвобождая дочернюю популяцию. В разрушении клеточной стенки участвуют различные факторы: фаговый лизоцим, увеличенное внутриклеточное давление. Вирус, по-видимому, также стимулирует образование аутолизинов либо блокирует механизмы, регулирующие их синтез (подобные литические факторы выявлены в фаголизатах многих бактерий).
Негативные колонии бактериофага
Размножение фагов в бактериальных культурах, засеянных сплошным «газоном» на твёрдых средах, сопровождается лизисом бактерий и образованием зон просветления — «стерильных пятен». Для их обозначения предложен термин «негативные колонии бактериофага». У разных фагов они имеют строго определённые размеры и форму (например, звёздчатую у дизентерийных фагов). При заражении бульонных культур литическим фагом наблюдают просветление среды. Способность образовывать негативные колонии в культурах чувствительных бактерий в микробиологической диагностике возбудителей инфекционных болезней известна как фагодиагностика
Источник
Бактериофаги
БАКТЕРИОФАГИ КАК АЛЬТЕРНАТИВА АНТИБИОТИКАМ В ЛЕЧЕНИИ ИНФЕКЦИЙ
Бактериофаги — вирусы бактерий, естественные микроорганизмы, которые, размножаясь внутри бактериальной клетки, ведут к ее быстрой гибели.
Из истории открытия
В 1896 году английский бактериолог Э. Ханкин, исследуя антибактериальное действие воды индийских рек, пришел к выводу о существовании агента, проходящего через бактериальные фильтры и вызывающего лизис холерных вибрионов. Российский микробиолог Н. Ф. Гамалея в 1897 году наблюдал лизис бацилл сибирской язвы. Однако первой научной публикацией о фагах стала статья английского микробиолога Ф. Туорта, в которой он в 1915 году описал инфекционное поражение стафилококков, значительно изменявшее морфологию колоний. В 1917 году канадский бактериолог Ф. Д’Эрелль независимо от Туорта сообщил об открытии вируса, «пожирающего» бактерии — бактериофага.
Интересный факт: при нанесении бактериофага на влажные слизистые он за 20 минут очищает их от определенного вида бактерий, например от стафилококка. Так быстро не работает ни один антибиотик.
Действие бактериофагов отличается от действия антибиотиков:
- Для определенного вида бактерий существует свой определенный бактериофаг. Но стоит отметить, что не ко всем бактериям есть бактериофаги (это основной недостаток этих препаратов). Для решения вопроса, какую терапию выбрать для лечения инфекции, врач должен сначала взять материал для посева на флору с точным определением вида возбудителя и только после получения анализа на чувствительность микроорганизма к бактериофагам выбрать препарат.
- Бактериофаги не действуют на нормофлору (нормальные бактерии), поэтому лечение бактериофагами экологично и не требует коррекции нормофлоры.
- Бактериофаги не влияют на организм человека, поскольку не способны проникнуть в клетки человека. Поэтому бактериофаги не токсичны и не вызывают побочных эффектов.
- После уничтожения патогена элиминируются (самовыводятся) из организма.
- Бактериофаги просты в применении: большинство их производится в жидком виде. Доступно наружное орошение при местном применении, полоскании, в виде микроклизм при кишечных инфекциях. Но действуют бактериофаги только местно, то есть именно там, где вы их применяете при полоскании, орошении и закапывании. В отличие от антибиотиков, которые при приеме внутрь распределяются по организму и действуют во всех органах и тканях.
- Бактериофаги стимулируют местный иммунитет, так как частицы уничтоженных бактерий побуждают иммунную систему к выработке специфических антител. Из-за этого свойства бактериофаги являются препаратом выбора в лечении бактерионосительства (например, стафилококконосительства) и хронических форм бактериальных инфекций.
- Сочетаются с другими препаратами, в том числе с антибиотиками. Их совместное применение ведет к быстрому выздоровлению от бактериальной инфекции.
- По совокупности описанных свойств бактериофаги применимы как основной препарат для лечения бактериальных инфекций у беременных, детей с рождения и людей пожилого возраста, а также в тех случаях, когда имеется полирезистентность микроорганизма к антибиотикам.
В лаборатории KDL предлагается 2 варианта посевов на флору с определением чувствительности выделенной культуры микроорганизма к препаратам бактериофагов и разным наборам антибиотиков в зависимости от ситуации пациента (выбирает врач), например:
Какие инфекции можно лечить бактериофагами:
- кожные, ожоговые и раневые инфекции;
- инфекции ЛОР органов;
- инфекции урогенитального тракта;
- отдельные инфекции желудочно-кишечного тракта.
Возбудителями этих инфекций могут быть такие бактерии, как золотистый стафилококк, синегнойная палочка, патогенные формы кишечной палочки, сальмонеллы, стрептококки.
В Новосибирском научном центре технологии персонализированного лечения бактериофагами в большой коллекции бактериофагов есть уникальные штаммы, способные бороться с недавно появившимися и уже получившими широкое распространение возбудителями больничных инфекций, такими как грамотрицательные бактерии Acinetobacter baumanii, Stenotrophomonas maltophilia и др.
Последние годы ознаменовались широкими исследованиями бактериофагов из-за нарастающей проблемы антибиотикорезистентности микроорганизмов, которые находят всё новые применения не только в терапии и профилактике, но и в биотехнологиях. Их очевидным практическим результатом должно стать возникновение нового мощного направления персонализированной медицины, а также создание целого спектра технологий в пищевой промышленности, ветеринарии, сельском хозяйстве и в производстве современных материалов. Мы ждем, что второе столетие исследований бактериофагов принесет не меньше открытий, чем первое.
Источник
Что такое бактериофаги
Поделиться:
Инфекционные заболевания были бичом человечества до того момента, как начали появляться антибактериальные препараты. Обычно новую эру связывают с именем Флеминга и пенициллином. Однако на десять лет раньше было сделано открытие, которое, возможно, еще пригодится всем нам в будущем.
Убить убийцу
Говорят, война — это всегда огромный скачок в развитии хирургии. На самом деле не только: военные действия нередко способствовали продвижению онкотерапии и терапии инфекционных болезней.
Читайте также:
Медицина в годы ВОВ
Во время 1-й мировой войны канадский врач Феликс Д’Эррель изучал вспышку дизентерии среди солдат-французов. Это неприятное кишечное заболевание вызывается бактериями рода Shigellа, которых легко можно выделить из стула больных.
Врач заинтересовался случаем одного солдата, который полностью выздоровел, причем раньше, чем появилось улучшение у других, кого начали лечить одновременно с ним. Взяв у него пробы стула, Д’Эррель не обнаружил бактерий — что-то загадочное убило их.
Исследователь отфильтровал свой «материал», пропустив его через фильтр с настолько мелкими порами, что через них не могла бы пройти ни одна бактерия или какие-нибудь частицы испражнений. В полученный раствор врач добавил готовую культуру бактерий, взятых от другого больного, высадил все это в чашку Петри и стал ждать.
Читайте также:
Профилактика и лечение острых кишечных инфекций
Через некоторое время начался рост бактериальной культуры, однако колонии были разорванными — словно что-то неведомое разъедало их изнутри. Взяв мазки из «пустых» областей, Д’Эррель добавил их в «хорошие», здоровые колонии шигелл — и в них тоже образовались пустоты.
Практика, обогнавшая теорию
Поскольку к этому моменту наш соотечественник Дмитрий Ивановский уже открыл вирусы, Д’Эррель предположил, что невидимый глазу убийца бактерий относится именно к ним. Понимая важность своего открытия, исследователь дал вирусам, поражающим бактерии, отдельное имя — бактериофаги.
Увидеть фагов удалось только после изобретения электронного микроскопа, а выяснить, чтó именно происходит при их контакте с бактериями, — и того позже. Поэтому в течение многих лет идея Д’Эрреля отвергалась значительной частью ученых, которым было трудно представить себе вирус, поражающий бактерию, но не причиняющий вреда человеку. К тому же опыты канадца удавалось повторить не всем и не всегда.
Однако врач, не дожидаясь никаких теоретических подтверждений своего открытия, перешел к практике. Он не мог, имея в руках лекарство, видеть умирающих людей — и принялся лечить солдат фаговым раствором. Правда, сперва Д’Эррель убедился в его безвредности традиционным для таких энтузиастов способом: сперва пил бактериофаг, затем впрыскивал себе под кожу.
Естественное против искусственного
Выяснив, что для человека бактериофаг совершенно не опасен, Д’Эррель вылечил многих пациентов, что принесло ему известность. Его исследования даже стали основой для художественного романа «Эрроусмит», позднее экранизированного Голливудом. Фаговые лекарства успешно производились и применялись — но уже в 40-х годах энтузиазм начал угасать.
Причиной этого стало открытие Флемингом пенициллина и появление большого числа антибиотиков. Врачи настороженно относились к идее лечения людей с помощью вирусов, а тут у них появилась альтернатива. Антибиотики — химические вещества, полученные искусственно, — не были живыми и казались медикам более надежными. Фармацевтические компании уловили настроения врачебного сообщества и, прекратив выпуск фагов, принялись множить антибиотики.
Бактериофаги сегодня
В наше время, когда антибиотикорезистентность является глобальной и очень опасной проблемой, бактериофаги снова заинтересовали ученых.
У них есть свои недостатки — например, не просто узкий, а суперузкий спектр действия: каждый фаг «умеет» убивать только один штамм бактерий — даже не вид, а штамм. Из-за этого, кстати, и проваливались регулярно попытки повторить эксперименты Д‘Эрреля: дизентерия в двух разных частях армии, идентичная по симптомам и течению, могла быть вызвана разными «вариантами» шигелл.
Однако эту проблему сегодня может решить постепенное распространение такого диагностического метода, как полимеразная цепная реакция (ПЦР), которая точно определит штамм бактерии.
Бактериофаги не могут проникать через стенку клетки, поэтому они пока бессильны против тех возбудителей, которые паразитируют внутриклеточно. «Пока» — потому что активные исследования в этом направлении, возможно, помогут фагам пробираться в самые потаенные места.
А вот среди плюсов бактериофагов с ходу можно выделить два: во-первых, они совершенно безвредны для человека, поскольку вообще никак не взаимодействуют с его организмом — только с бактериями.
И, во-вторых, бактерий они убивают не всех, а значит, не имеют традиционного недостатка применения антибиотиков — возникновения дисбиоза. Так что сегодня бактериофаги стали перспективной областью — и в каком-то смысле новой надеждой человечества.
Товар по теме: [product strict=»(бактериофаг»](бактериофаг)
Источник

 Читайте также:
Читайте также: 





