- Классификация дисперсных систем
- По агрегатному состоянию дисперсной фазы и дисперсионной среды
- По кинетическим свойствам дисперсной фазы
- По наличию взаимодействия частиц дисперсной фазы с молекулами дисперсионной среды
- По размеру частиц дисперсной фазы
- Коллоидные системы
- Дисперсные системы — классификация, виды и свойства
- Понятие и определение
- Классификация по агрегатному состоянию
- Существующие виды
- Взвеси и их особенности
- Коллоидные системы
- Высокомолекулярные вещества
- Ключевые свойства
Классификация дисперсных систем
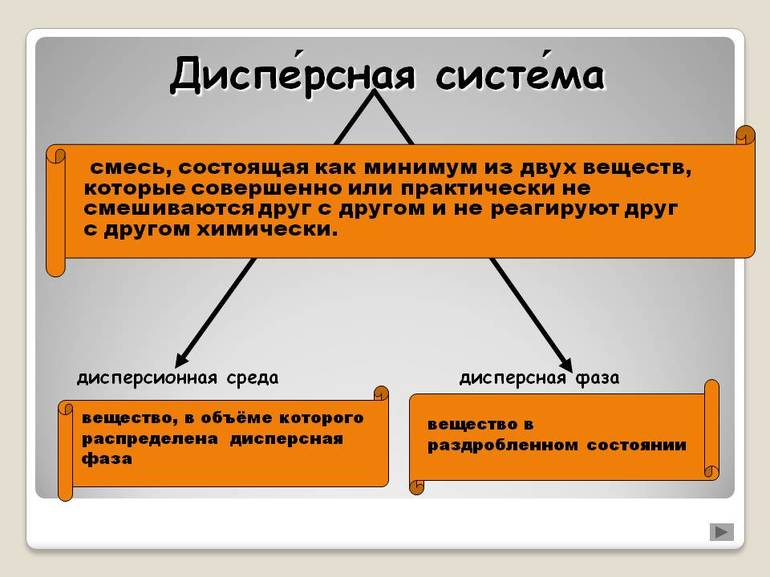
Дисперсные системы — это гетерогенные смеси двух и более составных частей, с высокоразвитой поверхностью раздела между ними.
Отличительная особенность дисперсных систем заключена в малом размере частиц при наличии значительной межфазной поверхности. Поэтому, наибольшее значение имеют свойства поверхности и происходящие на ней процессы, а не свойства частиц в целом.
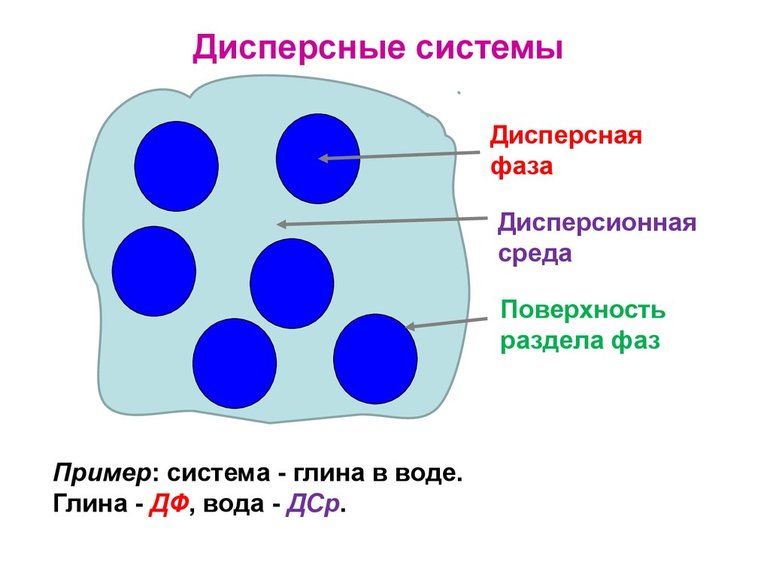
Итак, такие системы состоят из двух и более фаз, одна из которых находится в мелкораздробленном состоянии (дисперсная фаза) в среде другой фазы (дисперсионная среда).
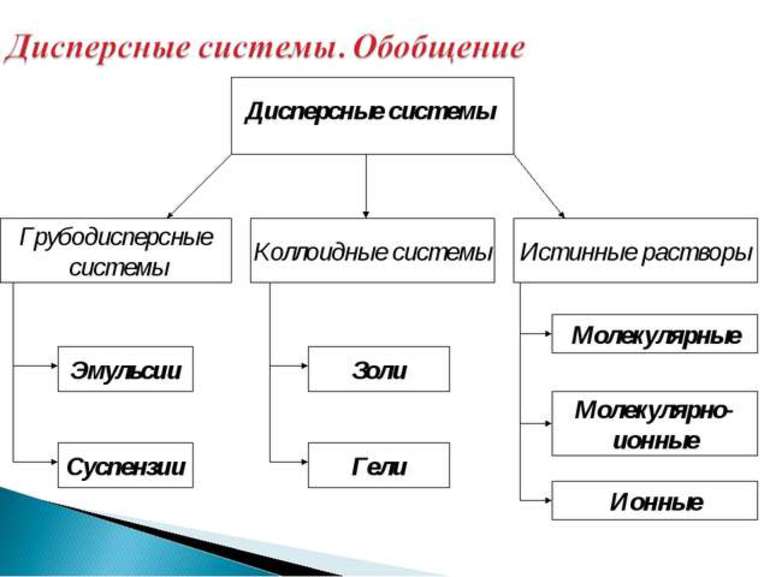
Классификация дисперсных систем разнообразна:
По агрегатному состоянию дисперсной фазы и дисперсионной среды
Для удобства, дисперсные системы принято условно обозначать через дробь, где в числителе указывают агрегатное состояние дисперсной фазы, а в числителе – дисперсионной среды:
| Дисперсная фаза | Дисперсионная среда | Условное обозначение | Название |
| Газ | Газ | Г/Г | Дисперсные системы не образуются |
| Газ | Жидкость | Г/Ж | Газовые эмульсии |
| Газ | Твердое вещество | Г/Т | Пористые тела |
| Жидкость | Газ | Ж/Г | Аэрозоли |
| Жидкость | Жидкость | Ж/Ж | Эмульсии |
| Жидкость | Твердое вещество | Ж/Т | Капиллярные системы |
| Твердое вещество | Газ | Т/Г | Порошки, пыли |
| Твердое вещество | Жидкость | Т/Ж | Суспензии и золи |
| Твердое вещество | Твердое вещество | Т/Т | Твердые гетерогенные системы |
По кинетическим свойствам дисперсной фазы
По наличию взаимодействия частиц дисперсной фазы с молекулами дисперсионной среды
— лиофильные – значительное взаимодействие частиц дисперсной фазы с молекулами дисперсионной среды. К ним могут относиться как природные, так и синтетические высокомолекулярные вещества.
— лиофобные – слабое взаимодействие частиц дисперсной фазы с молекулами дисперсионной среды. Это коллоидные растворы металлов, их оксидов, гидроксидов и солей.
По размеру частиц дисперсной фазы
-Грубодисперсные – размер частиц > 10 мкм;
-Среднедисперсные – размер частиц от 0,1 до 10 мкм;
-Высокодисперсные – размер частиц от 1 до 100 нм;
-Наноразмерные – размер частиц от 1 до 10 нм.
Предметом изучения коллоидной химии являются высокодисперсные или коллоидные системы (10-9-10-7 м).
Коллоидные системы
Коллоидные системы — это гетерогенные системы, в которых дисперсная фаза отделена от дисперсионной среды поверхностью раздела. При условии, что дисперсионная среда является жидкостью, а дисперсная фаза – твёрдым веществом, коллоидную систему называют золем; если дисперсная фаза является жидкостью, то коллоидную систему называют эмульсией.
Наиболее значимы коллоидные системы, в которых в качестве дисперсионной среды выступает вода. Они делятся на гидрофильные и гидрофобные коллоиды.
Гидрофильные коллоиды похожи на истинные растворы, которые являются однородными, гомогенными.
Гидрофобные коллоиды можно получить, если только они каким-то образом стабилизируются. Гидрофобные коллоиды можно стабилизировать при помощи адсорбции ионов на их поверхности. Адсорбированные ионы стабилизируют коллоид, взаимодействуя с водой. Укрупнение частиц и их слипание не происходит вследствие отталкивания частиц с адсорбированными на них ионов с одинаковым зарядом.
Гидрофобные коллоиды могут также стабилизироваться в присутствии других гидрофильных групп. Например, масло гидрофобно, и капельки масла, при смешивании с водой, отделяются от нее. При этом на поверхности воды образуется масляное пятно. Но такую систему можно стабилизировать, добавив в нее, например, стеарат натрия или другие поверхностно-активные вещества (ПАВ):
Молекула стеарата натрия состоит из двух частей: одна часть полярная или заряженая (гидрофильная), другая часть — неполярная (гидрофобная). При добавлении его к маслу, гидрофильные концы взаимодействуют с водой, а гидрофобные – с маслом.
Источник
Дисперсные системы — классификация, виды и свойства
Понятие и определение
Дисперсные системы представляют собой гетерогенные структуры, внутри которых одно или более веществ распределяются в другом. Они никак не контактируют друг с другом, химические или иные реакции полностью отсутствуют. Нет и смешения. Фактически каждый элемент является самостоятельным, и если его извлечь, он сохраняет свое изначальное состояние.
То вещество, которого больше всего в соединении, называется дисперсной средой, второстепенное — фазой. Частицы между собой не взаимодействуют, даже имеется некая прослойка, которая разделяет их. Поэтому системы являются гетерогенными или неоднородными.
Примеры дисперсных систем встречаются в природе постоянно — морская вода, почва, большинство продуктов питания и т. д. Они могут иметь любое агрегатное состояние. Иногда в среде находится сразу несколько фаз. Тогда их выделяют с помощью центрифуги или методом сепарирования.
Классификация по агрегатному состоянию
Классификация дисперсных систем осуществляется в соответствии с агрегатными состояниями вещества. Их имеется три вида: жидкое, твердое и газообразное. Поэтому разделение происходит на 9 основных категорий, примеры и описание которых можно посмотреть в таблице ниже.
| Вид | Среда | Фаза | Пример |
| Газ х 2 | Газ | Газ | Отсутствуют |
| Жидкость+газ | Газ | Жидкость | Туман, облако |
| Твердое тело (далее ТТ)+газ | Газ | ТТ | Дым, пыль |
| Газ+жидкость | Жидкость | Газ | Любая пена |
| Жидкость х 2 | Жидкость | Жидкость | Молоко |
| ТТ+жидкость | Жидкость | ТТ | Известь, ил |
| Газ+ТТ | ТТ | Газ | Пемза |
| Жидкость+твердое тело | ТТ | Жидкость | Грунт |
| ТТ+ТТ | ТТ | ТТ | Любые композиционные материалы, такие как бетон или цемент |
Каждый тип классификации, в свою очередь, имеет свое название. К примеру, газообразные соединения называются преимущественно аэрозолями, за редким исключением. Жидкие вещества — газовые эмульсии или суспензии. Взаимодействия, когда средой является твердое тело, определяются, как сплавы, капиллярные системы или пористые субстанции.
Существующие виды
Фазные частицы могут взаимодействовать между собой. При этом среда остается стабильной, химические реакции с ней отсутствуют. В зависимости от типа интерактивности, формируются виды дисперсных систем:
- Свободнодисперсные. Основное и главное свойство такой системы — текучесть. Поэтому сюда относят любые аэрозоли и растворы.
- Связнодисперсные. Это твердые или полутвердые системы. К ним относятся все концентрированные пасы или аморфные вещества.
Некоторые субстанции могут быть одновременно двумя видами. Отдельные золи при нормальной температуре являются достаточно текучими, чтобы определить их, как свободнодисперсные. Однако, если градус уменьшается, молекулы соединяются друг с другом сильнее, приобретая характеристики твердого тела. Поэтому переходят в связнодисперсную форму.
Взвеси и их особенности
Те дисперсные системы, фазы в которых можно легко определить невооруженным глазом, называются взвесями. Их характерная черта — непрозрачность. Если необходимо отделить среду и второстепенное вещество, можно воспользоваться рядовыми фильтрами, или процедурой отстаивания. Категорию разделяют на несколько видов:
- Эмульсии. В жидком агрегатном состоянии находится фаза и среда, они не взаимодействуют друг с другом и не растворяются. Многие получаются посредством гомогенизации. К ним относят большинство лекарственных препаратов или молоко.
- Суспензии. Здесь средой является жидкость, а фазой — твердая структура. Получают посредством пересыпания в жидкость порошка. Структура получается текучая, т. к. фаза крайне мелкая. Если оставлять структуру в неподвижном состоянии, выпадает осадок. Почти все строительные растворы относятся к категории.
- Аэрозоли. Взвесь в этом случае располагается в газе. Примеров множество, встречаются как в природе, так и в быту. Например, грозовые или обычные облака, туманы и некоторые виды осадков. Большинство химикатов, производимых для обработки сельскохозяйственных структур, тоже являются аэрозолями.
Взвеси важны в деятельности человека, равно как природных процессах. Почти все производство построено на применении растворов (удобрения, металлы, бумага и пр.). В окружающем мире естественные соединения с водой тоже встречаются постоянно, например, почвообразование или насыщение грунта полезными веществами. В жизнедеятельности всех живых существ они тоже принимают непосредственное участие.
Коллоидные системы
В отличие от взвесей, коллоидные системы невозможно разделить без использования современной техники или специальных препаратов. Без нужного инструмента и невооруженным глазом они выглядят, как однородная субстанция. Из-за этого определить дисперсность становится сложно. Подразделяются на два типа:
- Растворы или золи. Главное свойство — прозрачность. Чтобы определить наличие дисперсности, можно пропустить сквозь жидкость направленный пучок света. Тогда появляется «дорожка». Фазные частицы отражают лучи, образуя таковую. В качестве примера можно рассмотреть крахмал, белки, клей, в человеческом организме — лимфа или кровь. Чтобы отделить среду и второстепенное вещество, задействуется техника. Даже при продолжительном отстаивании осадка не образуется.
- Гели или студни. Это различные медицинские препараты, кондитерские кремы, желатин и многое другое. Многие изначально являются золями, затем переходят в новое состояние при понижении температуры. Отдельные преобразуются в эластичные твердые вещества, как пластилин или глина для лепки.
Если взвеси играют большую роль в природных процессах, то коллоидные системы являются неотъемлемой частью химии. Чаще всего они добываются посредством смешивания в специальном оборудовании. Без подобной структуры не удалось бы создать множество лекарственных препаратов, удобрений и других полезных материалов.
Высокомолекулярные вещества
Растворы высокомолекулярных веществ бывают двух видов: истинные и коллоидные. Все зависит от разных качеств, таких как тип фазы, среды, температуры и иных условий. У них есть ряд свойств:
- Процессы смешения происходят естественно и крайне медленно.
- Сначала происходит набухание, а затем смешивание.
- Полимерные и истинные растворы отличаются существенно. Те законы, которые характерны для одних (Рауля, Вант-Гоффа), несвойственны другим.
- По всей полученной субстанции свойства могут различаться из-за разного направления и/или размеров молекул.
- Повышенная вязкость.
Отдельные полимерные растворы образуются самопроизвольно. Когда процесс набухания образуется неорганическим способом, дисперсная система перестает существовать, поскольку фаза полностью растворяется в среде, образуется химическая реакция. Если же он органический, то появляется студень.
Ключевые свойства
Свойства дисперсных систем определяются по одному основному фактору — при их возникновении образуется четкая межфазная граница. Также появляется некоторое значение поверхностной энергии, которая не комбинируется, рассматривается в отдельном порядке по отношению к среде и фазе.
В природе и продуктах жизнедеятельности человека встречаются грубодисперсные системы. Здесь фазу и среду легко можно отличить под стандартным микроскопом, а то и вовсе невооруженным глазом. Но если рассматривать ее в целом, то она представляет собой сложную совокупность коллоидных веществ.
В свою очередь, тонкодисперсные системы являются настолько мелкими, что рассмотреть их можно только в специальный ультразвуковой микроскоп. В некоторых случаях даже при направленном в жидкость луче не появляется характерной «дорожки». Несмотря на существенные различия, свойства везде одинаковы. Они зависят от таких показателей, как:
- Степень (количество фаз).
- Молекулярный вес.
- Размеры частиц.
- Агрегатное состояние.
- Лиофобная/лиофильная группа.
В жизни человека рассматриваемые системы встречаются постоянно. Такое явление может быть как природным и естественным, так и выводимым в искусственном виде. Многочисленные лекарственные смеси, различные минеральные или химические удобрения, а также производственные процессы построены на дисперсности.
Источник