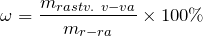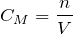- разработка урока «Дисперсные системы. Истенные растворы. Способы выражения концентрации растворов» план-конспект урока по химии (11 класс) на тему
- Скачать:
- Предварительный просмотр:
- Дисперсные системы и растворы
- Дисперсные системы и их виды
- Растворы
- Способы выражения концентрации растворов
- Растворимость
- Давление пара растворов
- Криоскопия. Эбулиоскопия. Второй закон Рауля
- Примеры решения задач
разработка урока «Дисперсные системы. Истенные растворы. Способы выражения концентрации растворов»
план-конспект урока по химии (11 класс) на тему
Тема: «Дисперсные системы. Истинные растворы. Способы выражения концентрации растворов».
Тип урока: урок новых знаний.
Цель:
- Образовательная:
- Сформулировать понятие дисперсной системы;
- Познакомить с классификацией дисперсной системы;
- Привлечь внимание учащихся к дисперсным системам большой практической значимости: суспензиям, эмульсиям, коллоидным растворам, истинным растворам, аэрозолям, пенам;
- Продолжить формирование общеучебных умений (осуществлять самоконтроль, сотрудничать).
- Развивающая:
- Развивать умение использовать химическую терминологию;
- Развивать мыслительные операции (анализ, синтез, установление причинно-следственных связей, выдвижение гипотезы, классификация, проведение аналогий, обобщение, умение доказывать, выделение главного);
- Развивать интересы, способности личности;
- Развивать умение проводить, наблюдать и описывать химический эксперимент;
- Совершенствовать коммуникативные умения учащихся в совместной деятельности (умение вести диалог, выслушивать оппонента, аргументировано обосновывать свою точку зрения) и информационно – познавательную компетентность учащихся.
- Воспитательная:
- Продолжить развитие познавательных интересов учащихся;
- Воспитывать культуру речи, трудолюбие, усидчивость;
- Продолжить формирование ответственного, творческого отношения к труду.
Ход урока:
І. Организационный момент.
ІІ. Проверка домашнего задания. Выполнить тест (индивидуальная работа)
1.Аллотропией называется:
Скачать:
| Вложение | Размер |
|---|---|
| disper_sistemi.doc | 69.5 КБ |
Предварительный просмотр:
Тема: «Дисперсные системы. Истинные растворы. Способы выражения концентрации растворов».
Тип урока: урок новых знаний.
- Образовательная:
- Сформулировать понятие дисперсной системы;
- Познакомить с классификацией дисперсной системы;
- Привлечь внимание учащихся к дисперсным системам большой практической значимости: суспензиям, эмульсиям, коллоидным растворам, истинным растворам, аэрозолям, пенам;
- Продолжить формирование общеучебных умений (осуществлять самоконтроль, сотрудничать).
- Развивающая:
- Развивать умение использовать химическую терминологию;
- Развивать мыслительные операции (анализ, синтез, установление причинно-следственных связей, выдвижение гипотезы, классификация, проведение аналогий, обобщение, умение доказывать, выделение главного);
- Развивать интересы, способности личности;
- Развивать умение проводить, наблюдать и описывать химический эксперимент;
- Совершенствовать коммуникативные умения учащихся в совместной деятельности (умение вести диалог, выслушивать оппонента, аргументировано обосновывать свою точку зрения) и информационно – познавательную компетентность учащихся.
- Воспитательная:
- Продолжить развитие познавательных интересов учащихся;
- Воспитывать культуру речи, трудолюбие, усидчивость;
- Продолжить формирование ответственного, творческого отношения к труду.
І. Организационный момент.
ІІ. Проверка домашнего задания. Выполнить тест ( индивидуальная работа )
- способность атомов элемента образовывать несколько сложных веществ с атомами другого элемента
- существование нескольких простых веществ, образованных атомами одного и того же элемента
- существование нескольких сложных веществ, молекулы которых имеют одинаковый состав, но различное химическое строение
- существование для атомов одного и того же элемента нескольких устойчивых изотопов
2.Два любых изомера:
- обладают одинаковой молярной массой
- содержат одинаковое число атомов всех элементов
- все приведенные выше утверждения верны
- имеют одинаковый качественный состав
3.Исключите лишний элемент с точки зрения возможности образования им аллотропных модификаций.
1 вещества, имеющие одинаковый состав,
но различное химическое строение А) гомологи
2 вещества, имеющие сходное Б) изотопы
строение и свойства, состав В) изобаты
которых отличается на одну Г) изомеры
или несколько групп СН 2 Д) гибридизация
3 атомы, имеющие одинаковое число протонов, но различное число нейтронов в ядре
4 атомы, имеющие различное число протонов в ядре, но одинаковое массовое число
5 процесс выравнивания орбиталей по форме и энергии
Ребята Сдайте свой тест.
ІІІ. Изучение нового материала. (Звучит песня Н. Добрынина «Синий туман», на демонстрационном столе коллекция дисперсных систем, используемых человеком в повседневной жизни)
— Как вы думаете, ребята, имеет ли прозвучавшая песня какое-нибудь отношение к теме сегодняшнего урока? Перед вами на столе находится коллекция дисперсных систем, мне бы хотелось чтобы вы попытались классифицировать эти системы на группы (ребята пытаются выполнить задание). ( работа в парах )
Мы живем в мире дисперсных систем. Посмотрите внимательно вокруг себя. Туман, пыль, снег – все это не только случайные неприятности, но и примеры дисперсных систем.
Большинство веществ окружающего нас мира, составляющих ткани живых организмов, гидросферу, земную кору и недра, космическое пространство часто представляют собой вещества в раздробленном, или, как говорят, дисперсном состоянии. Диспергирование означает раздробление.
— Как вы думаете какова цель сегодняшнего урока? (ответы детей)
Итак, цель нашего сегодняшнего урока – составить представление о дисперсных системах, их месте в природе и жизни человека, научиться характеризовать их свойства, объяснять причины большей или меньшей устойчивости.
— Но, что же все таки такое, дисперсная система?
Дисперсная система – это смесь, состоящая как минимум из двух веществ, которые совершенно или практически не смешиваются друг с другом и не реагируют друг с другом химически.
Дисперсная система
Дисперсионная среда Дисперсная фаза
В дисперсионной среде распределены частицы дисперсной фазы, которые могут быть твердыми, капельками жидкости или пузырьками газа. Дисперсная фаза мелко распределена в дисперсионной среде. (запись в тетради) . Наибольшее значение в практике имеют ДС, в которых средой является вода или другие жидкости, о них мы и поговорим подробнее.
Истинные растворы, в которых вещество раздроблено до мельчайших частиц (молекул или ионов) размерами менее 1нм.
Тонкодисперсные системы с размерами частиц 1 – 100 нм также называют коллоидными системами (растворами) или золями (интерактивная схема). В зависимости от природы дисперсионной среды, коллоидные системы подразделяют на золи и гели.
— Коллоидные системы (коллоиды, др. греч.) – дисперсные системы, промежуточные между истинными растворами и грубодисперсными системами – взвесями и эмульсиями. Коллоидные частицы не видны в обычный микроскоп, они крупнее молекул, но простым глазом их увидеть все же нельзя, т.е. по виду растворы не различимы. Но такая необходимость возникает в практической деятельности. Как же отличить коллоидный раствор от истинного?
— Некоторые золи при осаждении увлекают за собой жидкую фазу (иногда даже полностью), образуя при этом с водой общую массу. Подобные осадки называются гелями или студнями. Чтобы было легче представить себе, что такое гель, приведем примеры бытовых гелей – желе, мармелад, яичный белок, студень (интерактивная схема)
Гелями могут быть дисперсные системы с жидкой и газообразной дисперсионной средой. Гели обладают одновременно свойствами жидкости и твердого тела. Состояние жидкости в гелях непрочное. Они сравнительно легко изменяют свой объем при поглощении или отдачи дисперсионной среды. С течением времени из геля выделяется жидкая фаза и объем геля уменьшается. Это явление называется синерезисом, или старением геля (запись в тетради, интерактивная схема).
— А вот если у человека этот процесс затруднен (переход фибриногена в фибрин), на какое заболевание он может указывать? (гемофилия). Из курса биологии вам известно, что носителем гена гемофилии является….(женщина, а заболевают мужчины) . А, вы, знаете каких-нибудь выдающихся личностей у которых встречалось это заболевание? (Династия Романовых, которая царствовала более 300 лет, страдала этим заболеванием).
Рубиновые стекла, аморфные минералы, образовавшиеся в водных растворах и содержащие переменное количество воды, относятся к тв. гелям. Драгоценный камень агат – типичный минеральный гель, встречающийся в отложениях теплых источников, образуется также в процессе синерезиса.
— А сейчас давайте маленько отдохнем и отгадаем небольшие загадки касающиеся ДС.
1. Превратите крупную австралийскую птицу – страуса, в жидкость со взвешенными в ней частицами другой жидкости. (Эму — эмульсия)э
2. Как превратить атолл Роз в газ со взвешенными в нем мельчайшими частицами. (Роз – аэрозоль).
3. Название, какого раствора начинается с самой низшей школьной оценки? (Кол — коллоидный).
4. Из названий степного грызуна и города – областного центра черноземной зоны Росси составьте название жидкости со взвешенными в ней тв. частицами. (Суслик, Пенза — суспензия).
— Давайте выполним небольшой лабораторный опыт. У вас на столах находятся карточки- путеводители (приложение 2), которыми вы должны пользоваться при выполнении опыта. Не забываем о ТБ. После окончания работы сделайте вывод.
— Чем же обусловлено многообразие дисперсных систем? (Многообразие ДС обусловлено тем, что образующие их среды могут находиться в любом из трех агрегатных состояний).
Физ. митунка: зарядка для глаз
— А теперь давайте послушаем сообщение, которое подготовил……… на тему «Коллоидные растворы в нашей жизни. Их роль и значение».
— У ДС есть еще одно важной свойство – в-во в дисперсном состоянии стремиться поглотить другие в-ва. Подумайте и назовите пример всем известного в-ва из домашней или нашей школьной аптечки, которое в мелко дисперсном состоянии используется при отравлениях (активированный уголь)
— как мы уже выяснили, область применения весьма обширна, поэтому очень важно в целях получения высоких урожаев и защиты от вредителей нужно уметь приготавливать растворы соответствующих веществ.
Вы уже знаете как приготовить раствор с определенной массовой долей растворенного вещества, и теперь мы узнаем как приготовим раствор с определенной молярной концентрацией.
Что же такое молярная концентрация? (найти определение в учебнике стр. 36.) (индивидуальная работа)
Формула по которой определяют:
с м (х) = v (х)/ V (р-ра), измеряется в – моль/л
Пример задача №1 стр 38
— А теперь давайте расположим данные вещества в таблице: ( работа в группах )
Лак для волос, дым, минеральная вода, цветное стекло, мороженное, молоко, туман, смог, хлеб, сливочное масло, шоколадная паста, минералы, кровь, почва, жемчуг.
Источник
Дисперсные системы и растворы
Дисперсные системы и их виды
Существует классификация дисперсных систем по размеру частиц дисперсной фазы. Выделяют, молекулярно-ионные ( 100 нм) системы.
Различают гомогенные и гетерогенные дисперсные системы. Гомогенные системы по-другому называют истинными растворами.
Растворы
По агрегатному состоянию растворы делят на газообразные (воздух), жидкие, твердые (сплавы). В жидких растворах существует понятие растворителя и растворенного вещества. В большинстве случаев растворителем служит вода, однако это могут быть и неводные растворители (этанол, гексан, хлороформ).
Способы выражения концентрации растворов
Для выражения концентрации растворов используют: массовую долю растворенного вещества (
Молярная концентрация (СМ, моль/л) показывает, сколько моль растворенного вещества содержится в одном литре раствора. Растворыс концентрацией 0,1 моль/л называют децимолярными, 0,01 моль/л – сантимолярными, а с концентрацией 0,001 моль/л – миллимолярными.
Нормальная концентрация (СН, моль-экв/л) показывает число эквивалентов растворенного вещества в одном литре раствора.
Моляльная концентрация (Сm, моль/1кг H2O) – число моль растворенного вещества, приходящееся на 1 кг растворителя, т.е. на 1000 г воды.
Мольная доля растворенного вещества (N) – это отношение числа моль растворенного вещества к числу моль раствора. Для газовых растворов мольная доля вещества совпадает с объемной долей ( φ).
Растворимость
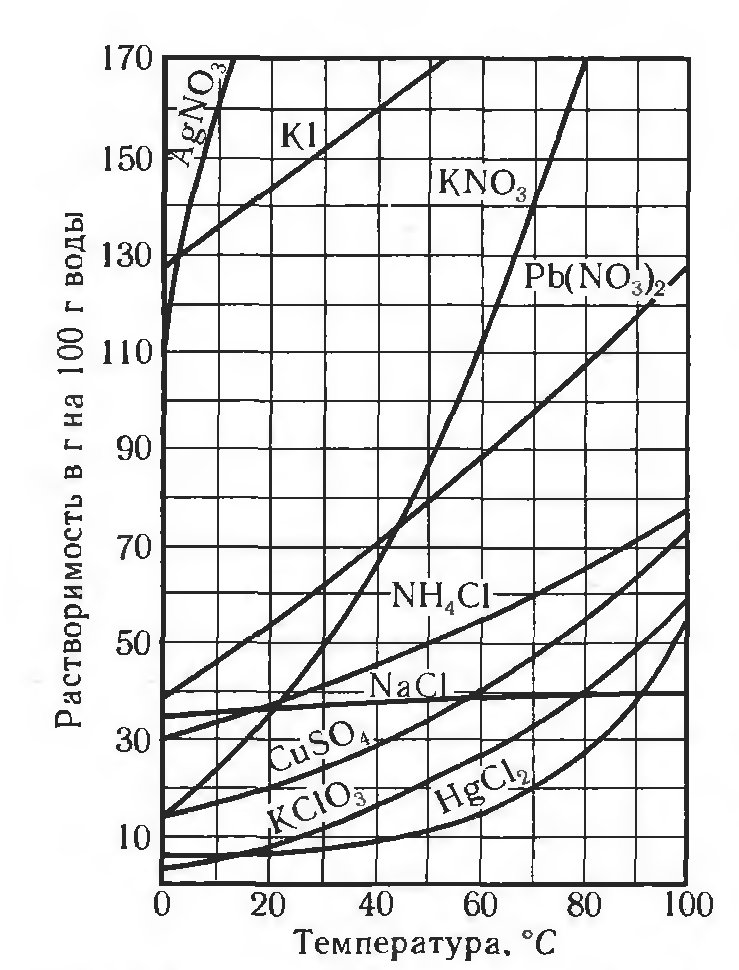
По растворимости растворы и вещества делят на 3 группы: хорошо растворимые (сахар), малорастворимые (бензол, гипс) и практически нерастворимые (стекло, золото, серебро). Абсолютно нерастворимых веществ в воде нет, нет приборов, с помощью которых возможно вычислить количества вещества, которое растворилось. Растворимость зависит от температуры (рис. 1), природы вещества и давления (для газов). При повышении температуры, растворимость вещества увеличивается.
Рис. 1. Пример зависимости некоторых солей в воде от температуры
С понятием растворимости тесно связано понятие насыщенного раствора, поскольку растворимость характеризует массу растворенного вещества в насыщенном растворе. Пока вещество способно растворяться раствор называют ненасыщенным, если вещество перестает растворяться – насыщенным; на некоторое время можно создать пересыщенный раствор.
Давление пара растворов
Пар, находящийся в равновесии с жидкостью называется насыщенным. При заданной температуре давление насыщенного пара над каждой жидкостью – величина постоянная. Поэтому каждой жидкости присуще давление насыщенного пара. Рассмотрим это явление на следующем примере: раствор неэлектролита (сахарозы) в воде – молекулы сахарозы значительно больше молекул воды. Давление насыщенного пара в растворе создает растворитель. Если сравнить между собой давление растворителя и давление растворителя над раствором при одинаковой температуре, то в растворе число молекул, перешедших в пар над раствором меньше, чем в самом растворе. Отсюда следует, что давление насыщенного пара растворителя над раствором всегда ниже, чем над чистым растворителем при той же температуре.
Если обозначить давление насыщенного пара растворителя над чистым растворителем p0, а над раствором – p, то относительное понижение давления пара над раствором будет представлять собой (p0-p)/p0.
На основании этого Ф.М. Рауль вывел закон: относительное понижение насыщенного пара растворителя над раствором равно молярной доле растворенного вещества : (p0-p)/p0 = N (молярная доля растворенного вещества).
Криоскопия. Эбулиоскопия. Второй закон Рауля
Понятия криоскопии и эбулиоскопии тесно связаны с температурами замерзания и кипения растворов, соответственно. Так, температура кипения и кристаллизация растворов зависят от давления пара над раствором. Любая жидкость кипит при той температуре, при которой давление ее насыщенного пара достигает внешнего (атмосферного давления).
При замерзании кристаллизация начинается при той температуре, при которой давление насыщенного пара над жидкой фазой равно давлению насыщенного пара над твердой фазой. Отсюда – второй закон Рауля: понижение температуры кристаллизации и повышение температуры кипения раствора пропорционально концентрациям растворенного вещества. Математическое выражение этого закона:
где К и Е криоскопическая и эбулиоскопическая константы, зависящие от природы растворителя.
Примеры решения задач
| Задание | Какое количество воды и 80%-го раствора уксусной кислоты следует взять для получения 200 г 8%-го раствора? |
| Решение | Записываем формулу для нахождения массовой доли: |
Пусть масса 80% раствора уксусной кислоты равна х г. Найдем массу растворенного в нем вещества:
mр.в-ва(CH3COOH) =mр-ра × 
Найдем массу растворенного вещества в растворе 8%-й уксусной кислоты:
Масса 80% раствора уксусной кислоты равна 20 (г).
Найдем необходимое количество воды:
m(H2O) = 200 (г) – 20 (г) = 180 (г)
| Задание | Смешали 200 г воды и 50 г гидроксида натрия. Определите массовую долю гидроксида натрия в растворе. |
| Решение | Записываем формулу для нахождения массовой доли: |
Найдем массу раствора гидроксида натрия:
mр-ра (NaOH) = 200 +50 = 250 (г)
Найдем массовую долю гидроксида натрия:

 (NaOH)=20%
(NaOH)=20%| Задание | Определите массу 10%-го раствора карбоната натрия, которую нужно добавить к 1020 г 2%-го раствора, чтобы получить 3%-й раствор. |
| Решение | Записываем формулу для нахождения массовой доли: |
Найдем массу растворенного карбоната натрия в его 2%-м р-ре:
m(Na2CO3) в 2%-м р-ре = mр-ра(Na2СO3)2% × 
m(Na2CO3) в 2%-м р-ре = 1020 × 0,02 = 20,4г
Найдем массу растворенного карбоната натрия в его 10%-м р-ре:
Тогда масса 3%-го раствора карбоната натрия:
А масса растворенного карбоната натрия в нем:
m(Na2CO3) в 3%-м р-ре = (х + 1020) × 0,03 (г)
Найдем массу растворенного карбоната натрия в конечном растворе:
Источник