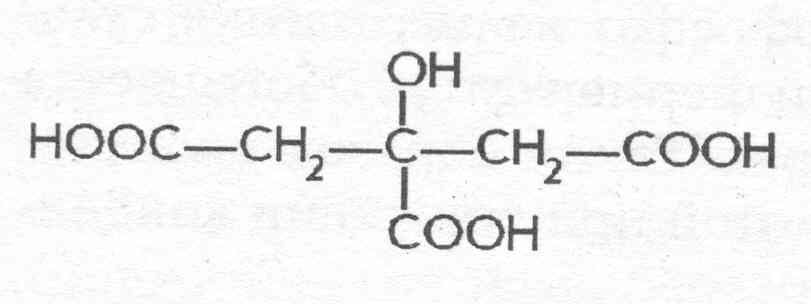О.В. Мосин
Лимонную кислоту широко используют в пищевой, медицинской, фармацевтической, лакокрасочной промышленности и в некоторых других отраслях народного хозяйства.
Около 60 лет назад лимонную кислоту выделяли преимущественно из плодов цитрусовых растений. Теперь же основную массу ее производят с помощью определенных штаммов плесневого гриба Aspergillus niger. В настоящее время ведущими производителями лимонной кислоты являются КНР, США, Франция, Россия и некоторые другие страны. Ранее, начиная с 1917 г., производство лимонной кислоты было основано на поверхностном культивировании микроба-продуцента; в 1938-1942 гг. освоено также глубинное культивирование в герметичных ферментаторах. Благодаря этому удалось механизировать и автоматизировать процесс, эффективнее использовать производственные площади и снизить себестоимость целевого продукта, сократить общую продолжительность технологического цикла, облегчить поддержание асептичности в производственных условиях.
Ныне в производстве применяют селекционированные штаммы A. niger, дающие выход лимонной кислоты 98-99% в расчете на потребленную сахарозу и обладающие повышенной осмотолерантностью (при начальных концентрациях сахара в питательной среде порядка 12%).
Лимонная кислота, как трехосновная оксикарбоковая кислота, наряду с глюконовой, фумаровой и другими, является интермедиатом метаболизма в цикле трикарбоновых кислот, когда имеет место неполное окисление соединений углерода в аэробных условиях. Ее сверхсинтез возможен при лимитировании гриба — продуцента по железу и фосфору, при одновременном избытке в среде источника углерода и при низких значениях рН. Лимонная кислота накапливается вначале в клетках продуцента, а затем выделяется в культуральную среду.
Вышеперечисленные факторы ингибируют такие ферменты, как аконитат-гидратазу, изоцитратдегидрогеназу и, возможно, -кетоглутаратдегидрогеназу. Поэтому не происходит полного метаболизма лимонной кислоты в ЦТК и ее можно получать в достаточно больших количествах с коммерческими целями.
Поскольку основным сырьем для производства лимонной кислоты является меласса, в которой содержится много железа, то на стадии предферментации необходимо его осадить с помощью желтой кровяной соли — Kd [Fe(CN6)J. К тому же доказано, что эта соль и лимонная кислота в клетках выступают ингибиторами изоцитратдегидрогеназы.
Известны два способа ферментации Aniger — поверхностный и глубинный. Первый из них реализуют на предприятиях малой и средней мощности в виде жидкофазной ферментации на жидкой среде (например, в ряде стран Европы и Америки) и в виде твердофазной ферментации (например, в Японии) на уплотненной среде. Технологическая схема жидкофазной ферментации представлена по Р. Я. Карклиныпу и А. К. Пробоку (1972) на рис. 1.
В отдельном цехе осуществляют наработку спор (конидий) гриба в виде трехстадийной схемы. В первую стадию A.niger выращивают на скошенной агаризованной среде (например, на сусло-агаре) в пробирках, во вторую и третью стадии его размножают на плотной или жидкой среде соответственно в колбах Эрленмейера или в алюминиевых кюветах площадью 8,5-12 дм2 и с высотой бортиков от 7 до 20 см. Продолжительность каждой стадии — от 2 до 4 суток при температуре 32?С. При образовании и созревании конидий вначале бесцветный мицелий становится затем черным; конидии собирают по принципу аспирации (по лат. aspiratio — вдыхание, надувание) специальным вакуумным насосом, подсушивают в термокамере при 28-30?С, смешивают со стерильным активированным углем (1:2), фасуют в стерильные флаконы (колбы) и хранят в течение от полутора до двух лет. С 10 дм2 питательной среды в кюветах можно получить до 4-5 г сухих конидий. Подобный посевной материал может быть самостоятельным коммерческим продуктом, поставляемым на заводы лимонной кислоты.
Поверхностный, способ жидкофазной ферментации A.niger для промышленного производства лимонной кислоты реализуют в «бродильных камерах», где размещают на стеллажах названные выше кюветы (8-10 штук на один стеллаж) одну над другой. На дне каждой кюветы имеется сливной штуцер. «Бродильные камеры» оборудованы приточно-вытяжной вентиляцией, обеспечивающей равномерный приток стерильного воздуха заданной температуры и влажности (3-4 м3/м2 мицелия x ч -1). Температура в камерах поддерживается на уровне 34-36?С, высота питающего слоя жидкой мелассной среды 6-12 см. Максимальное тепловыделение (500-550 кДж/м2 x ч) имеет место к 5 суткам; исходная концентрация Сахаров в питательной среде в среднем порядка 12%; начальное значение рН 6,8—7,0 снижается до 4,5 в течение первых трех суток и до 3,0 — к концу процесса (8-9 сутки). Максимальное кислото-образование в таких условиях происходит на 5-6 сутки (100-105 г/м2 пленки гриба-ч -1, а затем стабильно удерживается на уровне 50-60 г/м2x ч1.
Из трех вариантов проведения технологического процесса (периодический, или бессменный; сменный и доливной) наилучшим оценивают доливной, когда через б-7 суток от начала процесса ферментации (концентрация сахара снижается до 3-4%) подливают стерильный раствор мелассы без питательных солей — 30-35% начального объема (не забывать рационально использовать объем кювет при первоначальном заполнении питательной средой с учетом ее испарения). Таким путем добиваются продления цикла ферментации до 12 суток, а с этим на 30-35% возрастает количество перерабатываемой среды для получения целевого продукта. При сменном (одно- и многосменном) методе кулътуралъную жидкость в конце ферментации сливают из-под пленки, пленку снизу промывают стерильной водой и под нее же заливают свежую стерильную питательную среду, содержащую только углевод и лишенную минеральных солей. Ферментацию продолжают еще 4-6 суток.
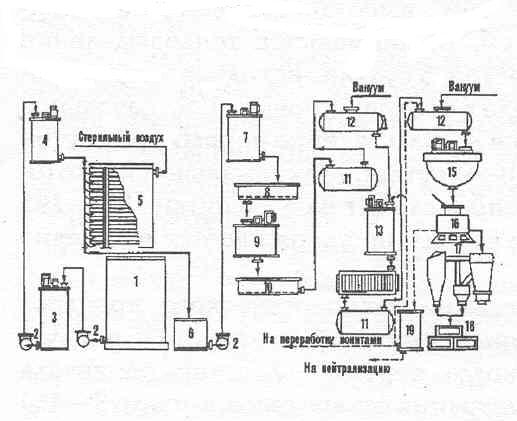
В собранной культуральной жидкости содержится смесь органических кислот — лимонная, глюконовая, щавелевая и неиспользованный сахар в примерном соотношении 45-50:3:1:7, то есть лимонная кислота составляет от 80 до 90%. Ее выделяют химическим путем — добавляют к нагретой до 100?С культуральной жидкости известковое молоко — Са(ОН)2 или мел — СаСО3, доводя рН до 6,8-7,0; это количество составляет примерно 2,5-3%; трехзамещённый кальция цитрат, хуже растворимый в горячей воде, чем в холодной, выпадает в осадок вместе с кальция оксалатом (кальция глюконат остается в растворе); осадок отфильтровывают, промывают горячей водой и гидролизуют серной кислотой. Свободная лимонная кислота остается в растворе, а негидролизованный кальция оксалат и образовавшийся гипс — CaSO4 остаются в осадке. Раствор лимонной кислоты очищают, подвергают вакуум-упариванию и кристаллизуют. Кристаллы кислоты высушивают и фасуют (Рис.1).
Рис. 1. Технологическая схема получения лимонной кислоты из мелассы поверхностным способом (жидкофазная ферментация): 1 — цистерна для мелассы, 2 — центробежные насосы, 3 — реактор для разбавления мелассы, 4 — стерилизатор, 5 — бродильная камера, 6 — сборник сбраживаемых растворов, 7 — нейтрализатор, 8, 10 — нутч-филь-тры, 9 — расщепитель, 11 — сбор-ник-монтежю, 12 — вакуум-аппарат, 13-дисольвер, 14 — фильтр-пресс, 15 — кристаллизатор, 16 — приемник, 17 — сушилка, 18 — готовая продукция, 19 — сборник фильтрата.
Мицелий продуцента либо используют для выделения фермента пектиназы, либо высушивают и поставляют на корм скоту и домашней птице (желательно — в обезвреженном — убитом виде); наконец, он может быть использован, как источник флавинов.
Твердофазная ферментация на уплотненных средах для получения лимонной кислоты — наиболее простой способ из всех известных, ферментацию определенного штамма A.niger, резистентного к высоким концентрациям металлов (особенно — железа), содержащихся в семенах злаковых растений, проводят на увлажненных отрубях риса или пшеницы, находящихся в кюветах. Условия биосинтеза кислот при этом аналогичны условиям на агаризованных или в жидких питательных средах. После окончания процесса отруби экстрагируют водой, куда переходят кислоты, а затем выделяют цитрат кальция и чистую лимонную кислоту согласно схеме, изложенной выше.
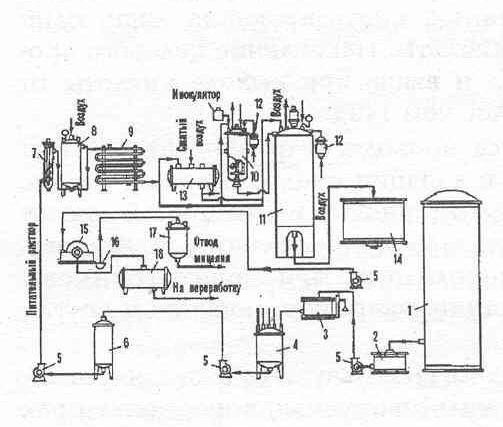
Общая технологическая схема получения лимонной кислоты при глубинной ферментации A.niger приведена на рис. 2.
Рис. 2. Технологическая схема получения лимонной кислоты при глубинной ферментации продуцента: 1 — емкость с мелассой, 2 — приемник мелассы, 3 — весы, 4 — варочный котел, 5 — центробежный насос, 6 — промежуточная емкость, 7 — стерилизующая колонка, 8 — выдержива-тель,9—холодильник, 10 — посевной аппарат, 11 — головной ферментатор, 12 — стерилизующие фильтры, 13 — емкость для хранения мелассы, 14 — промежуточный сборник, 15 — барабанный вакуум-фильтр, 16 — приемник для мицелия, 17 — вакуум-сборник для мицелия, 18 — вакуум-сборник фильтрата культуральной жидкости,
Согласно подсчетам глубинный метод экономически выгоден в тех случаях, когда мощность завода превышает 2,5 тыс. тонн лимонной кислоты в год, в противном случае поверхностный метод оказывается предпочтительнее из-за меньших энергозатрат и себестоимости продукции.
Лимонную кислоту можно получать из н-парафинов с помощью дрожжевых организмов рода Candida — C.lipolytica, C.tropicalis, C.parapsilosis, C.oleophila, C.guilliermondii, C.zeylanoides. Наиболее активными из них являются дрожжи C.lipolytica. К тому же другие виды (кроме C.oleophila) относят к разряду условно патогенных.
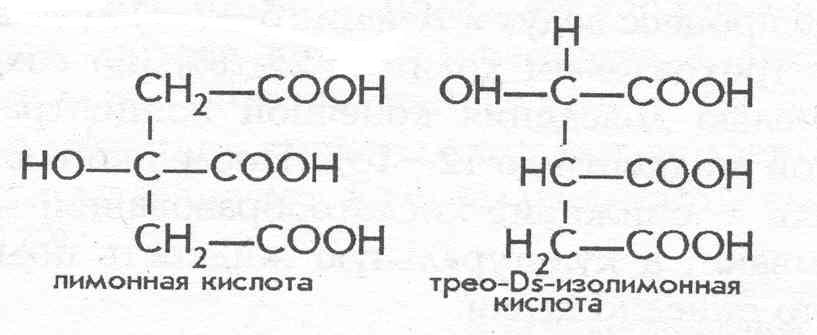
Кроме лимонной дрожжи образуют на н-алканах Tpeo-Ds-изо-лимонную, представляющую собою геометрический изомер лимонной кислоты.
При лимитировании продуцента в азоте, фосфоре, сере и магнии, но при избытке в среде парафина, можно наблюдать сверхсинтез равных количеств обоих изомеров. Методами генетики и селекции получены мутанты, синтезирующие лишь один какой-либо изомер лимонной кислоты. Накопление целевого продукта может достигать 200 г/л и выше при выходе кислоты от использованного парафина более чем 140%.
Культивирование C.lipolytica проводят в ферментаторах при интенсивных перемешивании и аэрации среды. В нашей стране отработаны методы получения лимонной и изолимонной кислот на н-алканах. Большая заслуга в этом принадлежит Т. В. финогеновой. Получаемые технические соли цитраты и изоцитраты имеют важное значение при изготовлении, например, моющих и других веществ.
Биотехнология/под ред. И. Хиггинса, Д. Беста, Дж. Джонса/перевод с английского/под ред. А. А. Баева. — М.: Мир, 1988. — 479 с.
Биотехнология микробного синтеза/под ред. М. Е. Бекера — Рига: Зинатне, 1980. — 350 с.
Воробьев Л. И. Техническая микробиология. — М.: Высшая школа, 1987. — 94 с.
Д е б а б о в В. Г., Лившиц В. А. Биотехнология. — М.: Высшая школа, 1988.
Кн. 2. Современные методы создания промышленных штаммов микроорганизмов. 1988. — 208 с.
Промышленная микробиология и успехи генетической инженерии. Сборник: перевод с английского под ред. Г. К- Скрябина. — М.: Мир, 1984. — 172 с.
Смирнов В. А. Пищевые кислоты. — М.: Легкая и пищевая промышленность, 1983. — 240 с.
Basic biotechnology Ed. by John Bu’Lock and Bjern Kristiansen.- Acad. Press, London, Orlando San Diego, New York, Austin, Boston, Sydney Tokio, Toronto, 1987. — 561 p.
Источник
Способ биосинтеза лимонной кислоты
Изобретение относится к биотехнологическому производству пищевых кислот. Биосинтез лимонной кислоты проводят при условии циклической подачи источника углерода в питательную среду, содержащую источники азота и минеральных веществ в условиях аэрации. Объем подачи источника углерода в цикле зависит от скорости роста биомассы и/или скорости биосинтеза лимонной кислоты. Длительность одного цикла 0,5-2 ч. В первом цикле обычно вводят 10-15% источника углерода, далее — в зависимости от вышеуказанных параметров процесса. Технический результат заключается в уменьшении удельного расхода питательной среды при уменьшении ее себестоимости. 5 з.п. ф-лы.
Изобретение относится к области биотехнологического производства пищевых кислот, в частности лимонной кислоты, и может быть применено на биотехнологических предприятиях.
Лимонная кислота в настоящее время является одной из наиболее используемых оксикислот. Она широко используется в пищевой, легкой, электронной, радиотехнической и других видах промышленности. Лимонная кислота может быть получена как химическим, так и биохимическим путем. Общеизвестно, что химический синтез лимонной кислоты (как из органического, так и неорганического сырья) экономически не целесообразен как из-за высокой стоимости и сезонности сырья, так и из-за нетехнологичности способов синтеза. В настоящее время практически всю лимонную кислоту получают биотехнологическим способом, используя в качестве сырья отходы сахарного производства и продукты переработки нефти. Известен, в частности, способ синтеза лимонной кислоты (US, патент N 4389484, кл. C 12 P 7/48, 1983), согласно которому на питательной среде, содержащей источники углерода, азота и минеральных веществ, выращивают дрожжи Candida в условиях аэрации и перемешивания с последующим выделением лимонной кислоты традиционным путем. Недостатком известного способа следует признать излишний расход питательной среды, в частности источника углерода, и, следовательно, повышение себестоимости лимонной кислоты при уменьшении процента выхода лимонной кислоты.
Техническая задача, на решение которой направлено предлагаемое изобретение, состоит в повышении удельного выхода лимонной кислоты.
Технический результат, получаемый в результате реализации изобретения, состоит в уменьшении удельного расхода питательной среды при уменьшении ее себестоимости.
Способ биосинтеза лимонной кислоты согласно предлагаемому изобретению включает в себя выращивание микроорганизмов на питательной среде, содержащей источники углерода, азота и минеральных веществ в условиях аэрации и перемешивания с последующим выделением лимонной кислоты, причем источники азота и минеральных веществ вводят в зону реакции единовременно, а источник углерода вводят в зону реакции циклически, при этом количество источника углерода, подаваемое в течение одного цикла зависит от скорости образования биомассы и/или скорости синтеза лимонной кислоты. Предпочтительно биосинтез лимонной кислоты проводят при содержании репродуцирующих веществ примерно 1,0%. Время цикла зависит от используемой культуры микроорганизмов, вида источников углерода и обычно составляет 1 — 2 ч. Как следует из опыта работы на первых циклах предпочтительно при определении объема подаваемого источника углерода учитывать скорость роста биомассы, а для последующих циклов предпочтительно учитывать скорость синтеза лимонной кислоты. Преимущественно скорость роста биомассы следует учитывать на первых трех циклах. Предпочтительно в первом цикле ввести 5 — 10% от необходимого объема источника углерода.
Заявитель отмечает, что совокупность признаков, введенная им в независимый пункт формулы изобретения, необходима и достаточна для получения указанного технического результата. Признаки, введенные заявителем в зависимые пункты формулы изобретения, развивают и дополняют признаки, введенные в независимый пункт формулы, незначительно усиливая технический результат. Признаки, введенные заявителем в зависимые пункты формулы изобретения, характеризуют некоторые варианты реализации изобретения, не исчерпывая при этом всех возможных вариантов.
Пример 1. В посевном ферментере обычным образом выращивают культуру мицелия Aspergillus Niger. В основной ферментатор подают стерилизованный концентрат минеральных веществ в виде концентрированных растворов FeSO4, ZnSO4, (NH4)2SO4, KH2PO4, MgSO4 

Пример 2. В посевном ферментере обычным образом выращивают культуру дрожжей Candida lipolytica ВКПМ — 2706 и при этом время цикла составляло 0,5 ч, остаточное количество сахара не превышало 0,5%. Выход лимонной кислоты составил 92%.
Приведенные примеры не ограничивают область применения способа.
1. Способ биосинтеза лимонной кислоты, включающий проведение ферментации на питательной среде, содержащей источники углерода, азота и питательных минеральных веществ, в условиях аэрации и перемешивания с последующим выделением лимонной кислоты, отличающийся тем, что источник углерода подают в процесс ферментации циклически, причем количество источника углерода, подаваемое за каждый цикл, меняют в зависимости от скорости образования биомассы и/или от скорости биосинтеза лимонной кислоты.
2. Способ по п.1, отличающийся тем, что процесс ведут при остаточной концентрации редуцирующих веществ в среде 0,5 — 1,0%.
3. Способ по п.1, отличающийся тем, что длительность цикла составляет 0,5 — 2 ч.
4. Способ по п.1, отличающийся тем, что расход источника определяют в первых циклах по скорости образования биомассы.
5. Способ по п. 4, отличающийся тем, что расход источника углерода по скорости образования биомассы определяют на первых трех циклах.
6. Способ по п.1, отличающийся тем, что в первом цикле вводят 10 — 15% источника углерода.
Источник