- Способы получения аренов
- Получение аренов
- 1. Реакция Вюрца-Фиттига
- 2. Дегидроциклизация алканов
- 3. Дегидрирование циклоалканов
- 4. Декарбоксилирование солей бензойной кислоты
- 5. Алкилирование бензола и его гомологов
- 6. Тримеризация ацетилена
- 7. Получение стирола
- Арены бензол способы получения
- Арены — номенклатура, получение, химические свойства
- Строение молекулы бензола
- Химические свойства бензола
- Гомологи бензола
Способы получения аренов
Арены (ароматические углеводороды) – это непредельные (ненасыщенные) циклические углеводороды, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Общая формула: CnH2n–6 при n ≥ 6.
Получение аренов
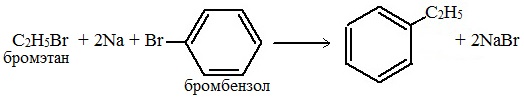
1. Реакция Вюрца-Фиттига
Хлорбензол реагирует с хлорметаном и натрием. При этом образуется смесь продуктов, одним из которых является толуол:
2. Дегидроциклизация алканов
Алканы с углеродной цепью, содержащей 6 и более атомов углерода в главной цепи, при дегидрировании образуют устойчивые шестиатомные циклы, т. е. циклогексан и его гомологи, которые далее превращаются в ароматические углеводороды.
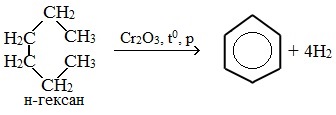
Гексан при нагревании в присутствии оксида хрома (III) в зависимости от условий может образовать циклогексан и потом бензол:
Гептан при дегидрировании в присутствии катализатора образует метилциклогексан и далее толуол:
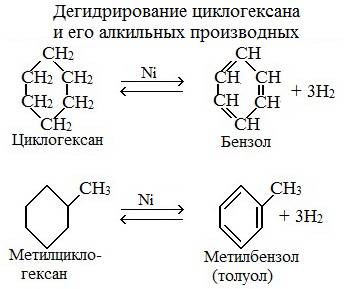
3. Дегидрирование циклоалканов
При дегидрировании циклогексана и его гомологов при нагревании в присутствии катализатора образуется бензол или соответствующие гомологи бензола.
| Например, при нагревании циклогексана в присутствии палладия образуется бензол и водород |
| Например, при нагревании метилциклогексана в присутствии палладия образуется толуол и водород |
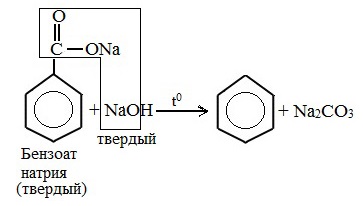
4. Декарбоксилирование солей бензойной кислоты
Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении.
R–COONa + NaOH → R–H + Na2CO3
Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты.
Взаимодействие бензоата натрия с гидроксидом натрия в расплаве протекает аналогично реакции получения алканов по реакции Дюма с образованием бензола и карбоната натрия:
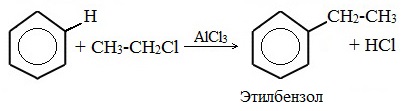
5. Алкилирование бензола и его гомологов
- Арены взаимодействуют с галогеналканами в присутствии катализаторов (AlCl3, FeBr3 и др.) с образованием гомологов бензола.
| Например, бензол реагирует с хлорэтаном с образованием этилбензола |
- Ароматические углеводороды взаимодействуют с алкенами в присутствии хлорида алюминия, бромида железа (III), фосфорной кислоты и др.
| Например, бензол реагирует с этиленом с образованием этилбензола |
| Например, бензол реагирует с пропиленом с образованием изопропилбензола (кумола) |
- Алкилирование спиртами протекает в присутствии концентрированной серной кислоты.
| Например, бензол реагирует с этанолом с образованием этилбензола и воды |
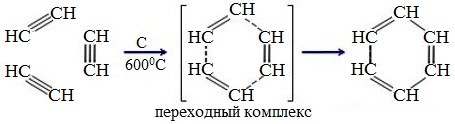
6. Тримеризация ацетилена
При нагревании ацетилена под давлением над активированным углем молекулы ацетилена соединяются, образуя бензол.
При тримеризации пропина образуется 1,3,5-триметилбензол.
7. Получение стирола
Стирол можно получить дегидрированием этилбензола:
Стирол можно также получить действием спиртового раствора щелочи на продукт галогенирования этилбензола (1-хлор-1-фенилэтан):
Источник
Арены бензол способы получения
Основным природным источником ароматических углеводородов является нефть и каменный уголь.
В промышленности
1.При коксовании (сухая перегонка) каменного угля образуется каменноугольная смола, из которой выделяют бензол, толуол, ксилолы, нафталин и многие другие органические соединения.
2.Ароматизация нефти
а) дегидроциклизация (дегидрирование и циклизация) алканов в присутствии катализатора (с числом атомов углерода больше 6):
б) дегидрирование циклоалканов и его гомологов:
При пропускании ацетилена над активированным углем образуется бензол (реакция Зелинского):
В лаборатории
1.Декарбоксилирование солей бензойной кислоты (сплавление солей бензойной кислоты с твердой щелочью)
Соли бензойной кислоты называются бензоаты.
2.Гомологи бензола получают из галогенпроизводных (реакция Вюрца- Фиттига)
Реакции получения аренов указывают на взаимосвязь между различными группами углеводородов и на взаимное превращение их друг в друга.
3.Алкилирование бензола (получение гомологов бензола)
Гомологи бензола получают его взаимодействием с галогеналканами или алкенами в присутствии безводного хлорида алюминия (реакция Фриделя-Крафтса):
При дегидрировании этилбензола образуется производное бензола с непредельной боковой цепью – винилбензол (стирол) C6H5-CН=СН2 (исходное вещество для получения ценного полимера полистирола).
Источник
Арены — номенклатура, получение, химические свойства
Ароматические углеводороды – соединения углерода и водорода, в молекуле которых имеется бензольное кольцо. Важнейшими представителями ароматических углеводородов являются бензол и его гомологи – продукты замещения одного или более атомов водорода в молекуле бензола на углеводородные остатки.
Строение молекулы бензола
Первое ароматическое соединение – бензол – было открыто в 1825 г. М. Фарадеем. Была установлена его молекулярная формула – С6Н6. Если сравнить его состав с составом предельного углеводорода, содержащего такое же количество атомов углерода, — гексаном (С6Н14), то можно заметить, что бензол содержит на восемь атомов водорода меньше. Как известно, к уменьшению количества атомов водорода в молекуле углеводорода приводит появление кратных связей и циклов. В 1865 г. Ф. Кекуле предложил его структурную формулу как циклогексантриена – 1, 3, 5.

Таким образом, молекула, соответствующая формуле Кекуле, содержит двойные связи, следовательно, бензол должен иметь ненасыщенный характер, т. е. легко вступать в реакции присоединения: гидрирования, бромирования, гидратации и т. д.
Однако данные многочисленных экспериментов показали, что бензол вступает в реакции присоединения только в жестких условиях (при высоких температурах и освещении), устойчив к окислению. Наиболее характерными для него являются реакции замещения, следовательно, бензол по характеру ближе к придельным углеводородам.
Пытаясь объяснить эти несоответствия, многие ученые предлагали различные варианты структуры бензол. Окончательно строение молекулы бензола было подтверждено реакцией его образования из ацетилена. В действительности углерод — углеродные связи в бензоле равноценны, и их свойства не похожи на свойства ни одинарных, ни двойных связей.
В настоящее время бензол обозначают или формулой Кекуле, или шестиугольником, в котором изображают окружность.
Так в чем же особенность структуры бензола? На основании данных исследователей и расчетов сделан вывод о том, что все шесть углеродных атомов находятся в состоянии sp 2 -гибридизации и лежат в одной плоскости. Негибридизированные p-орбитали атомов углерода, составляющие двойные связи (формула Кекуле), перпендикулярны плоскости кольца и параллельны друг другу.
Они перекрываются между собой, образуя единую π-систему. Таким образом, система чередующихся двойных связей, изображенных в формуле Кекуле, является циклической системой сопряженных, перекрывающихся между собой -связей. Эта система представляет собой две тороидальные (похожие на бублик) области электронной плотности, лежащие по обе стороны бензольного кольца. Так, изображать бензол в виде правильного шестиугольника с окружностью в центре ( π -система) более логично, чем в виде циклогексатриена-1,3,5. 
Американский ученый Л. Полинг предложил представлять бензол в виде двух граничных структур, отличающихся распределением электронной плотности и постоянно переходящих друг в друга, т. е. считать его промежуточным соединением, «усреднением» двух структур.
Данные измерения длин связей подтверждают эти предположения. Выяснено, что все С—С связи в бензоле имеют одинаковую длину (0,139 нм). Они несколько короче одинарных С—С связей (0,154 нм) и длиннее двойных (0,132 нм).
Существуют также соединения, молекулы которых содержат несколько циклических структур.
Изомерия и номенклатура
Для гомологов бензола характерна изомерия положения нескольких заместителей. Простейший гомолог бензола — толуол (метилбензол) — не имеет таких изомеров; следующий гомолог представлен в виде четырех изомеров:

Основой названия ароматического углеводорода с небольшими заместителями является слово бензол. Атомы в ароматическом кольце нумеруют, начиная от старшего заместителя к младшему:

По старой номенклатуре положения 2 и 6 называют ортоположениями, 4 — пара-, а 3 и 5 — метаположениями.
Физические свойства
Бензол и его простейшие гомологи в обычных условиях весьма токсичные жидкости с характерным неприятным запахом. Они плохо растворяются в воде, но хорошо — в органических растворителях.
Химические свойства бензола
Реакции замещения. Ароматические углеводороды вступают в реакции замещения.
1. Бромирование. При реакции с бромом в присутствии катализатора, бромида железа (ΙΙΙ), один из атомов водорода в бензольном кольце может замещаться на атом брома:
2. Нитрирование бензола и его гомологов. При взаимодействии ароматического углеводорода с азотной кислотой в присутствии серной (смесь серной и азотной кислот называют нитрующей смесью) происходит замещение атома водорода на нитрогруппу —NO2:
Восстановлением образовавшегося в этой реакции нитробензола получают анилин — вещество, которое применяется для получения анилиновых красителей:
Эта реакция носит имя русского химика Зинина.
Реакции присоединения. Ароматические соединения могут вступать и в реакции присоединения к бензольному кольцу. При этом образуются циклогексан или его производные.
1. Гидрирование. Каталитическое гидрирование бензола протекает при более высокой температуре, чем гидрирование алкенов:
2. Хлорирование. Реакция идет при освещении ультрафиолетовым светом и является свободнорадикальной:
Гомологи бензола
Состав их молекул отвечает формуле СnH2n-6. Ближайшие гомологи бензола:
Все следующие за толуолом гомологи бензола имеют изомеры. Изомерия может быть связана как с числом и строением заместителя (1, 2), так и с положением заместителя в бензольном кольце (2, 3, 4). Соединения общей формулы С8Н10:
По старой номенклатуре, употребляемой для указания относительного расположения двух одинаковых или разных заместителей в бензольном кольце, используют приставки орто— (сокращенно о-) – заместители расположены у соседних атомов углерода, мета- (м-) – через один атом углерода и пара— (п-) – заместители друг против друга.
Первые члены гомологического ряда бензола – жидкости со специфическим запахом. Они легче воды. Являются хорошими растворителями.
Гомологи бензола вступают в реакции замещения (бромирование, нитрирование). Толуол окисляется перманганатом при нагревании:
Гомологи бензола используются как растворители, для получения красителей, средств для защиты растений, пластмасс, лекарств.
Источник