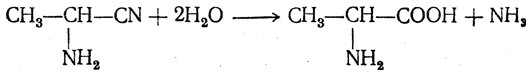
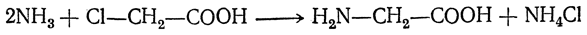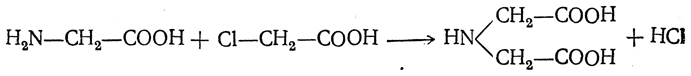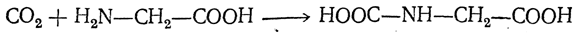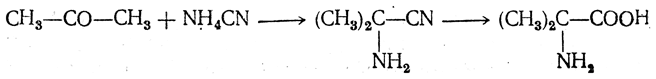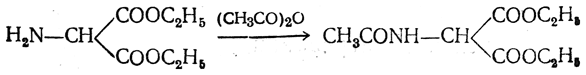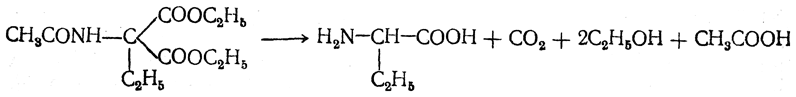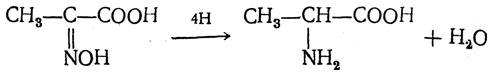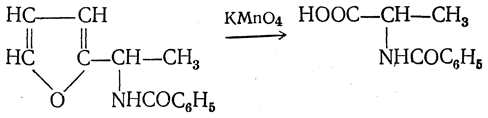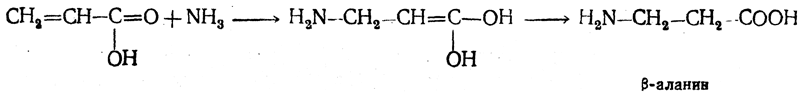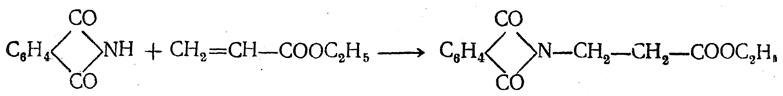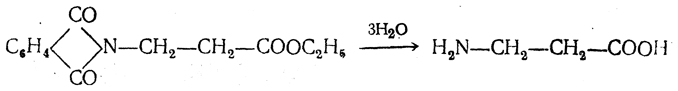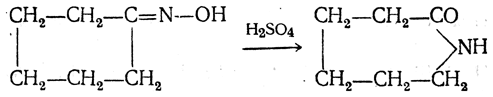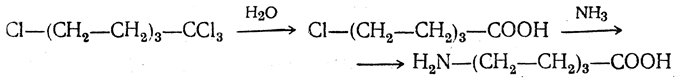Общие способы получения аминокислот
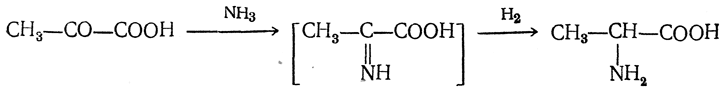
Чтобы свести к минимуму нежелательное образование иминодиуксусной кислоты по реакции
реакцию ведут с очень большим избытком аммиака или в присутствии карбоната аммония, который защищает аминогруппу. Образующееся карбаминовое производное аминокислоты
легко разлагается при нагревании.
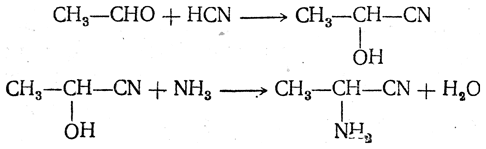
2. Получение из циангидринов альдегидов и кетонов (циангидринный метод). Важной реакцией получения α-аминокислот является действие аммиака на циангидрины альдегидов и кетонов
Аминонитрилы можно получить также, действуя на альдегиды или кетоны непосредственно цианистым аммонием. Эта реакция приобрела особое значение после того, как Н. Д. Зелинский с сотрудниками показали, что синильную кислоту и аммиак или цианистый аммоний можно заменить смесью водных растворов хлористого аммония и цианистого калия, в результате обменного разложения дающих цианистый аммоний, который и вступает в реакцию с альдегидами или кетонами:
3. Синтезы из сложных эфиров, содержащих подвижный атом водорода. Большое значение приобрели синтезы аминокислот из малонового, циануксусного и ацетоуксусного эфиров. Пользуясь этими методами, можно получить аминокислоты, содержащие различные радикалы.
а) Синтез из малонового эфира. Из малонового эфира получают нитрозомалоновый эфир, который восстанавливают в аминомалоновый эфир водородом в присутствии катализатора или цинком в кислой среде:
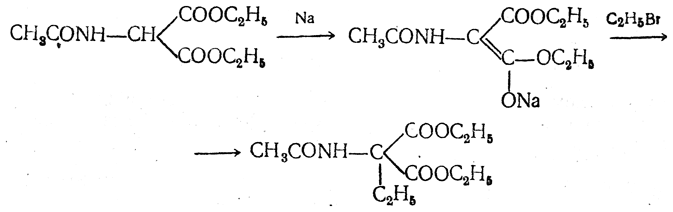
полученный ацетиламиномалоновый эфир алкилируют, действуя на него последовательно металлическим натрием и галоидным алкилом:
После омыления и декарбоксилирования получается α-аминокислота:
б) Синтез из циануксусного эфира проводится аналогично синтезу из малонового эфира.
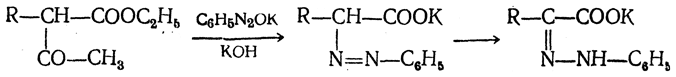
в) Синтез из ацетоуксусного эфира. При действии на однозамещенные ацетоуксусные эфиры раствором фенилдиазотата, а затем щелочью отщепляется уксусная кислота и образуется неустойчивое азосоединение, которое изомеризуется в фенилгидразон соответствующей кетокислоты:
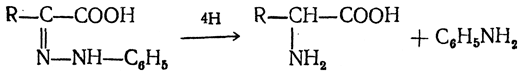
Восстановление фенилгидразона кетокислоты цинком в солянокислой спиртовой среде приводит к α-аминокислоте:
Этот метод синтеза аминокислот предложен В. В. Феофилактовым.
4. В осст а н ов л ен и е оксимов или гидразонов альдегид о- или кетонокислот. Например:
Особенно удачным оказался метод, состоящий в одновременном действии на кетокислоту аммиака и водорода в присутствии катализатора (платины или палладия). По-видимому, при этом промежуточно образуется иминопроизводное:
Этим методом синтезируют аминокислоты, содержащие изотоп азота N 15 («меченый азот»), которыми пользуются при изучении поведения аминокислот в живом организме.
В последние годы предложено еще два новых общих метода синтеза аминокислот, основанных на использовании дешевого промышленного сырья — фурана и тиофена.
5. Синтез аминокислот из фурановых производных (метод А. П. Терентьева и Р. А. Грачевой) основан на легкости окисления фуранового кольца перманганатом с образованием карбоксильной группы. Если в боковой цепи у фуранового кольца имеется аминогруппа (обычно защищенная бензоильной группой), то в результате окисления получается бензоиламинокислота, а после омыления — сама аминокислота. В зависимости от положения аминогруппы в цепи получается α-, β-, γ- и т. п. кислота.
Так, при окислении 1-бензоиламино-1-(α-фурил)-алкилов получается α-кислота, например из 1-бензоиламино-1-(α-фурил)-этана — бензоил-α-аланин:
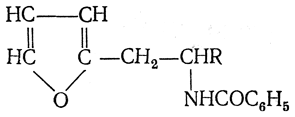
Для получения β-аминокислот пользуются 2-бензоиламино-1-(α-фурил)алкилами
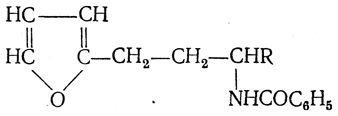
а для синтеза γ-аминокислот берут 3-бензоиламино-1-(α-фурил)-алкилы:
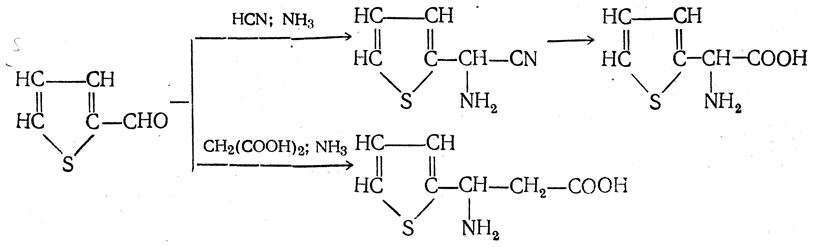
6. Синтез аминокислот из производных тиофен а (метод Я. Л. Гольдфарба, Б. П. Фабричного и И. Ф. Шалавиной) основан на восстановительном десульфировании производных тиофена или его гомологов водородом скелетного никелевого катализатора. В зависимости от взятого производного десульфирование приводит к аминокислотам с разным положением аминогруппы.
Из тиенилальдегида обычными методами получают тиенил-α- или тиенил-β -аминокислоты
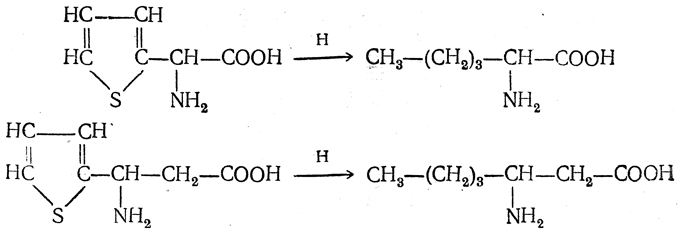
которые затем десульфируют:
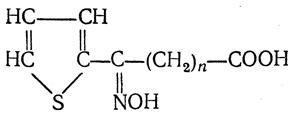
Из разных оксиминокислот тиофенового ряда
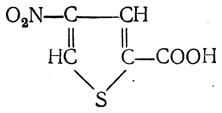
можно получать аминокислоты с любым положением аминогруппы. Наконец, можно ввести непосредственно в ядро тиофена нитро- и карбоксильную группы, например
и затем прогидрировать полученное соединение никелем Ренея. Этим путем можно получать только γ- и δ-аминокислоты.
Способы получения аминокислот с удаленной аминогруппой (β-, γ-, δ-, ε-, . . ., ω-аминокислот). Кроме общих способов получения аминокислот, дающих возможность синтезировать как
α-аминокислоты, так и кислоты с удаленной аминогруппой, для получения последних имеются и специальные методы, рассматриваемые ниже.
1. Присоединение аммиака к ненасыщенным кислотам. При действии аммиака в спиртовом растворе на α,β-ненасыщенные кислоты или их эфиры аминогруппа вступает в β-положение. Как и в случае присоединения воды при образовании оксикислот, аммиак, вероятно, сначала присоединяется в положение 1,4 системы сопряженных двойных связей:
Поэтому присоединение аммиака идет против правила Марковникова.
Реакцию удобнее проводить, действуя на эфир акриловой кислоты не аммиаком, а фталимидом (в присутствии гидроокиси триметилфениламмония как катализатора):
Гидролизом образующегося эфира фталил-β-аланина можно получить и сам β-аланин:
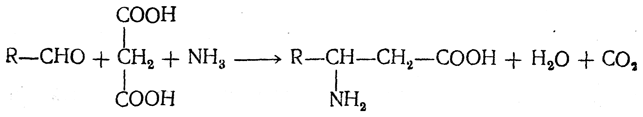
2. Конденсация альдегидов с малоновой кислотой в присутствии спиртового раствора аммиака. Этот путь синтеза, разработанный В. М. Родионовым с сотрудниками, является общим методом получения β-аминокислот:
3. Получение из оксимов циклических кетон о в. δ- и ε-Аминокислоты получают чаще всего из оксимов циклических кетонов путем так называемой бекмановской перегруппировки. Так, например, оксим циклогексанона под действием серной кислоты изомеризуется с расширением цикла, в результате чего образуется ε-капролактам:
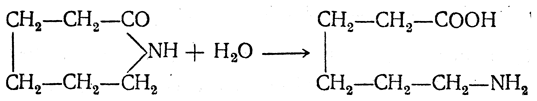
Эта реакция используется для производства капролактама в промышленном масштабе. Гидролиз капролактама приводит к ε-аминокапроновой кислоте:
4. Получение «-аминокислот действием аммиака на ω-га л о и дз а м еще н н ы е кислоты. ω-Аминокислоты с нечетным числом углеродных атомов получаются из тетрахлоралканов типа Сl—(СН2—СН2)n—ССl3, являющихся продуктами реакции теломеризации. Гидролиз тетрахлоралканов указанного типа, полученных из этилена и четыреххлористого углерода, приводит к ω-хлоркарбоновым кислотам, которые действием избытка аммиака превращаются в соответствующие ω-аминокислоты, например:
Этим путем получается ω-аминоэнантовая кислота — исходный продукт для получения синтетического волокна энант (А. Н. Несмеянов, Р. X. Фрейдлина и др.).
Источник
Способ получения гамма-аминомасляной кислоты (гамк)
Изобретение относится к биотехнологии и представляет собой способ получения гамма-аминомасляной кислоты (ГАМК) с использованием ауксотрофной по L-изолейцину бактерии Escherichia coli. Указанную бактерию выращивают в питательной среде, содержащей не менее 100 мг/л L-изолейцина, затем выделяют гамма-аминомасляную кислоту из культуральной жидкости. Данное изобретение позволяет увеличить выход ГАМК. 2 з.п. ф-лы, 2 табл.
Настоящее изобретение относится к микробиологической промышленности и медицине и касается способа получения гамма-аминомасляной кислоты (ГАМК) с использованием ауксотрофных по L-изолейцину бактерий, принадлежащих к роду Escherichia.
Предшествующий уровень техники
Гамма-аминомасляная кислота (ГАМК) считается одним из основных ингибирующих аминокислотных медиаторов нервных импульсов в мозгу млекопитающих. Будучи широко (хотя и неравномерно) распространенным в мозгу млекопитающих, ГАМК является, как предполагается, медиатором приблизтельно 30% синапсов в мозгу. ГАМК является посредником в множестве функций синапсов посредством образования комплексов с белками (рецепторами ГАМК), расположенными как на клетках, так и на нервных окончаниях. Постсинаптический ответ на ГАМК происходит путем изменения проводимости хлоридов, что, как правило, хотя и не обязательно, приводит к гиперполяризации клетки (WO 0200221 A1). Поскольку ГАМК является эффективным нейромедиатором, она используется в медицине для лечения нарушений мозговой деятельности, таких как амнезия, парафазия (нарушение речи), гемиплегия (паралич половины тела), гипертонии и других. Также ГАМК может использоваться в качестве карциностатического агента (JP 60139622 A2).
Известны химические методы синтеза ГАМК (Garmaise et al, Canad. J.Chemistry, 1956, 34, 742-748; Авторское свидетельство СССР №452196). Для медицинских целей также может быть испльзована пища, обогащенная ГАМК. Известны различные продукты, получаемые из растений, обогащенных ГАМК. К ним относятся листья чая (выложенная заявка Японии 9-205989), листья кофе (выложенная заявка Японии 8-173111), растения рода крестоцветных и их сок (Европейская заявка ЕР 1082911 А2), нитевидные грибы (JP 2000060536 A2), порошок или сок растений вида Brassicaceous (JP 2001136929 А2) и другие.
Описаны микробиологические способы получения ГАМК с использованием бактерий Е. coli ВКПМ В-7460 и ВКПМ В7452, содержащих плазмиду с геном глутаматдекарбоксилазы (патент РФ №2143002), Bad. cadaveris ATCC 9760 (JP69-01197), Е. coli ATCC 9637 (JP70-15437) и Arthrobacter simplex ATCC 15799 (JP69-01196).
Но до настоящего времени не было сообщений, описывающих тот факт, что ауксотрофные по L-изолейцину бактерии, принадлежащие к роду Escherichia, могут продуцировать ГАМК в условиях, когда такие бактерии выращиваются в питательной среде, содержащей значительное количество L-изолейцина.
Объектом настоящего изобретения является способ получения гамма-аминомасляной кислоты (ГАМК), включающий стадии выращивания ауксотрофной по L-изолейцину бактерии, принадлежащей к роду Escherichia, в питательной среде, содержащей значительное количество L-изолейцина.
Цель была достигнута путем установления того факта, что ауксотрофные по L-изолейцину бактерии, принадлежащие к роду Escherichia, в ходе выращивания в питательной среде, содержащей L-изолейцин в количестве, большем, чем это необходимо для комплементации ауксотрофии по L-изолейцину, могут продуцировать ГАМК.
Таким образом было совершено настоящее изобретение.
Так, настоящее изобретение включает следующее.
1) Способ получения гамма-аминомасляной кислоты (ГАМК), включающий стадии:
— выращивания ауксотрофной по L-изолейцину бактерии, принадлежащей к роду Escherichia, в питательной среде, содержащей не менее 100 мг/л L-изолейцина, с целью продукции и накопления гамма-аминомасляной кислоты (ГАМК), и
— выделения гамма-аминомасляной кислоты (ГАМК) из культуральной жидкости.
2) Способ в соответствии с 1), в котором бактерия модифицирована с целью увеличения экспрессии генов биосинтеза L-глутамата.
3) Способ в соответствии с 1), в котором используется бактерия Escherichia coli VL334thrC + или Escherichia coli 702ilvA (ВКПМ B-8012).
Далее настоящее изобретение будет описано более подробно. Способом согласно настоящему изобретению является способ получения гамма-аминомасляной кислоты (ГАМК), включающий стадии:
— выращивания ауксотрофной по L-изолейцину бактерии, принадлежащей к роду Escherichia, в питательной среде, содержащей не менее 100 мг/л L-изолейцина, с целью продукции и накопления гамма-аминомасляной кислоты (ГАМК), и
— выделения гамма-аминомасляной кислоты (ГАМК) из культуральной жидкости. Термин “ауксотрофная по L-изолейцину бактерия” означает, что указанная бактерия требует наличия L-изолейцина в питательной среде для своего роста. В данном случае “ауксотрофной по L-изолейцину бактерией” является бактерия, которая требует наличия в питательной среде не менее 10 мг/л L-изолейцина. Поэтому концентрация L-изолейцина в питательной среде для ауксотрофной по L-изолейцину бактерии составляет обычно не менее 10 мг/л. Способы получения ауксотрофных по L-изолейцину бактерий хорошо известны и описаны, например, в Европейском патенте ЕР 1172433.
Термин “бактерия, принадлежащая к роду Escherichia” означает, что бактерия относится к роду Escherichia в соответствии с классификацией, известной специалисту в области микробиологии. В качестве примера микроорганизма, принадлежащего к роду Escherichia, использованного в настоящем изобретении, может быть упомянута бактерия Escherichia coli (Е. coif).
Примерами ауксотрофных по L-изолейцину бактерий, принадлежащих к роду Escherichia, являются штаммы, дефицитные по гену ilvA, такие как штаммы Е. coli B7ILE (VKPM B-8013), VL334thrC + 702ilvA (VKPM В-8012) и 237 (VKPM В-7925), описанные в Европейском патенте ЕР 1172433.
Авторы настоящего изобретения установили, что ауксотрофные по L-изолейцину бактерии, принадлежащие к роду Escherichia, в ходе выращивания в питательной среде, содержащей L-изолейцин в количестве, большем, чем это необходимо для комплементации ауксотрофии по L-изолейцину, могут продуцировать ГАМК. Другими словами, в условиях, когда потребность в L-изолейцине не является фактором, лимитирующим рост ауксотрофных по L-изолейцину бактерий, выращивание указанных бактерий приводит к накоплению ГАМК в культуральной жидкости. Концентрация L-изолейцина должна быть не менее 100 мг/л. Детальный механизм установленного факта остается неустановленным.
Согласно настоящему изобретению выращивание, выделение и очистка ГАМК из культуральной или подобной ей жидкости может быть осуществлена способом, подобным традиционным способам ферментации, в которых ГАМК продуцируется с использованием бактерий.
Питательная среда, используемая для выращивания, может быть как синтетической, так и натуральной, при условии, что указанная среда содержит источники углерода, азота, минеральные добавки и необходимое количество L-изолейцина, необходимого для роста бактерии. Количество L-изолейцина, используемое в способе согласно настоящему изобретению, должно быть не менее 100 мг/л. К источникам углерода относятся различные углеводы, такие как глюкоза и сахароза, а также различные органические кислоты. В зависимости от характера ассимиляции используемого микроорганизма, могут использоваться спирты, такие как этанол и глицерин. В качестве источника азота могут использоваться различные неорганические соли аммония, такие как аммиак и сульфат аммония, другие соединения азота, такие как амины, природные источники азота, такие как пептон, гидролизат соевых бобов, ферментолизат микроорганизмов. В качестве минеральных добавок могут использоваться фосфат калия, сульфат магния, хлорид натрия, сульфат железа, сульфат марганца, хлорид кальция и подобные им соединения. В качестве витаминов могут использоваться тиамин и дрожжевой экстракт.
Выращивание осуществляется предпочтительно в аэробных условиях, таких как перемешивание культуральной жидкости на качалке, взбалтывание с аэрацией, при температуре в пределах от 20 до 40°С, предпочтительно в пределах от 30 до 38°С. рН среды поддерживают в пределах от 5 до 9, предпочтительно от 6.5 до 7.2. рН среды может регулироваться аммиаком, карбонатом кальция, различными кислотами, основаниями и буферными растворами. Обычно выращивание в течение от 1 до 5 дней приводит к накоплению целевой кислоты в культуральной жидкости.
После выращивания твердые остатки, такие как клетки, могут быть удалены из культуральной жидкости методом центрифугирования или фильтрацией через мембрану, а затем ГАМК может быть выделена и очищена методами ионообменной хроматографии, концентрирования и кристаллизации.
Наилучший способ осуществления изобретения
Более детально настоящее изобретение будет разъяснено ниже со ссылкой на Примеры.
Пример 1. Продукция ГАМК с использованием дефицитного по гену ilvA штамма Е. coli VL334thrC + .
Штамм VL334 (ВКПМ В-1641) является ауксотрофным по L-изолейцину и L-треонину штаммом, содержащим мутации в генах thrC и ilvA (патент США 4278765). Природный аллель гена thrC был перенесен методом общей трансдукции с использованием бактериофага Р1, выращенного на клетках природного штамма Е. coli К12 (ВКПМ В-7). В результате был получен ауксотрофный по L-изолейцину штамм VL334thrC + . Указанный штамм обладал способностью к продукции L-глутаминовой кислоты (Европейский патент ЕР 1172433).
Питательная среда для ферментации содержала 60 г/л глюкозы, 25 г/л сульфата аммония, 2 г/л КН2 PO4, 1 г/л MgSO4, 0.1 мг/мл тиамина и 25 г/л мела (рН 7.2). L-изолейцин добавляли в различных концентрациях. Глюкозу и мел стерилизовали раздельно. 2 мл питательной среды были помещены в пробирки и инокулированы одной петлей микроорганизма. Выращивание проводили при 30°С в печение 3 дней с перемешиванием.
ГАМК определяли с помощью метода “Waters Accq-Tag Amino Acid Analysis Method” в соответствии с рекомендациями производителя. Указанный метод заключается в получении производных пептидов и аминокислот из гидролизованных белков перед нанесением на колонку с последующим разделением полученных производных с помощью обращенно-фазовой ВЭЖХ с флюоресцентной детекцией. Коэффициент удерживания (RC) определяется как отношение времени удерживания пика вещества (RT) к времени удерживания L-фенилаланина (рН элюента 5.05). RC L-пролина = 0.695, RC ГАМК=0.701. Длина волны возбуждения флюоресцентного детектора была 250 нм, область длин волн испускания была 320-560 нм. Максимум испускания для L-пролина составлял 395 нм, максимум испускания для ГАМК составлял 395 нм и 460 нм. Подлинность ГАМК также была подтверждена методами масс-спектроскопии и ЯМР.
Количество ГАМК и L-глутаминовой кислоты измеряли с помощью бумажной хроматографии (состав подвижной фазы: бутанол уксусная кислота вода =4:1:1). Результаты выращивания представлены в таблице 1.

Пример 2. Продукция ГАМК с использованием дефицитного по гену ilvA штамма Е. coli 702ilvA.
Штамм 702ilvA (ВКПМ В-8012) является штаммом, дефицитным по гену ilvA, и обладает способностью к продукции L-пролина (Европейский патент ЕР 1172433). Штамм 702ilvA выращивали в тех же условиях, которые описаны в Примере 1. Результаты выращивания представлены в таблице 2.

1.Способ получения гамма-аминомасляной кислоты (ГАМК), включающий стадии выращивания ауксотрофной по L-изолейцину бактерии Escherichia coli в питательной среде, содержащей не менее 100 мг/л L-изолейцина, и выделения гамма-аминомасляной кислоты (ГАМК) из культуральной жидкости.
2. Способ по п.1, отличающийся тем, что бактерия модифицирована с целью увеличения экспрессии генов биосинтеза L-глутамата.
3. Способ по п.1, отличающийся тем, что используют штамм бактерии Escherichia coli VL334thrC + или Escherichia coli 702ilvA (ВКПМ В-8012).
Источник