- Активный транспорт
- Активный и пассивный транспорт через мембрану
- Виды транспорта через мембрану
- Пассивный транспорт через мембрану
- Диффузия
- Отличие каналов и пор
- Облегченная диффузия
- Активный транспорт
- Первично-активный транспорт
- Вторично-активный транспорт
- Экзоцитоз и эндоцитоз
- Транспорт через несколько слоев клеток
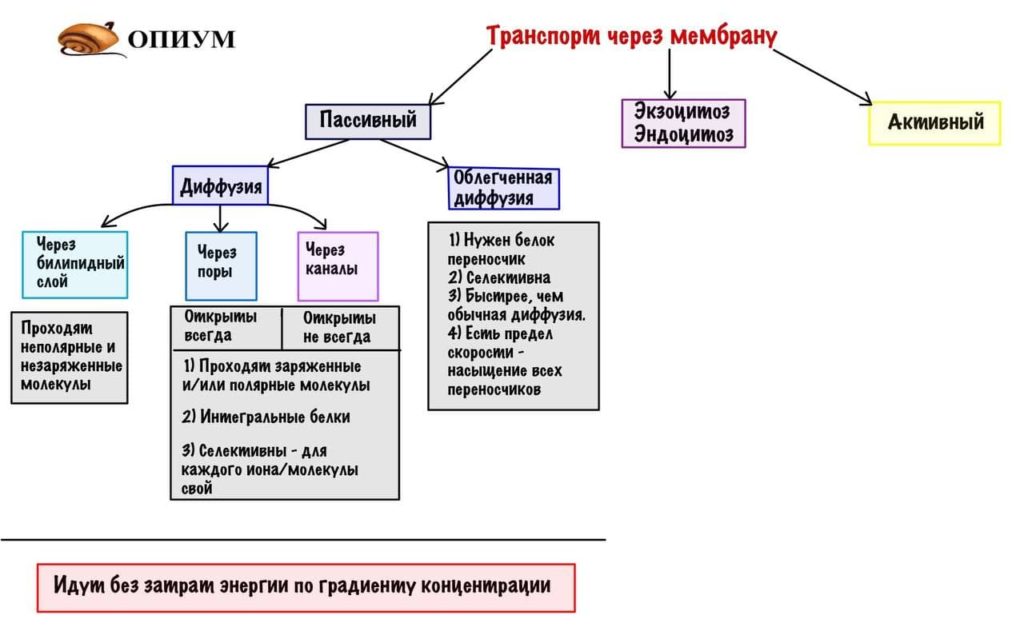
Активный транспорт



Активный транспорт — энергозависимый трансмембранный перенос против электрохимического градиента. Различают первичный и вторичный активный транспорт. Первичный активный транспорт осуществляют насосы (различные АТФазы), вторичный — симпортёры (сочетанный однонаправленный транспорт) и антипортёры (встречный разнонаправленный транспорт).
Первичный активный транспорт. Движущая сила трансмембранного переноса возникает при ферментативном гидролизе макроэргических связей АТФ. Родовой термин для таких АТФаз (например, Na + ,K + -, H + ,K + -, Ca 2+ ‑АТФазы) — насосы.
Вторичный активный транспорт. Движущая сила для трансмембранного переноса одного вещества (или ионов) против электрохимического градиента возникает за счёт потенциальной энергии, запасённой за счёт сочетанного переноса ионов (как правило, Na + ) по электрохимическому градиенту. В большинстве случаев поступление Na + в цитозоль из межклеточного пространства и обеспечивает вторичный активный транспорт разных ионов и веществ. Известно 2 типа вторичного активного переноса — симпорт и антипорт (рис. 2–6).
Первичный активный транспорт обеспечивают следующие насосы — натрий, калиевые АТФазы, протонные и калиевые АТФазы, Са 2+ -транспортирующие АТФазы, митохондриальные АТФазы, лизосомальные протонные насосы и др.
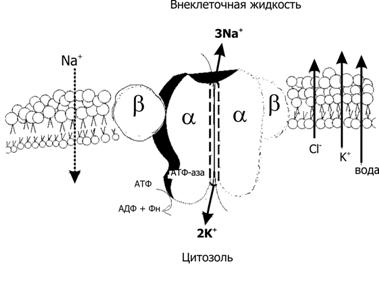
Натрий, калиевая АТФаза (рис. 2–11) регулирует трансмембранные потоки основных катионов (Na + , K + ) и опосредованно — воды (что поддерживает постоянный объём клетки), обеспечивает Na + –связанный трансмембранный перенос (симпорт и антипорт) множества органических и неорганических молекул, участвует в создании МП покоя и генерации ПД нервных и мышечных элементов.
Электрогенность. При каждом цикле гидролиза АТФ 3 иона Na + выбрасываются из клетки, а 2 иона K + поступают в цитозоль, суммарный эффект — выброс из клетки одного катиона. Другими словами, Na + ,K + ‑насос обладает электрогенностью: его работа приводит к поддержанию положительного заряда наружной (внеклеточной) поверхности мембраны.
Сердечные гликозиды (например, уабаин и дигоксин) блокируют работу Na + ,K + –насоса, конкурентно с K + взаимодействуя с участком связывания K + на наружной поверхности мембраны. В результате при гипокалиемии (низкий [K + ] плазмы крови) увеличивается токсичность сердечных гликозидов.
Рис. 2–11. Na + ,K + –насос[7]. Модель Na + ,K + –АТФазы, встроенной в плазматическую мембрану. Na + ,K + –насос — интегральный мембранный белок, состоящий из 4 СЕ (формирующие канал 2 каталитические субъединицы и 2 гликопротеина ). Na + ,K + ‑насос осуществляет транспорт катионов против электрохимического градиента (X) — транспортирует Na + из клетки в обмен на K + (при гидролизе одной молекулы АТФ 3 иона Na + выкачиваются из клетки, и 2 иона K + закачиваются в неё). Слева и справа от насоса при помощи стрелок показаны направления трансмембранного потока ионов и воды в клетку (Na + ) и из клетки (K + , Cl – и вода) в силу различий их X. АДФ — аденозиндифосфат, Фн — неорганический фосфат.
Протонная и калиевая АТФаза (H + ,K + ‑насос). При помощи этого фермента париетальные клетки желёз слизистой оболочки желудка участвуют в образовании соляной кислоты (электронейтральный обмен 2 внеклеточных ионов K + на 2 внутриклеточных иона H + при гидролизе одной молекулы АТФ).
H + ,K + ‑АТФаза — гетеродимер (2 высокомолекулярных ‑СЕ и 2 меньшей мол. массы и сильно гликозилированной ‑СЕ).
‑СЕ — главный Аг, к которому при некоторых заболеваниях (например, при витамин B12–анемиях и атрофическом гастрите) в крови циркулируют АТ.
Са 2+ —транспортирующие АТФазы (Са 2+ ‑АТФазы) выкачивают ионы кальция из цитоплазмы в обмен на протоны против значительного электрохимического градиента Са 2+ .
Са 2+ ‑АТФазы плазмолеммы переносят ионы кальция из цитоплазмы во внеклеточное пространство в обмен на протоны (1 H + в обмен на 1 Ca 2+ при гидролизе 1 молекулы АТФ).
Са 2+ ‑АТФазы саркоплазматического ретикулума. Как и Са 2+ ‑АТФазы плазмолеммы, Са 2+ -транспортирующие АТФазы саркоплазматического ретикулума откачивают ионы кальция из цитоплазмы (2 H + в обмен на 2 Ca 2+ при гидролизе 1 молекулы АТФ), но не во внеклеточное пространство, а во внутриклеточные депо кальция (в замкнутые межмембранные объёмы гладкой эндоплазматической сети, именуемой в скелетных МВ и кардиомиоцитах — саркоплазматический ретикулум). Недостаточность Са 2+ ‑АТФазы саркоплазматического ретикулума проявляется симптомами мышечной усталости (миопатия) при физической нагрузке.

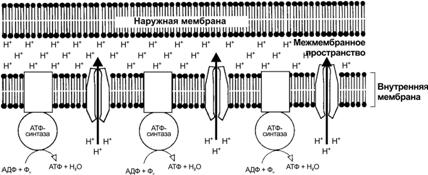
Митохондриальная АТФаза типа F (F0F1) — АТФ–синтаза внутренней мембраны митохондрий — катализируют конечный этап синтеза АТФ (рис. 2–12). Кристы митохондрий содержат АТФ-синтазу, сопрягающую окисление в цикле Кребса и фосфорилирование АДФ до АТФ. АТФ синтезируется при обратном токе протонов в матрикс через канал в АТФ-синтезирующем комплексе.
Хемиосмотическое сопряжение. Сопряжение переноса электронов и синтеза АТФ (механизм предложил Питер Митчелл в 1961 г.) обеспечивает протонный градиент. Внутренняя мембрана непроницаема для анионов и катионов. Но при прохождении электронов по дыхательной цепи ионы H + откачиваются из матрикса митохондрий в межмембранное пространство (рис. 2–12). Эта энергия электрохимического протонного градиента и используется для синтеза АТФ и транспорта метаболитов и неорганических ионов в матрикс.
Рис. 2–12. Механизм хемиосмотического сопряжения при образовании АТФ в митохондриях [11]. При транспорте электронов по дыхательной цепи из матрикса через внутреннюю мембрану в межмембранное пространство митохондрий поступает H + . Созданный таким образом электрохимический градиент (H) позволяет АТФ-синтазе катализировать реакцию АДФ + неорганический фосфат (Фн) АТФ.
Лизосомальные протонные насосы (H + ‑АТФазы типа V [от Vesicular]), встроенные в мембраны, окружающие лизосомы (также комплекс Гольджи и секреторные пузырьки), транспортируют H + из цитозоля в эти мембранные органеллы. В результате в них понижается значение pH, что оптимизирует функции этих структур.
Транспортёры ABC (от ATP-Binding Cassette — АТФ-связывающая последовательность) — либо гидролизующие АТФ насосы для активного транспорта разных ионов и молекул, либо ионные каналы или регуляторы ионных каналов. Так, ген CFTR (от cystic fibrosis transmembrane regulator — трансмембранный регулятор кистозного фиброза) кодирует структуру хлорного канала (одновременно регулятор функционирования других каналов), мутации которого приводят к развитию муковисцидоза (кистозного фиброза).
Вторичный активный транспорт. Известны 2 формы активного вторичного транспорта: сочетанный (симпорт) и встречный (антипорт) (см. рис. 2–6).
Симпорт — сочетанный перенос (котранспорт, сочетанный транспорт) — движение двух веществ сквозь мембрану при помощи одного и того же переносчика (симпортёра).
Антипорт — одновременное трансмембранное перемещение двух веществ, но в противоположном направлении (встречный транспорт) при помощи одного и того же переносчика (антипортёра, обменника).
Симпорт реализуют интегральные мембранные белки. Перенос вещества Х против его электрохимического градиента (Х) в большинстве случаев происходит за счёт поступления в цитозоль из межклеточного пространства по градиенту диффузии ионов натрия (т.е. за счёт Na), а в ряде случаев — за счёт поступления в цитозоль из межклеточного пространства по градиенту диффузии протонов (т.е. за счёт H). В итоге и ионы (Na + или H + ), и вещество Х (например, глюкоза, аминокислоты, неорганические анионы, ионы калия и хлора) перемещаются из межклеточного вещества в цитозоль.
Всасывание глюкозы происходит через верхушечные поверхности клеток, окаймляющих просвет проксимальных извитых канальцев почки и тонкого кишечника при помощи сочетанного транспорта с ионами Na + . Разные изоформы транспортёра переносят Na + и глюкозу в соотношении 1:1 или 2:1. Расчёты показывают, что максимальная концентрация глюкозы в клетке может в 100 или в 10 4 раз превышать её концентрацию в плазме крови.
При стехиометрии 1:1 движущая сила равна сумме разностей электрохимического потенциала для Na + (Na) и химического потенциала для глюкозы (глюкоза). Равновесие достигается, когда Na в одном направлении становится равным глюкоза в противоположном направлении:
Источник
Активный и пассивный транспорт через мембрану
Ты уже шаришь какое строение у биологических мембран, так что можно переходить к тому, как вся эта система работает. И начнем мы с транспорта веществ через мембрану. Довольно важная тема, без нее мы не поймем, как формируется потенциал действия, как в клетку попадают энергетические субстраты и вода. Так что присаживаемся поудобнее и поехали!
Виды транспорта через мембрану
Начнем с небольшой классификации. Транспорт можно разделить на пассивный и активный (никаких шуток про геев мне тут), такое разделение основано на затратах энергии. При пассивном транспорте — затрат энергии нет, а при активном транспорте — есть. Это может быть энергия заключенная в АТФ, либо энергия градиента концентрации. Не пугаемся, дальше все будем разбирать подробнее. Еще есть особенный транспорт — экзоцитоз и эндоцитоз (транспортируются макромолекулы), их скорее можно отнести к активному транспорту, но мы рассмотрим их отдельно.
Пассивный транспорт через мембрану
Здесь всего два вида — простая диффузия и облегченная диффузия. В чем отличие? При облегченной диффузии для молекулы, которая будет проходить через мембрану нужен проводник — белок переносчик. Для простой диффузии же переносчик не требуется, она и сама справляется.
Диффузия
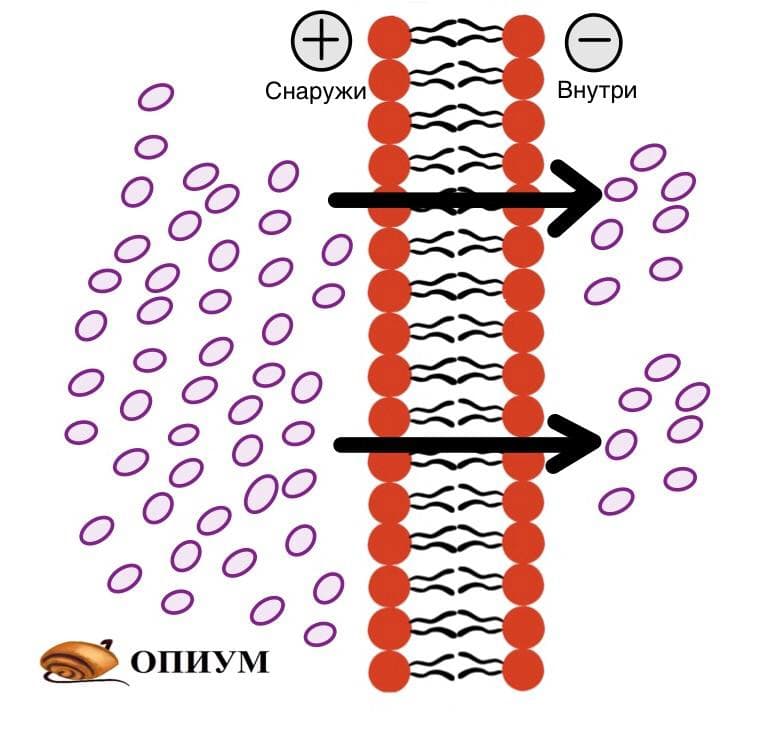
Она идет по градиенту концентрации — если на одной стороне мембраны вещества много, то оно будет стремиться перейти на другую сторону. На самом деле диффузия зависит не только от градиента концентрации — еще на нее влияет заряд мембраны и частиц, которые пытаются пройти через мембрану, и давление.
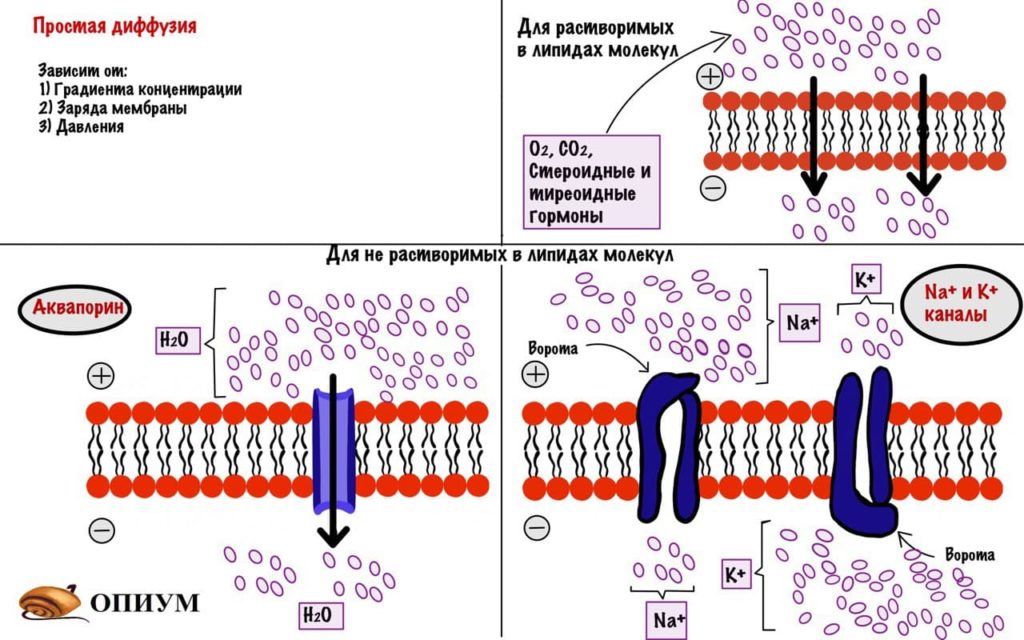
Вспоминаем, что основа мембраны — это амфифильные липиды. Если вещество растворимо в липидах, то оно без проблем перейдет на другую сторону. Лучше всего растворимы в липидах неполярные и незаряженные молекулы (CO2,O2, стероидные гормоны). Но через мембрану могут проходить полярные молекулы и незаряженные (тонированные), но здесь все решает размер. Вода пройдет через мембрану, а вот глюкоза — нет. Вода хоть и проходит через мембрану, но хуже чем неполярные и незаряженные молекулы, поэтому для нее есть специальные поры (аквапорины). Кстати, возможно аквапорины еще нужны потому, что вода в растворе переходит в ион гидроксония.
А вот совсем не могут пройти заряженные и полярные молекулы — ионы натрия, калия, гидроксония. Поэтому простую диффузию разделим еще на два варианта:
1) Диффузия жирорастворимых веществ. Молекула растворима в мембране, то есть она неполярная и незаряженная. Она спокойно проходит через мембрану. Избранные молекулы проходят так — O2, CO2, стероидные и тиреоидные гормоны.
2) Но что делать простым пацанам с района, которые не растворимы в жирах? Не парьтесь, для них есть интегральные белки — они образуют каналы и поры. Это просто трубы. Эти каналы очень избирательны, например, у ионов K + , Na + и молекул воды свои собственные каналы, которые не пропускают другие вещества. Это связано с их строением, так у натриевого канала очень много отрицательных групп, которые буквально вытягивают натрий. Поры же пропускают молекулы только определенного размера (если меньше, то пройдет).
Отличие каналов и пор
Отличие каналов и пор в том, что первые открыты не всегда, а вторые постоянно. У натриевых и калиевых каналов есть шляпка (или ворота), которая открывается двумя способами — в зависимости от типа клетки. Первый способ — изменение электрического заряда мембраны (или ее потенциала). Потеря отрицательного заряда клеткой ведет к открытию натриевых каналов — это важно для потенциала действия. Второй способ — действие химического вещества. Есть ацетилхолиновые каналы, которые открываются под действием(угадайте сами чего)… Так нервные клетки передают сигнал о сокращении мышцам.
Представьте два входа в клуб и один отдельный выход из него. Перед каждым входом стоит фейсер, но в первом нет двери — там просто дверной проем, а у второго и третьего дверь есть и для нее нужен ключик. Первый вход — это пора, молекула воды подходит к нему и фейсер пропускает ее, но иногда в толпе воды может затеряться другая молекула, например, мочевина. Фейсер по ошибке пропускает ее, ну а что — за всеми не углядишь, и она попадает внутрь клетки. Ко второму входу подходит ион натрия, фейсер его пропускает, но войти он не может пока дверь не откроют ключом — изменением потенциала или ацетилхолином. У выхода из клуба тоже стоит фейсер, вот такой вот странный клуб, к нему подходит ион калия и ждет пока дверь откроется таким же ключом. Фейсеры — это часть канала или поры, которая отвечает за узнавание ионов и молекул, а дверь или проем — это сам канал. Ну вы поняли.
Почему клеткам просто не забить: убрать фейсеров и держать двери постоянно открытыми? Смотрите — внутри клетки много калия, но мало натрия. В межклеточном веществе наоборот, очень много натрия и мало калия. А это значит, что калий стремится сбежать из клетки, а натрий войти в клетку.
Во-первых, такая разница ионов создает заряд внутри клетки — отрицательный, если бы каналы были постоянно открыты, то такой разницы бы не существовало, клетка стала бы незаряженной. Что не очень хорошо, так как она не сможет создать потенциал действия. Во-вторых, натрий это любимчик воды и если в клетке его будет много, то будет много и воды. Клетка просто лопнет от такой тусовки.
Облегченная диффузия
Здесь молекуле, которая идет тоже по градиенту концентрации, необходим переносчик. Все это из-за того, что молекула слишком большая для перехода через мембрану самостоятельно. Переносчик — это интегральный белок, который пронизывает мембрану, у него тоже есть фейсер (только здесь это участок связывания). При взаимодействии молекулы с переносчиком — он изменяет свою структуру (конформационные изменения белка) и переносит молекулу в клетку, а затем возвращается обратно.
Такой механизм характерен для переносчиков глюкозы — ГЛЮТов в жировой и мышечной ткани. Однако ГЛЮТы не всегда находятся на поверхности клетки, а только после еды — повышенный уровень глюкозы в крови вызывает секрецию инсулина из Б-клеток островков Лангерганса. Инсулин действует на жировую и мышечную ткань и взывает к ГЛЮТам, которые встраиваются в мембрану. Ой, как-то на автомате получилось. Еще таким способом транспортируются аминокислоты.
Смотрите, еще один прикол. Эти переносчики могут работать в обе стороны, все зависит от градиента концентрации глюкозы. Если ее будет слишком много в клетке, то они могут выкидывать ее в кровь. Прикольненько?
Если интересно, что быстрее: диффузия или облегченная диффузия, то вот график. Видим, что вначале быстрее облегченная диффузия, а потом обычная. Почему? Просто белки могут связать только одну молекулу, когда молекул глюкозы становится очень много, то все переносчики связаны с ней. Наступает насыщение переносчиков, и они не могут быстрее работать. Диффузия же не зависит от переносчиков, но она немного медленнее.
Пассивный транспорт все, поэтому давайте суммируем все и добавим в нашу начальную схему.
Активный транспорт
Здесь для переноса вещества через мембрану необходимо приложить энергию. Но зачем, а главное почему? Потому что такой транспорт идет против градиента концентрации, а без прикладывания энергии молекулу или ион просто не вытолкнуть. Разделяется на два варианта: первично-активный транспорт и вторично-активный транспорт, отличие между ними поймете чуть ниже.
Первично-активный транспорт
Здесь для того, чтобы перенести молекулы/ионы вещества на другую сторону мембраны используется энергия молекул АТФ. Классический вариант — натрий-калиевый насос. Этот насос представляет из себя белок, а именно фермент — АТФазу (помните, что «не все белки — ферменты, но все ферменты — белки» — десятая заповедь от кафедры биохимии). Занимается тем, что переносит ионы натрия из клетки, а ионы калия внутрь клетки. То есть работает против градиента концентрации, ведь натрия очень много вне клетки, а калия наоборот мало.
У насоса есть участки связывания — два для калия и три для натрия. Состоит из двух субъединиц — альфа и бета, альфа это и есть переносчик, а бета похоже якорит его в мембране. На один цикл: переноса трех ионов натрия из клетки и двух ионов калия внутрь клетки, требуется одна молекула АТФ. Как видим, этот насос создает разницу потенциалов, так как в обмен на три заряженных иона внутрь клетки поступает только два — этому пареньку мы обязаны за отрицательный заряд внутри клетки. Действует такой насос во всех клетках, он не дает клетке лопнуть из-за избытка натрия (вспоминаем про воду).
Кроме такого насоса есть еще несколько — Ca ++ и H + — АТФазы. Избыток кальция вредит клетке, так как он может запустить апоптоз. Водородный насос действует в париетальных клетках желудка и дистальном отделе канальца нефрона — в первом случае он создает кислую среду в желудке для функционирования пепсина. Да и вообще, из внешней среды поступает много всякой заразы, которой неприятно встречаться с кислотой. Во втором случае насос перемещает ионы водорода в просвет канальца. Полезная штука, а то прикинь — позанимался спортом и умер от ацидоза, не круто.
Вторично-активный транспорт
Тут одна молекула идет по градиенту концентрации и энергия, которая создается ей, используется для переноса другой молекулы. Представляете, сколько всего ионов натрия во внеклеточной жидкости? Вот и я не представляю, но очень много, а в клетке же наоборот его очень мало. Такая разница создает просто огромную энергию, которая идет на работу белка переносчика. Этот белок переносчик, как вы уже поняли — интегральный белок и имеет два участка связывания. Эти участки могут находиться на одной стороне белка или на разных. Поэтому такой транспорт можно разделить на два варианта:
1) Молекула, которая идет против градиента концентрации, переносится в одну сторону с молекулой, которая идет по градиенту концентрации. Это называется котранспорт (или симпорт). Так переносятся молекулы глюкозы и аминокислот из кишечника и канальцев нефрона. Натрий идет по градиенту концентрации внутрь клетки и захватывает с собой глюкозу или аминокислоты. Тут ты можешь сказать : «Чет странно, ведь в кишке много глюкозы после еды, почему она идет против градиента?». И да, это верно, в кишечнике много глюкозы. Но клеток очень много, а глюкоза растянута по всей поверхности кишки. Вот и получается, что в кишке ее много, но возле каждой клетки маловато. Такая же тема с аминокислотами.
2) Молекула идет против градиента концентрации, но не в одну сторону с переносимым по градиенту концентрации веществом — контртранспорт (или антипорт). Так происходит транспорт ионов водорода в проксимальных канальцах нефрона: водород попадает в просвет канальца, а натрий внутрь клетки.
Заметили кое-что? Клетка всегда чего-то боится: потерять или перебрать. Не всосать глюкозу и аминокислоты в кишечнике, либо смыть их в унитаз. И здесь она работает не только на свое благо, а на благо всего организма. Ведь ей не очень и нужна эта глюкоза, в ней ее достаточно, но она заботится не только о себе. А говорят, что коммунизм не построить , а он уже существует в организме каждого из нас. Ну это так, просто к слову пришлось… Перебрать же она боится, потому что из-за этого погибнет — поэтому натрий-калиевый насос работает постоянно, как и кальциевый.
Ну что сведем все это опять в нашу табличку?
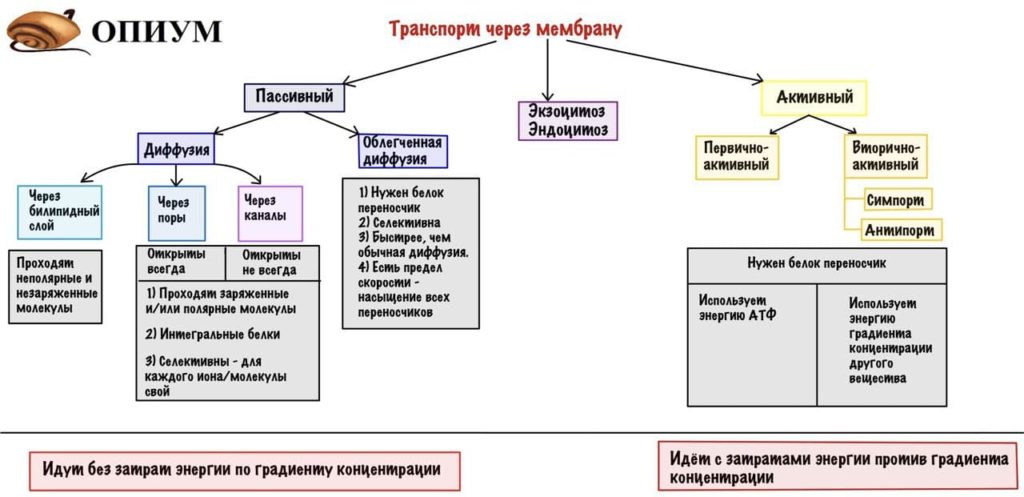
Все что мы разбирали до этого относится к небольшим по размерам молекулам, а что делать с большими? Для этого есть две легенды, о которых ниже.
Экзоцитоз и эндоцитоз
Начнем с экзоцитоза и сделаем это на каком-нибудь примере. Пусть это будут пищеварительные ферменты в поджелудочной железе. Синтезировала значит клетка липазу, но она ведь внутри клетки — это значит проку от нее мало. Нужно ее как-то переместить в проток поджелудочной железы, хорошо было бы использовать белок переносчик. А тут проблемка. Липаза слишком большая — ее не засунуть в белок переносчик. Но ничего — у клетки есть выход.
Все ферменты, белки плазмы, пептидные гормоны и так далее, синтезируются в упаковке — пузырьке (по строению он амфифильный). Оно и правильно, представьте — липаза попадает в цитоплазму клетки и просто переваривает ее. Эти пузырьки направляются к мембране, сливаются с ней и попадают в кровь, межклеточное вещество или проток поджелудочной железы. В общем куда им надо, туда они и попадают.
Теперь эндоцитоз. Все тоже самое только наоборот — это мое лучшее объяснение… Ладно, шутки кончились. На клеточной мембране есть определенный участок с рецепторами — окаймленная ямка. На рецепторах накапливаются макромолекулы, а потом ямка погружается в клетку и охватывает их, образуя пузырек. Этот пузырек направляется к лизосоме, где из него образуются мономеры. Эти мономеры клетка использует по своему усмотрению. Посмотрите картинку и все поймете, базарю.
Таким способом идет фагоцитоз лейкоцитами, а еще так в клетку попадают липопротеиды низкой плотности — это переносчики холестерина и жирных кислот.
Транспорт через несколько слоев клеток
Буквально пару слов. Разберем на примере кишки — там несколько слоев (три, ну ладно — четыре, если с подслизистой). Через все должна пройти глюкоза, но как? Это похоже на эстафету: сначала из кишечника вторично-активным транспортом глюкоза попадает в клетку, потом в следующую клетку уже по облегченной диффузии. Так она доходит до крови, а дальше уже идет по своим делам. Всё!
Хочешь задать вопрос, похвалить или наговорить гадостей? Тогда залетай в телегу. Там ты сможешь предложить новый формат или разбор темы. А если серьёзно, то эти статьи пишутся для вас, поэтому мне важна обратная связь.
Источник